
【题目】下列情况会对人体健康造成较大危害的是
A.用SO2漂白木耳制成银耳
B.用漂白粉[Ca(ClO)2]稀溶液对餐具进行杀菌消毒
C.用食醋清洗热水瓶胆内壁附着的水垢(CaCO3)
D.用小苏打(NaHCO3)发酵面团制作馒头
科目:高中化学 来源: 题型:
【题目】如图所示转化关系,A为单质,试对下列情况进行推断,并回答下列问题: 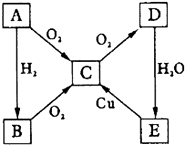
(1)A为固体时:
①A的化学式为 ,
②写出由C生成D的化学方程式 ,
③写出由E生成C的化学方程式;
(2)A为气体时:
①A的化学式为 ,
②写出由B生成C的化学方程式 ,
③写出由D生成E的离子方程式 ,
④写出由E生成C的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据键的成键特征,可判断出C=C键的键能与C-C键的键能的大小关系为( )
A.C=C键的键能等于C-C键键能的两倍
B.C=C键的键能大于C-C键键能的两倍
C.C=C键的键能小于C-C键键能的两倍
D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在,钴以Co2O3·CoO的形式存在,吸附在铝箔的单面或双面,锂混杂于其中。从废料中回收氧化钴(CoO)工艺流程如下:

(1)过程Ⅰ中采用NaOH溶液溶出废料中的Al,反应的离子方程式为________
(2)过程Ⅱ中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴。则浸出钴的化学反应方程式为 (产物中只有一种酸根)_________________
在实验室模拟工业生产时,也可用盐酸浸出钴,但实际工业生产中不用 盐酸,请从氧化还原和环境保护的角度分析不用盐酸浸出钴的主要原因是____________________
(3)过程Ⅲ得到锂铝渣的主要成分是LiF和Al(OH)3,碳酸钠溶液在产生Al(OH)3时起重要作用,请写出该反应的离子方程式__________________
(4)碳酸钠溶液在过程Ⅲ和Ⅳ中所起作用有所不同,请写出在过程Ⅳ中起的作用是______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能达到相应实验目的的是
选项 | 实验内容 | 实验目的 |
A | 将SO2通入紫色石蕊试液中,观察溶液是否褪色 | 验证有SO2有无漂白性 |
B | 用洁净的铂丝蘸取溶液进行焰色反应,火焰呈黄色 | 该溶液中一定含有钠盐 |
C | 常温下,测得浓度均为0.1mol/L溶液的pH:NaA>NaB | 证明常温下水解程度:A->B- |
D | 等体积、pH均为2的HA和HB两种酸分别与足量Zn反应,HA放出的H2多 | 证明HA是强酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水和苯不互相溶,苯不与钠反应,在烧杯中加水和苯,将一小块钠投入烧杯中,观察到的现象可能是
A. 钠在水层中反应并四处游动 B. 钠停留在苯层中不发生反应
C. 钠在苯的液面上反应并四处游动 D. 钠在苯与水的界面处反应,可能做上下跳动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,被还原的物质和被氧化的物质的物质的量之比最大的是
A. 铜和稀硝酸3Cu+8HNO3(稀)=2NO↑+3Cu(NO3)2+4H2O
B. 二氧化锰和浓盐酸 MnO2+4HC1(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
C. 二氧化氮和水3NO2+H2O=2HNO3+NO
D. 氯气和氨气3Cl2+8NH3=N2+6NH4C1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外研究性学习小组拟用粗盐(含有少量杂质包括:泥沙、CaCl2、MgCl2、Na2SO4)经提纯后,配制0.4mol/L 450mL NaCl溶液.他们设计并实施了如下实验,请根据已学过的知识回答下列问题:
(1)取一定量的粗盐置于烧杯中加水溶解,所加的水量应为: . (填选项)
A.多加水配成较稀的溶液
B.加入适量的水至能溶解的固体溶解即止
(2)将(1)中配制的粗盐悬浊液过滤后取滤液加入过量的除杂试剂,如果除杂试剂可从下列六种溶液中选择 ①Na2CO3溶液 ②KOH溶液 ③AgNO3溶液 ④NaOH溶液 ⑤NaHCO3溶液 ⑥BaCl2溶液,则正确的试剂和加入的顺序应为 . (填选项,多选、少选、错选都不得分)
A.①②③B.②⑥⑤C.④⑥①D.①④⑥E.⑥①④F.⑥②⑤
将所得的悬浊液经过滤后取滤液加入足量的盐酸,充分反应后对混合溶液进行蒸发、过滤、洗涤、干燥操作,得到纯净的NaCl固体,请描述在蒸发操作过程中玻璃棒的作用是 .
(3)利用(2)中所得的NaCl固体继续配制所需溶液.在托盘天平上称量g NaCl固体.配制过程中需要使用的玻璃仪器有:烧杯、玻璃棒、和 .
(4)配制结束后同学们对实验中出现的某些错误操作,对最终配制的溶液浓度的影响进行了分析,则下列错误操作会导致最终配制溶液中NaCl的浓度相比0.4mol/L的偏差是:(填“偏大”、“偏小”、“无影响”)
①在上述(2)步中没有使用盐酸处理滤液,结果会 ,
②定容时俯视凹液面,结果会
③上下颠倒摇匀后液面低于刻度线,未及时加水至刻度线,结果会
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,W的最简单氢化物甲是一种能使湿润的红色石蕊试纸变蓝的无色气体,常用作制冷剂,Y的金属性是所有短周期主族元素中最强的,Z与X属于同一主族,Z与Y属于同一周期。
(1)元素W在周期表位置_______________;
(2)元素W的另一常见氢化物乙是一种高能燃料,为18电子微粒,乙的结构式为___________;
(3)X、Y、Z的原子半径由小到大为______________________;
(4)若X与Z的最外层电子数之和是W核外电子数的2倍,甲可与Z单质发生置换反应,产物之一可作化肥,其反应的化学方程式为_______________,该产物化肥中含有的化学键有______________________。
(5)若由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气味气体产生。则元素Z是____元素,反应的离子方程式为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com