
| A、高铁酸钾与水反应时,水发生氧化反应 |
| B、干法制备中,每生成1mol Na2FeO4,共转移4mol电子 |
| C、湿法制备中,每生成1mol Na2FeO4,共转移3mol电子 |
| D、K2FeO4处理水时,不仅能杀菌,还能除去等H2S、NH3,并使悬浮杂质沉降 |


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤 | 解释或实验结论 |
| (1)测得A的蒸气密度是同状况下甲烷的4.375倍 | 试通过计算填空: (1)A的相对分子质量为 |
| (2)将此A 5.6g在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重7.2g和17.6g | (2)A的实验式是 (3)A的分子式为 |
| (3)将A通入溴水中,溴水褪色 | (4)说明A属于 |
(4)A的核磁共振氢谱如图: | (5)综上所述,A的结构简式为 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在100℃、101kPa条件下,1mol液态水气化时需要吸收40.69kJ的热量,则H2O(g)?H2O(l)的△H=+40.69kJ?mol-1 | ||||||||
| B、已知CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-802.33kJ/mol,则CH4的燃烧热为802.33kJ | ||||||||
C、H2(g)+Br2(g)═2HBr(g)△H=-72kJ?mol-1其它相关数据如表:
| ||||||||
| D、已知S(g)+O2(g)=SO2(s);△H1,S(g)+O2(g)=SO2(g);△H2,则△H2<△H1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件下关于离子存在的说法中正确的是( )
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件下关于离子存在的说法中正确的是( )| A、a点对应的溶液中大量存在:Na+、Ba2+、Fe3+、Cl- |
| B、b点对应的溶液中大量存在:NH4+、K+、I-、NO3- |
| C、c点对应的溶液中大量存在:Cu2+、Na+、Cl-、S2- |
| D、d点对应的溶液中大量存在:K+、AlO2-、ClO-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶解 过滤 蒸发结晶 |
| B、加热 溶解 过滤 |
| C、溶解 过滤 蒸馏 |
| D、溶解 过滤 分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6kJ?mol-1 |
B、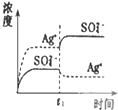 表示向Ag2SO4饱和溶液中加入等体积Na2SO4稀溶液,平衡会向左移动,Ksp减小 |
C、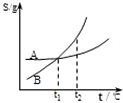 表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1℃升温至t2℃时,溶质的质量分数B>A |
D、 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除去乙烷中混有的乙烯的方法是通氢气在一定条件下反应,使乙烯转化为乙烷 |
| B、苯、溴苯在常温、常压下为无色且密度比水小的液体 |
| C、丙烯与2-丁烯都存在順反异构体 |
| D、苯不能与溴水发生加成反应,也不能被酸性KMnO4溶液氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、胶体能发生电泳现象是因为胶体带电 |
| B、生石灰与水混合的过程只发生物理变化 |
| C、O3是由3个氧原子构成的化合物 |
| D、CuSO4?5H2O是一种混合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com