
【题目】室温时,向20mL0.1molL﹣1的醋酸溶液中不断滴人0.1molL﹣1的NaOH溶液,溶液的pH变化曲线如图所示.在滴定过程中,关于溶液中离子浓度大小关系的描述不正确的是( ) 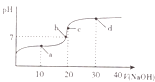
A.a点时:c( CH3COOH)>c( Na+)>c( CH3COO﹣)>c( H+)>c( OH ﹣)
B.b点时:c( Na+)=c( CH3COO﹣)>c(H+)=c( OH﹣)
C.c点时:c(H+)=c(CH3COOH)+c( OH﹣)
D.d点时:c(Na+)>c(CH3COO ﹣)>c(OH﹣)>c(H+)
【答案】AC
【解析】解:A.a点时醋酸过量,溶液为CH3COOH和CH3COONa的混合物,溶液呈酸性,应存在c(CH3COO﹣)>c(CH3COOH),故A错误;B.b点由溶液电荷守恒可知溶液中应存在c(Na+)+c(H+)=c(CH3COO﹣)+c(OH﹣),溶液呈中性,应有c(H+)=c(OH﹣),则c(Na+)=c(CH3COO﹣),故B正确;
C.c点时,溶液呈碱性,应有c(H+)<c(OH﹣),所以c(H+)<c(CH3COOH)+c(OH﹣),故C错误;
D.d点为NaOH和CH3COONa的混合物,溶液呈碱性,由于CH3COO﹣存在微弱的水解,则有c(Na+)>c(OH﹣)>c(CH3COO﹣)>c(H+),故D正确.
故选AC.
A.a点溶液为CH3COOH和CH3COONa的混合物,溶液呈酸性;
B.根据电荷守恒进行判断;
C.c点时,溶液呈碱性;
D.d点为NaOH和CH3COONa的混合物,溶液呈碱性.


科目:高中化学 来源: 题型:
【题目】利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品.
(1)有科学家提出可利用FeO吸收和利用CO2 , 相关热化学方程式如下:6FeO(s)+CO2(g)=2Fe3O4(s)+C(s)△H=﹣76.0kJmol一1
上述反应中每生成1mol Fe3O4 , 转移电子的物质的量为mol.
(2)在一定条件下,二氧化碳转化为甲烷的反应如下:
CO2(g)+4H2 (g) C H4 (g)+2H2O(g),向一容积为2L的恒容密闭容器中充人一定量的CO2和H2 , 在300℃时发生上述反应,达到平衡时各物质的浓度分别为CO2 0.2molL一1 , H2 0.8molL一1 , CH40.8molL一1 , H2O1.6molL一1 . 则CO2的平衡转化率为300℃时上述反应的平衡常数K= . 200℃时该反应的平衡常数K=64.8,则该反应的△H(填“>’’或“<”)O.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)常温下某溶液中由水电离出的离子浓度符合c(H+)c(OH﹣)=1×10﹣20的溶液,其pH为 , 此时水的电离受到
(2)在某温度下,H2O的离子积常数为1×10﹣13 mol2L﹣2 , 则该温度下:100mL 0.1molL﹣1H2SO4溶液与100mL 0.4molL﹣1的KOH溶液混合后,pH= .
(3)已知一溶液有4种离子:X+、Y﹣、H+、OH﹣ , 下列分析结果肯定错误的是
A.c(Y﹣)>c(X+)>c(H+)>c(OH﹣)
B.c(X+)>c(Y﹣)>c(OH﹣)>c(H+)
C.c(H+)>c(Y﹣)>c(X+)>c(OH﹣)
D.c(OH﹣)>c(X+)>c(H+)>c(Y﹣)
(4)在25℃下,将a molL﹣1的氨水与0.01molL﹣1的盐酸等体积混合,反应时溶液中c(NH4+)=c(Cl﹣).则溶液显(填“酸”“碱”或“中”)性;用含a的代数式表示NH3H2O的电离常数Kb= .
(5)水溶液中的行为是中学化学的重要内容.已知下列物质的电离常数值:
HClO:Ka=3×10﹣8 H2CO3:Ka1=4.3×10﹣7 Ka2=5.6×10﹣11;84消毒液中通入少量的CO2 , 该反应的化学方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质一定属于同系物的是( )
① ![]() ②
② ![]() ③
③ ![]() ④C2H4 ⑤CH2=CH﹣CH=CH2 ⑥C3H6 ⑦
④C2H4 ⑤CH2=CH﹣CH=CH2 ⑥C3H6 ⑦ ![]() ⑧
⑧ ![]()
A.①和②
B.④和⑥
C.①和③
D.④和⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若将阿伏加德罗常数规定为0.024kg12C中所含有的C原子数,而其他概念和规定一律不变,则下列各项的数值不会发生变化的是( )
A.物质的量
B.相对原子质量
C.物质的摩尔质量
D.12g12C中所含有的C原子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】油脂是重要的工业原料.关于“油脂”的叙述错误的是
A.不能用植物油萃取溴水中的溴
B.皂化是高分子生成小分子的过程
C.和H2加成后能提高其熔点及稳定性
D.水解可得到丙三醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有反应:mA(g)+nB(g)pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)m+np(填“>”“=”“<”).
(2)若加压时,A的质量分数 . (填“增大”“减小”或“不变”,下同)
(3)若加入A(体积不变),则B的转化率 .
(4)若降低温度,则平衡时B、C的浓度之比 ![]() 将 .
将 .
(5)若加入催化剂,平衡时气体混合物的总物质的量 .
(6)若B是有色物质,A、C均无色,维持容器内压强不变,充入氖气时,混合物颜色(填“变深”“变浅”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.230Th和232Th是钍的两种同素异形体
B.H2与T2互为同位素
C.甲醇与乙二醇互为同系物
D.乙酸乙酯与丁酸互为同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com