
| Ka1 | Ka2 | |
| H2A | 1.3��10-2 | 6.3��10-6 |
| H2B | 4.2��10-7 | 5.6��10-7 |
| A�� | H2A�ĵ��뷽��ʽ��H2A�T2H++A2- | |
| B�� | �����£���ˮ��Na2B��ˮ��ƽ�ⳣ��Ϊ��Ka1=$\frac{K_W}{{4.2��{{10}^{-7}}}}$ | |
| C�� | ��Ũ�ȵ�Na2A��Na2B��Һ����ˮ���������H+Ũ�ȴ�С��ϵΪ��ǰ�ߴ��ں��� | |
| D�� | ��Na2B��Һ�м�������H2A��Һ���ɷ�����Ӧ��B2-+H2A=A2-+H2B |
���� A��H2A�Ƕ�Ԫ���ᣬ����ֲ���ɣ����Ե��뷽��ʽ��H2A?H++HA-��
B��Na2B��ˮ�ⷽ��ʽΪ��B2-+H2O?HB-+OH-��K=$\frac{c��H{B}^{-}��•c��O{H}^{-}��}{c��{B}^{2-}��}$���м��㣻
C��HA-�ĵ���ƽ�ⳣ��6.3��10-6��HB-�ĵ���ƽ�ⳣ��5.6��10-7�����Ե�Ũ�ȵ�Na2A��ˮ��̶�С��Na2B��Һ��ˮ��̶ȣ�
D���ɱ���֪��H2A����ǿ��H2B��������Na2B��Һ�м�������H2A��Һ���ɷ�����Ӧ��B2-+H2A=A2-+H2B��
��� �⣺A��H2A�Ƕ�Ԫ���ᣬ����ֲ���ɣ����Ե��뷽��ʽ��H2A?H++HA-����A����
B��Na2B��ˮ�ⷽ��ʽΪ��B2-+H2O?HB-+OH-������K=$\frac{c��H{B}^{-}��•c��O{H}^{-}��}{c��{B}^{2-}��}$=$\frac{c��H{B}^{-}��•c��O{H}^{-}��•c��{H}^{+}��}{c��{B}^{2-}��•c��{H}^{+}��}$=$\frac{{K}_{W}}{5.6��1{0}^{-7}}$����B����
C��HA-�ĵ���ƽ�ⳣ��6.3��10-6��HB-�ĵ���ƽ�ⳣ��5.6��10-7�����Ե�Ũ�ȵ�Na2A��ˮ��̶�С��Na2B��Һ��ˮ��̶ȣ����Ե�Ũ�ȵ�Na2A��Na2B��Һ����ˮ���������H+Ũ�ȴ�С��ϵΪ��ǰ��С�ں��ߣ���C����
D���ɱ���֪��H2A����ǿ��H2B��������Na2B��Һ�м�������H2A��Һ���ɷ�����Ӧ��B2-+H2A=A2-+H2B����D��ȷ��
��ѡD��
���� ���⿼����������ʵĵ��롢����ƽ�ⳣ����ˮ�����ӻ�����ȷ������ʵ����ص㣬�Ƚ����ף�


 ͬ����ϰ���ϴ�ѧ������ϵ�д�
ͬ����ϰ���ϴ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 10 | B�� | 11 | C�� | 12 | D�� | 13 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{a}{36V}$mol/L | B�� | $\frac{a}{18V}$mol/L | C�� | $\frac{a}{54V}$mol/L | D�� | $\frac{a}{27V}$mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
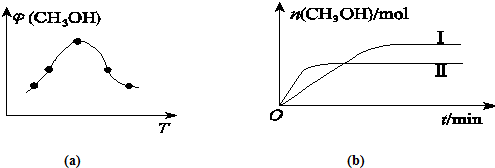
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaB��Һ��pH=8��c��Na+��-c��B-��=9.9��10-6mol•L-1 | |
| B�� | pH��ȵĢ�NH4C1���ڣ�NH4��2SO4����NH4HSO4������Һ�У�c��NH4+����С˳��Ϊ����=�ڣ��� | |
| C�� | Na2CO3��Һ�У�2c��Na+��=c��CO32-��+c��HCO3-��+c��H2CO3�� | |
| D�� | 10mLpH=12������������Һ�м���pH=2��HA��pH�պõ���7��������Һ���V���ܣ���20mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ֱͨ�������Һ�����ʷ��ӷֱ��������ƶ����������з�ɢ��������ijһ���ƶ� | |
| B�� | ��Fe��OH��3�����в��ϵμ�ϡ���ᣬ���ս���۳��������ɫ���� | |
| C�� | ����ͭ��Һͨ��һ������������������Һ��ͨ��һ����������һ��������ͨ· | |
| D�� | ��Һ���������ӵ��˶��й��ɣ����������˶����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | X/m mol | B�� | 2X/3mol | C�� | ��X+Y��mol | D�� | 2��X+Y��/3mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
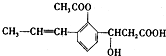 �������йظ��л��������˵������ȷ����
�������йظ��л��������˵������ȷ����| A�� | �������ֹ����� | |
| B�� | �ܷ���ȡ�����ӳɡ���ȥ�������ȷ�Ӧ• | |
| C�� | 1mol���л�����������2molNaOH��Ӧ | |
| D�� | ���л������ڷ����廯���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| �ܶȣ�g/cm3�� | �۵㣨�棩 | �е㣨�棩 | �ܽ��� | |
| ���Ҵ� | 0.96 | 25.93 | 161 | ������ˮ |
| ����ϩ | 0.81 | -103 | 83 | ������ˮ |
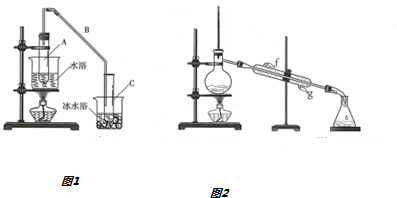
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com