
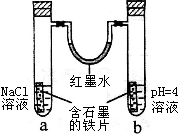
如右图装置所示,将装置放置一段时间。下列有关描述错误的是:
A.生铁块中的石墨是原电池的正极
B.红墨水柱两边的液面变为左低右高
C.两试管中相同的电极反应式是:Fe – 2e- = Fe2+
D.b试管中的正极反应是:2H+ +2e- = H2↑
 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| △ |
| ||
| △ |
| 2016×6 |
| 2688×5 |
| 2016×6 |
| 2688×5 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源:江苏省前黄高级中学2007届高三年级第一学期期中考试、化学试卷 题型:022
(1)下列有关实验操作或判断不正确的是________(填有关序号,选错倒扣分).
A、用10mL量筒量取稀硫酸溶液8.0mL
B、用干燥的pH试纸测定氯水的pH
C、用碱式滴定管量取KMnO4溶液19.60mL
D、使用容量瓶配制溶液时,俯视液面定容后所得溶液的浓度偏大
E、圆底烧瓶、锥形瓶、蒸发皿加热时都应垫在石棉网上
F、测定硫酸铜晶体中结晶水含量时,将加热后的坩埚置于干燥器中冷却后再称量
G.用冰醋酸,蒸馏水和容量瓶等仪器配制pH为1的醋酸稀溶液
(2)实验室利用如右图装置进行中和热的测定.

回答下列问题:
①该图中有两处未画出,它们是________、________;
②如果用0.5mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将(填“偏大”、“偏小”或“不变”);原因是________.
(3)在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:
2MnO4-+5C2O42-+16H+![]() 2Mn2++10CO2↑+8H2O
2Mn2++10CO2↑+8H2O
①用托盘天平称取WgNa2C2O4晶体.
②将WgNa2C2O4配成100mL标准溶液,移取20.00mL置于锥形瓶中,则酸性KMnO4溶液应装在________(填“酸式”或“碱式”)滴定管中.
③若滴定管的起始读数和终点读数如图所示,则酸性KMnO4的物质的量浓度为________(填表达式).
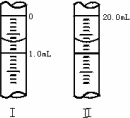
④若滴定完毕立即读数,测定的KMnO4溶液的浓度________(填“偏高”“偏低”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
(7分)制备溴苯的实验装置如右图所示,回答下列问题:
(1)反应开始前已向仪器A中加入的是药品是 。装在左侧分液漏斗中的药品是 。
(2)将左侧分液漏斗的旋纽打开后,在A中可观察到的现象是 。
(3)右侧分液漏斗中的物质在什么时间加入A中? 。其作用是 。
(4)要证明该反应是取代反应,最方便的实验方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(共22分)
Ⅰ.(4分)下列实验操作中,合理的是
A.实验室制乙烯时,在酒精和浓硫酸的混合液中,放入几片碎瓷片,加热混合物,使液体温度迅速升到170℃
B.验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置,待液体分层后,滴加硝酸银溶液
C.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入无水乙醇中,完成乙醇氧化为乙醛的实验
D.苯酚中滴加少量稀溴水,可用来定量检验苯酚
E.工业酒精制取无水酒精时,先加生石灰然后蒸馏,蒸馏必须将温度计的水银球插入反应液中,测定反应液温度
Ⅱ.(10分)实验室用下图所示装置制备溴苯,并验证该反应是取代反应。
(1) 关闭F活塞,打开C活塞,在装有少量苯的三颈瓶中由A口加入少量溴,再加入少量铁屑,塞住A口,则三颈瓶中发生反应的化学方程式为: 。
(2) D试管内装的是 ,其作用是 。
(3) E试管内装的是 ,E试管内出现的现象为 。
(4) 待三口烧瓶中的反应即将结束时(此时气体明显减少),打开F活塞,关闭C活塞,可以看到的现象是 。
(5) 上一步得到粗溴苯后,要用如下操作精制:
a蒸馏; b水洗; c用干燥剂干燥; d 10%NaOH溶液洗涤; e水洗
正确的操作顺序是
Ⅲ.(8分)用如右图所示装置进行实验,将A逐滴加入B中:
(1) 若B为Na2CO3粉末,C为C6H5ONa溶液,实验中观察到小试管内溶液由澄清变浑浊,则试管C中化学反应的离子方程式:________________ 。然后往烧杯中加入沸水,可观察到试管C中的现象: 。
(2) 若B是生石灰,观察到C溶液中先形成沉淀,然后沉淀溶解.当沉淀完全溶解,恰好变澄清时,关闭E.然后往小试管中加入少量乙醛溶液,再往烧杯中加入热水,静置片刻,观察到试管壁出现光亮的银镜,则A是 (填名称),C是 (填化学式),与乙醛的混合后,该溶液中反应的化学方程式: _____________。仪器D在此实验中的作用是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com