
 ,
, ;
;

科目:高中化学 来源: 题型:
| 溶液中检测出的溶质 | |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、BaCl2、Na2CO3、NaCl |
| 第三次 | KCl、K2CO3、Na2SO4、NaCl |
| 实验步骤 | 实验操作 | 实验目的 | 反应的离子方程式 |
| 第一步 | 向溶液中滴加过量的硝酸 | 检验① |
② |
| 第二步 | 继续滴加过量的 ③ |
检验SO42-的存在 | ④ |
| 第三步 | 过滤,再向滤液中滴加 ⑤ |
检验 ⑥ |
Ag++Cl-=AgCl↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
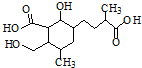 (1)书写化学方程式:①苯乙烯加聚反应;②丙烯与溴的加成反应
(1)书写化学方程式:①苯乙烯加聚反应;②丙烯与溴的加成反应查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 品 名 | 浓缩菠萝汁 |
| 配 料 | 水.浓缩菠萝汁.蔗糖.柠檬酸.黄原胶.甜蜜素.维生素C,菠萝香精.柠檬黄.日落黄.山梨酸钾等 |
| 果汁含量 | ≥80% |
| 生产日期 | 标于包装袋封口上 |
查看答案和解析>>
科目:高中化学 来源: 题型:
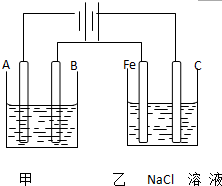 如图为相互串联的甲乙两个电解池,请回答:
如图为相互串联的甲乙两个电解池,请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com