
【题目】某无机盐X(仅含三种元素,原子个数比为1:1:4,摩尔质量270g·mol-1),为探究其组成和性质,某学习小组进行了如下实验,X与水反应只生成A、B两种物质,其中气体单质 A 能使带火星的木条复燃。下列说法正确的是:

(1)X的组成元素为 O和_____________(用元素符号表示)。
(2)X 的 化学式为____________。
(3)下列说法正确的是(NA为阿伏加德罗常数)_________ 。
a.酸式盐B的焰色反应颜色可以直接观察
b.盐X中的两种非金属元素所组成的氧化物都能使酸性高锰酸钾溶液褪色
c.1摩尔的固体B中含2NA个离子
d.氮气和气体单质A点燃即可发生反应
(4)X氧化能力极强,可用于脱硫脱硝,写出在碱性条件下X氧化SO32-的离子方程式____________。
【答案】K 、 S K2S2O8 C S2O8 2-+ SO32-+2OH-=3SO42-+ H2O
【解析】
单质 A 能使带火星的木条复燃,则A为O2,B焰色反应呈紫色,则含有K元素,B的酸性溶液与BaCl2反应产生白色沉淀,则B中含有SO42-,27gX物质的量为0.1mol,S元素物质的量![]() ,则S原子个数为
,则S原子个数为![]() ,结合摩尔质量和原子个数比推出分子式。
,结合摩尔质量和原子个数比推出分子式。
单质 A 能使带火星的木条复燃,则A为O2,B焰色反应呈紫色,则含有K元素,B的酸性溶液与BaCl2反应产生白色沉淀,则B中含有SO42-,27gX物质的量为0.1mol,S元素物质的量![]() ,则S原子个数为
,则S原子个数为![]() ,原子个数比为1:1:4,摩尔质量270g·mol-1,则化学式为K2S2O8,
,原子个数比为1:1:4,摩尔质量270g·mol-1,则化学式为K2S2O8,
(1)X的组成元素为 O和K 、 S,
故答案为:K 、 S;
(2)由上述推断可知X 的化学式为K2S2O8,
故答案为:K2S2O8;
(3)a.K的焰色反应需透过蓝色钴玻璃片观察,故a错误;
b.盐X中的两种非金属元素所组成的氧化物有SO2、SO3、H2O、H2O2;SO2和H2O2能使酸性高锰酸钾溶液褪色,SO3和H2O不能使酸性高锰酸钾溶液褪色,故b错误;
c. B为酸性溶液则B为KHSO4,固体B中含有K+和HSO4-离子,故1摩尔的固体B中含2NA个离子,故c正确;
d.氮气和O2不可点燃,故d错误 ;
故答案选:c;
(4)X氧化SO32-X为氧化剂,SO32-为还原剂,根据化合价升降守恒可得离子方程式为:![]() ,
,
故答案为:![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】工业上利用粗ZnO(含FeO、CuO)制取金属锌的流程如下(部分步骤省略):

已知:几种离子形成氢氧化物沉淀时的pH如下表:
待沉淀的离子 | Fe2+ | Fe3+ | Zn2+ | Cu2+ |
开始沉淀时pH | 6.3 | 1.5 | 6.2 | 5.2 |
沉淀完全时pH | 9.7 | 3.2 | 8.0 | 6.4 |
请回答下列问题:
(1)酸浸粗氧化锌的过程中,常将粗氧化锌粉碎成细颗粒,适当增加硫酸的浓度,目的是_________。
(2)步骤A的目的是将Fe2+氧化为Fe3+,并全部形成Fe(OH)3沉淀,为了暂不形成Cu(OH)2 Zn(OH)2 ,该步骤需控制溶液pH的范围是____________,该步骤中先加入H2O2充分反应后再加入氨水,写出加入H2O2的离子方程式_____________。
(3)步骤C的反应离子方程式为____________。
(4)若步骤A中加入H2O2后,室温下将溶液的pH调为4,求Fe3+ 离子浓度为_________。(已知Ksp[Fe(OH)3]= 4.0×10-3 8)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[Zn(CN)4]2-在水溶液中可与HCHO发生反应生成[Zn(H2O)4]2+和HOCH2CN,下列说法错误的是( )
A.Zn2+基态核外电子排布式为[Ar]3d10
B.1molHCHO分子中含有σ键的数目为3mol
C.HOCH2CN分子中碳原子轨道的杂化类型是sp3
D.[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,结构可表示为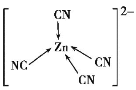
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家发现对冶金硅进行电解精炼提纯可降低高纯硅制备成本。相关电解装置如图所示,用Cu-Si合金作硅源,在950℃利用三层液熔盐进行电解精炼,有关说法正确的是
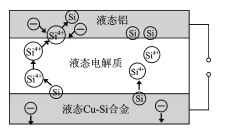
A.在该液相熔体中Cu优先于Si被氧化,Si4+优先于Cu2+被还原
B.液态Cu-Si合金作阳极,固体硅作阴极
C.电流强度的大小不会影响硅提纯速率
D.三层液熔盐的作用是增大电解反应接触面积,提高硅沉积效率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有学生将铜与稀硝酸反应实验及NO、NO2性质实验进行改进、整合,装置如图(洗耳球:一种橡胶为材质的工具仪器)。

实验步骤如下:
(一)组装仪器:按照如图装置连接好仪器,关闭所有止水夹;
(二)加入药品:在装置A中的烧杯中加入30%的氢氧化钠溶液,连接好铜丝,在装置C的U型管中加入4.0 mol/L的硝酸,排除U型管左端管内空气;
(三)发生反应:将铜丝向下移动,在硝酸与铜丝接触时可以看到螺旋状铜丝与稀硝酸反应产生气泡,此时打开止水夹①,U型管左端有无色气体产生,硝酸左边液面下降与铜丝脱离接触,反应停止;进行适当的操作,使装置C中产生的气体进入装置B的广口瓶中,气体变为红棕色;
(四)尾气处理:气体进入烧杯中与氢氧化钠溶液反应;
(五)实验再重复进行。
回答下列问题:
(1)实验中要保证装置气密性良好,检验其气密性操作应该在____。
a.步骤(一)(二)之间 b.步骤(二)(三)之间
(2)装置A的烧杯中玻璃仪器的名称是____。
(3)加入稀硝酸,排除U型管左端管内空气的操作是________。
(4)步骤(三)中“进行适当的操作”是打开止水夹____(填写序号),并用洗耳球在U型管右端导管口挤压空气进入。
(5)在尾气处理阶段,使B中广口瓶内气体进入烧杯中的操作是____。尾气中主要含有NO2和空气,与NaOH溶液反应只生成一种盐,则离子方程式为 ___。
(6)某同学发现,本实验结束后硝酸还有很多剩余,请你改进实验,使能达到预期实验目的,反应结束后硝酸的剩余量尽可能较少,你的改进是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是自然界碳循环中的重要物质。下列过程会引起大气中CO2含量上升的是
A. 光合作用 B. 自然降雨
C. 化石燃料的燃烧 D. 碳酸盐的沉积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积固定的密闭容器中加入反应物N2、H2,发生反应:N2(g)+3H2(g)![]() 2NH3(g)。反应过程中的部分数据如表所示:
2NH3(g)。反应过程中的部分数据如表所示:

下列说法正确的是
A.0~2min内,H2的反应速率为0.1 mol/(L·min)
B.2min时,NH3的物质的量浓度为0.2 mol/L
C.4min时,反应已达到平衡状态,此时正、逆反应的速率都为0
D.4~6min内,容器内气体分子的总物质的量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法错误的是
A. PM2.5是指粒径不大于2.5μm的可吸入悬浮颗粒物
B. 绿色化学要求从源头上消除或减少生产活动对环境的污染
C. 燃煤中加入CaO可以减少酸雨的形成及温室气体的排放
D. 天然气和液化石油气是我国目前推广使用的清洁燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在体积均为20mL、浓度均为0.1mol·L-1的HX溶液、HY溶液中分别滴加同浓度的NaOH溶液,反应后溶液中水电离的c(H+)表示为pH水=-lgc(H+)水。pH水与滴加氢氧化钠溶液体积的关系如图所示。
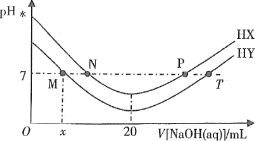
下列推断正确的是
A.HX的电离方程式为HX=H++X-
B.T点时c(Na+)=c(Y-)>c(H+)=c(OH-)
C.常温下用蒸馏水分别稀释N、P点溶液,pH都降低
D.常温下,HY的电离常数![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com