
| A | B | C | D |
 |  |  | 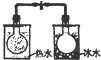 |
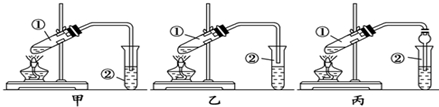
| 根据电流表(A)中指针是否偏转即可比较Zn,Cu的金属活泼性 | 根据小试管中液面的变化可判断铁钉发生了析氢腐蚀 | 根据温度计读数的变化测定浓硫酸和NaOH溶液反应的反应热 | 根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)判断2NO2(g)?N2O4(g)是吸热反应 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.原电池中活泼性强的为负极;
B.中性溶液在铁发生吸氧腐蚀;
C.浓硫酸溶解放热;
D.升高温度向吸热方向移动,溶液变深.
解答 解:A.Zn、Cu形成原电池,锌活泼性强的为负极,检流计的指针偏向正极Cu,所以能够根据指针偏向确定正负极,即可判断金属性强弱,故A正确;
B.在氯化钠溶液中铁发生吸氧腐蚀,试管中压强减小,导管中液面上升,不是发生的析氢腐蚀,故B错误;
C.浓硫酸溶解放热,所以用浓硫酸和NaOH反应测定中和热,测定的数值偏大,应该用稀硫酸或稀盐酸,故C错误;
D.热水中变深、冰水中变浅,说明升高温度向逆方向移动,则逆方向为吸热反应,则正方向为放热反应,故D错误.
故选A.
点评 本题考查了原电池原理、铁的电化学腐蚀、中和热的测定、温度对平衡的影响,题目涉及的知识点较多,侧重于对基础知识的综合考查,难度中等.


科目:高中化学 来源: 题型:解答题
 ,该化合物中含有的化学键是共价键、离子键.
,该化合物中含有的化学键是共价键、离子键.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子中3个碳原子在同一直线上 | B. | 分子中所有原子在同一平面上 | ||
| C. | 与氯化氢加成只生成一种产物 | D. | 能发生加聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
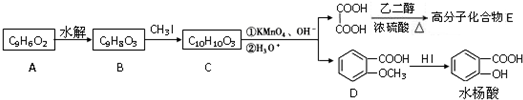
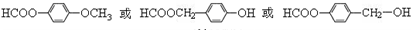 .
.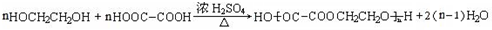 .
.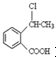 为原料制备
为原料制备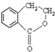 的合成路线流程图(无机试剂任用),并注明反应条件.合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2$\stackrel{Br_{2}}{→}$
的合成路线流程图(无机试剂任用),并注明反应条件.合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2$\stackrel{Br_{2}}{→}$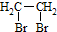 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 限制使用电动车 | |
| B. | 利用太阳能、风能和氢能等能源代替化石燃料 | |
| C. | 鼓励私人购买和使用汽车代替公交车 | |
| D. | 以煤等燃料作为主要生活燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 CH3COOC2H5+H2O;
CH3COOC2H5+H2O;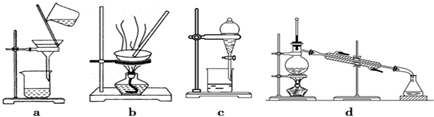
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com