
����Ŀ�����ǻ������ᶡ��(�׳��Ჴ����)���������������Խ�ĸ��ù���к�ǿ���������ã���ҵ�ϳ��ö��ǻ��������붡����Ũ������½���������Ӧ���Ƶá�������ij�����鿪���Ĵ����ۡ��õĻ���ԭ�ϳ����Ʊ����ǻ������ᶡ���ĺϳ�·�ߣ�
��֪������Ϣ��
��ͨ����ͬһ��̼ԭ�������������ǻ����ȶ�������ˮ�γ��ʻ���
��D����������Һ��Ӧ����������
��F�ĺ˴Ź������ױ����������ֲ�ͬ��ѧ�������⣬�ҷ������Ϊ1��1��
�ش��������⣺
��1��A�Ļ�ѧ����Ϊ��
��2����B����C�Ļ�ѧ��Ӧ����ʽΪ �� �÷�Ӧ������Ϊ��
��3��D�Ľṹ��ʽΪ��
��4��F�ķ���ʽΪ��
��5��G�Ľṹ��ʽΪ��
��6��E��ͬ���칹���к��б������ܷ���������Ӧ�Ĺ����֣����к˴Ź������������ֲ�ͬ��ѧ�������⣬�ҷ������Ϊ2��2��1����(д�ṹ��ʽ)��
���𰸡�
��1���ױ�
��2�� ������ȡ����Ӧ
������ȡ����Ӧ
��3��![]()
��4��C7H4O3Na2
��5��![]()
��6��13��![]()
��������(1)������֪AΪ�ױ������ݷ�Ӧ�����������̷ֱ�ȷ��B��C��D��E��F��G�Ľṹ��(2)�ɹ�������֪��B����C�ķ�ӦΪ����ȡ����Ӧ��(3)����Ϣ��֪  ����ȡ����Ӧ��Ȼ��ʧˮ����
����ȡ����Ӧ��Ȼ��ʧˮ���� 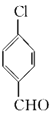 ��(4)EΪ
��(4)EΪ 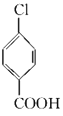 ���ڼ��������·�Ӧ����
���ڼ��������·�Ӧ����  ��(5)F�����������·�Ӧ���ɶ��ǻ������ᡣ(6)��������ͬ���칹�����д������ȩ�������б�������ע�ⱽ�����ڡ��䡢��λ�á�
��(5)F�����������·�Ӧ���ɶ��ǻ������ᡣ(6)��������ͬ���칹�����д������ȩ�������б�������ע�ⱽ�����ڡ��䡢��λ�á�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȥCl2��������HCl���壬���ѡ�õ��Լ���(����)
A. ����ˮ B. ��������
C. ����ʳ��ˮ D. ����������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��ҡ�����λͬѧ�ֱ�����������ʵ��װ�ü���ѧҩƷ�����м�ʯ��Ϊ�����������ƺ���ʯ�ҵĻ�����ȡ����������ش��������⣺ 
��1����λͬѧ��ȡ�����Ļ�ѧ����ʽΪ�� ��
��2����λͬѧ���������ſ������ռ���������ԭ���� ��
��3����λͬѧ������װ����ȡ����ʱ��������һλͬѧû���ռ�������������ǵ�ʵ���������ȷ��������Ϊû���ռ���������ͬѧ������ס������ҡ����������ռ�������������Ҫԭ�������û�ѧ����ʽ��ʾ����
��4�����鰱���Ƿ��ռ����ķ����ǣ�������������������ͽ��ۣ� ��
��5����λͬѧ����Ϊ���ǵ�ʵ��װ��Ҳ�����ڼ���̼����粒�����ȡ�����İ��������ж��ܹ��ﵽʵ��Ŀ��������ס������ҡ�����������װ���е�NH4HCO3�����ܷ���NH4Cl������棿����ܡ����ܡ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڿ��淴ӦA��g��+3B��g��2C��g��+2D��g�����ڲ�ͬ�����µĻ�ѧ��Ӧ�������£����б�ʾ�ķ�Ӧ���������ǣ�������
A.v��A��=0.5 molL��1min��1
B.v��B��=1.2 molL��1s��1
C.v��D��=0.4 molL��1min��1
D.v��C��=0.1 molL��1s��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ������գ�
��1��������A���еĹ�����Ϊ��
��2��1molA��2molH2��Ӧ����1molE���䷴Ӧ����ʽΪ��
��3����A������ͬ�����ŵ�A��ͬ���칹��Ľṹ��ʽ����
��4��B��������������Br2��Ӧ�õ�D��D��̼������֧������ṹ��ʽ����
��5��F�Ľṹ��ʽ������E��F�ķ�Ӧ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2014��7��31���й����������ӱ�ʡ��չ������������ר�������ж���ǿ�������ϡ�������ij������������Ҫ�ɷ�ΪSiO2��MgO��Al2O3��Fe2O3�ȳɷ֣����շ����еĽ���Ԫ�صĹ���������ͼ��ʾ�� 
��֪�������£����Ͱ�ˮ��pHԼΪ11���������ӳ�������pH���������ʾ��
���� | ������������ʽ��ȫ����ʱ����pH | �������������ȫ�ܽ�ʱ����pH |
Fe3+ | 3.2 | |
A13+ | 5.3 | 11.9 |
Mg2+ | 12.3 |
��1���Լ���Ϊ �� �Լ���Ϊ��
A��AgNO3 B��NaOH C��NH3H2O D��H2SO4
��2������C�Ļ�ѧʽ�� �� ��ҺF�н���Ԫ�صĴ�����ʽΪ��
��3��д������A���Լ��ڷ�Ӧ�Ļ�ѧ����ʽ����F��ͨ�����CO2�����������ӷ���ʽΪ��
��4�������Լ��ڣ�ʵ����ҺD����ҺF��ת�����������Һ��pHΪ ��
A.6
B.10
C.12
D.13
��5��25��ʱ������4������pH������ҺF��c��Mg2+��=5.6��10��10mol/L����������þ��Ksp=��
��6�����һ����Ӧ���漰�������Σ�������ʽ�ε���Һ�и�����Ũ���ɴ�С��˳��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������CO2����ͨ��ˮ�����У�Ȼ��������ɣ����ڸ����³��ȼ�գ�������õĹ���������(����)
A. Na2SiO3 B. Na2CO3��Na2SiO3 C. Na2CO3��SiO2 D. SiO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�ʱ��2L������X��Y��Z������̬���ʵ����ʵ�����n����ʱ�䣨t���仯��������ͼ��ʾ����ͼ�����ݷ����� 
��1���÷�Ӧ�Ļ�ѧ����ʽΪ�� ��
��2����Ӧ��ʼ��2min����Z��ʾ��ƽ����Ӧ����Ϊ�� ��
��3����������ʵ�У�ʲô����Ӱ���˻�ѧ��Ӧ�����ʣ� ��ͬŨ�ȡ�ͬ����������з����С��ͬ����Ƭ��þƬ���������п���������
���ۻ���KClO3�ų����ݺ�������������MnO2�ܿ�������壺 ��
��4�����ܱ������ͨ��a mol X��g����b mol Y��g����������ӦX��g��+Y��g��2Z��g�������ı���������ʱ����Ӧ���ʻᷢ��ʲô�仯����ѡ���������С�����䡱�� �������¶ȣ���Ӧ������
�ڱ�������������䣬���벻�μӷ�Ӧ�Ķ������壬��Ӧ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ú˴Ź������ⶨ�л�����ӵ���ά�ṹ���о������2002��ŵ������ѧ�������л�������У���ͬ��ԭ�ӵĺ˴Ź������и����ķ�ֵ���źţ�Ҳ��ͬ�����ݷ�ֵ���źţ�����ȷ���л����������ԭ�ӵ��������Ŀ����������ѵĽṹ��ʽΪ��CH3��CH2��O��CH2��CH3 �� ��˴Ź������и����ķ�ֵ���źţ�����������ͼ��ʾ�� 
��1�����������У���˴Ź��������и����ķ�ֵ���źţ�ֻ��һ����������ѡ�۷֣���
A.CH3CH3
B.CH3COOH
C.CH3COOCH3
D.CH3OCH3
��2��CH3COOCH3������һ������д��������ŵķ��� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com