
| A、①② | B、①③ | C、②④ | D、③④ |


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
| A、950 mL,78 g |
| B、500 ml,80g |
| C、1 000 mL,80 g |
| D、1 000 mI.,76 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3CH2CH2OH和 CH3CH(OH)CH3 |
| B、CH3 CH(CH3)2和 CH3 CH2CH2CH3 |
| C、CH3CH2CHO和 CH3COCH3 |
| D、CH2=CHCH2CH2CH3和CH3CH2CH=CHCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
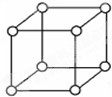 查资料表知,只有钋的晶体中的原子具有如图所示的堆积方式,钋的外围电子排布式是6s26p4.下列关于钋的说法错误的是( )
查资料表知,只有钋的晶体中的原子具有如图所示的堆积方式,钋的外围电子排布式是6s26p4.下列关于钋的说法错误的是( )| A、右图的堆积方式空间利用率太低,金属极少采取这种堆积方式 |
| B、钋晶体中原子的配位数为 6 |
| C、钋基态原子的能层数=周期序数=价电子数 |
| D、钋的常见化合价为+4、+6、-2价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
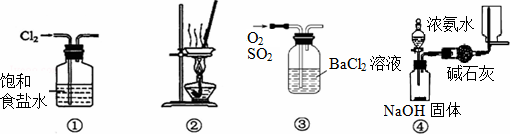
| A、用装置①除去Cl2中含有的少量HCl |
| B、用装置②从KCl溶液中获得KCl晶体 |
| C、用装置③除去O2中混有的一定量SO2 |
| D、用装置④在实验室制取并收集氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
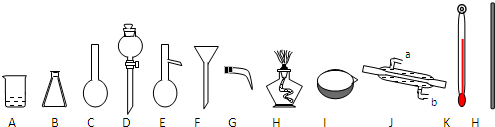
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com