
【化学-选修5有机化学基础】(15分)
咖啡酸苯乙酯 是一种天然抗癌药物。在一定条件下能发生如下转化。
是一种天然抗癌药物。在一定条件下能发生如下转化。

请回答下列问题:
(1)A分子中的官能团是_______________________________。
(2)高分子化合物M的结构简式是_______________________________。
(3)写出A→B反应的化学方程式:__________________________________。
(4)A→B的反应类型为__________;E→M的反应类型为________;B→C的反应类型为__________。
(5)A的同分异构体有很多种,其中同时符合下列条件的同分异构体有________种。
①苯环上只有两个取代基 ②能发生银镜反应
③能与碳酸氢钠溶液反应 ④能与氯化铁溶液发生显色反应
(1)羟基(或酚羟基)、羧基、碳碳双键(每个1分,共3分)
(4)取代反应 加聚反应 加成反应(每个2分,共6分) (5) 3(2分)
【解析】
试题分析:咖啡酸苯乙酯在稀硫酸的作用下水解生成A和D,根据A的分子式可知A的结构简式为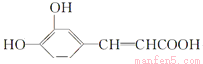 ,则D是苯乙醇。苯乙醇在浓硫酸的作用下发生消去反应生成E,则E是苯乙烯。苯乙烯含有碳碳双键,发生加聚反应生成M,则M的结构简式为
,则D是苯乙醇。苯乙醇在浓硫酸的作用下发生消去反应生成E,则E是苯乙烯。苯乙烯含有碳碳双键,发生加聚反应生成M,则M的结构简式为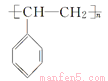 。A和甲醇发生酯化反应生成B,则B的结构简式为
。A和甲醇发生酯化反应生成B,则B的结构简式为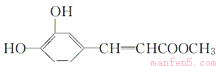 。B中含有碳碳双键与溴的四氯化碳溶液发生加成反应生成C。
。B中含有碳碳双键与溴的四氯化碳溶液发生加成反应生成C。
(1)根据以上分析可知A分子中的官能团是酚羟基、羧基、碳碳双键。
(2)根据以上分析可知高分子化合物M的结构简式是 。
。
(3)A→B是A与甲醇的酯化反应,反应的化学方程式为 。
。
(4)根据以上分析可知A→B的反应类型为取代反应;E→M的反应类型为加聚反应;B→C的反应类型为加成反应。
(5)A的同分异构体有很多种,其中同时符合下列条件的同分异构体有________种。
①苯环上只有两个取代基;②能发生银镜反应,说明含有醛基;③能与碳酸氢钠溶液反应,说明含有羧基;④能与氯化铁溶液发生显色反应,说明还含有酚羟基,则苯环上的取代基应该是—OH和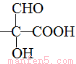 ,其位置是邻间对,共计3种同分异构体。
,其位置是邻间对,共计3种同分异构体。
考点:考查有机物推断、官能团、反应类型、同分异构体判断和方程式书写
考点分析: 考点1:有机化学知识综合应用 试题属性

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2014-2015学年山东省泰安市高三下学期一模理科综合化学试卷(解析版) 题型:实验题
硫酰氯(SO2Cl2)是一种化工原料,有如下有关信息:
常温下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气。氯化法是合成硫酰氯的常用方法,实验室合成反应和实验装置如下:

回答下列问题:
(1)仪器A的名称为______,甲中活性炭的作用是______,B中加入的药品是______。实验时从仪器C中放出溶液的操作方法是________。
(2)装置丁中发生反应的离子方程式为___________。用亚硫酸钠固体和浓硫酸制备二氧化硫气体时,如要控制反应速度,下图中可选用的发生装置是________(填写字母)。

(3)氯磺酸(C1SO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为_________________,分离产物的方法是_________。
(4)若缺少装置乙,氯气和二氧化硫可能发生反应的化学方程式为_______。为提高本实验中硫酰氯的产率,在实验操作中还需要注意的事项有(只答一条即可)_______。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省江门市高三3月模拟考试理科综合化学试卷(解析版) 题型:选择题
某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是

A.正极反应为Ag-e-=Ag+
B.放电时,交换膜右侧溶液中有大量白色沉淀生成
C.当电路中转移0.1mol e-时,通过交换膜的阳离子为0.2mol
D.用KCl溶液代替盐酸,则电池总反应不改变
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省六校高三3月联考化学试卷(解析版) 题型:填空题
选考[化学—选修物质结构与性质](15分)
前四周期元素A、B、C、D、E、F,原子序数依次增大,其中A和B同周期,固态的AB2能升华;C和E原子都有一个未成对电子,C+比E-少一个电子层,E原子得到一个电子后3p轨道全充满;D最高价氧化物中D的质量分数为40%,且核内质子数等于中子数;F为红色单质,有F+和F2+两种离子。回答下列问题:
(1)元素电负性:D____E (填>、<或=);
(2)A、C单质熔点A_____C(填>、<或=);
(3)AE4中A原子杂化轨道方式为:________杂化;其固态晶体类型为_______;
(4)F的核外电子排布式为______;向F的硫酸盐中逐滴加入氨水先产生沉淀,后沉淀溶解为深蓝色溶液,加入乙醇会析出蓝色晶体,该晶体中F与NH3之间的化学键为_______;
(5)氢化物的沸点:B比D高的原因______;
(6)元素X的某价态阴离子Xn-中所有电子正好充满K和L电子层,CnX晶体的最小结构单元如图所示。该晶体中阳离子和阴离子个数比为___,晶体中每个Xn-被__个等距离的C+离子包围。
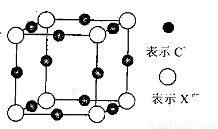
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省六校高三3月联考化学试卷(解析版) 题型:选择题
类推的思维方法在化学学习与研究中经常用到,但有时会产生错误的结论。因此,推出的结论最终要经过实践的检验才能决定其是否正确。以下几种类推结论中,正确的是
A.IVA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则VA族元素氢化物沸点顺序也是:AsH3>PH3>NH3
B.第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3
C.Fe3O4可以写成FeO·Fe2O3;Pb3O4也可以写成PbO·Pb2O3
D.NaHSO4与NaHSO3溶于水显酸性,则所有酸式盐溶于水显酸性
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省长望浏宁四县高三一模考试化学试卷(解析版) 题型:实验题
(14分)过碳酸钠(2Na2CO3·3H2O2)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂。某兴趣小组制备过碳酸钠的实验方案和装置示意图如下:
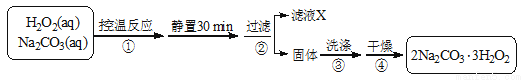
已知:主反应:2Na2CO3 (aq) + 3H2O2 (aq)  2Na2CO3·3H2O2 (s) ΔH < 0
2Na2CO3·3H2O2 (s) ΔH < 0
副反应:2H2O2 = 2H2O + O2↑
50℃时2Na2CO3·3H2O2 (s) 开始分解
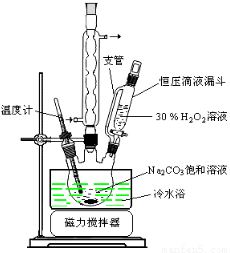
请回答下列问题:
(1)步骤①的关键是控制温度,原因是 , 其措施有_______、_________和_________。
(2)在滤液X中加入适量NaCl固体可析出过碳酸钠,原因是_________________。
(3)步骤③中选用无水乙醇洗涤产品的目的是 。
(4)下列物质中,会引起过碳酸钠失效的有 。
A.NaHCO3 B.MnO2 C.Na2SiO3 D.Na2SO3
(5)过碳酸钠产品中往往含有少量碳酸钠,可用重量法测定过碳酸钠的质量分数;其操作步骤:取样品溶解→加入BaCl2溶液→过滤→洗涤→干燥→称量。需要直接测定的物理量有: 样品的质量m1g、沉淀的质量m2g(用字母表示并注明其含义)。产品中过碳酸钠质量分数的表达式为: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省长望浏宁四县高三一模考试化学试卷(解析版) 题型:选择题
下图为雾霾的主要成分示意图。下列说法不正确的是

A.重金属离子可导致蛋白质变性
B.苯是最简单的芳香烃
C.SO2和NxOy都属于酸性氧化物
D.汽车尾气的大量排放是造成雾霾天气的人为因素之一
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省绥化市高三下学期开学联考化学试卷(解析版) 题型:填空题
(8分)实验室中需要220mL0.5mol/L H2SO4,现用98%浓硫酸(密度为1.84g/cm3)稀释配制。
(1)本实验室中需要的仪器是 。
(2)要将浓硫酸在 中稀释,稀释时的操作方法是 。
(3)必须将稀释后的硫酸 后再移液,原因是 ,否则,所配制的稀硫酸浓度会 (偏高、偏低、无影响)。
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高一上学期学期期末化学试卷(解析版) 题型:实验题
(6分)某待测液中可能含有Ba2+、Fe3+、K+、Fe2+、CO32-、Cl-等离子,进行如下实验:
①取适量待测液于试管中,加入稀H2SO4,有白色沉淀生成;
②过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现;
③在步骤②中的溶液中,继续滴加氯水,溶液立即变红。
根据实验现象回答:
(1)待测液中一定含有的离子是 ,一定不含有的离子是 ;
(2)还有一种离子不能确定是否存在,要确认这种离子的实验方法和现象是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com