
【题目】将NH4HCO3在试管中加热,使放出的气体依次通过盛有足量过氧化钠的干燥管、足量浓硫酸的洗气瓶,最后得到的气体是( )
A.NH3B.O2C.H2OD.CO2
科目:高中化学 来源: 题型:
【题目】在一定容积的密闭容器中进行反应;N2(g)+3H2(g)![]() 2NH3(g)。己知反应过程中某一时刻N2、H2、NH3的浓度分别为0.1mol/L、0.3mol/L、0.2mol/L。当反应达到平衡时,可能存在的数据是
2NH3(g)。己知反应过程中某一时刻N2、H2、NH3的浓度分别为0.1mol/L、0.3mol/L、0.2mol/L。当反应达到平衡时,可能存在的数据是
A. N2为0.2mol/L;H2为0.6mol/L B. N2为0.15mol/L
C. N2、H2均为0.18 mol/L D. NH3为0.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学工业中Mn可用作氧化剂、助燃剂、活性电极材料、催化剂、油漆和油墨的干燥剂等,碳酸锰矿可作为制备MnO2原料
(1)已知25℃,101kPa时有如下的三个热化学方程式
①MnCO3(s) ![]() MnO(s)+CO2(g) △H1=+116 6kJ/mol
MnO(s)+CO2(g) △H1=+116 6kJ/mol
②2MnO(s)+O2(g) ![]() 2MnO2(s) △H2=-272.0kJ/mol
2MnO2(s) △H2=-272.0kJ/mol
③2MnCO3(s)+O2(g) ![]() 2Mn2(s)+2CO2(g) △H3
2Mn2(s)+2CO2(g) △H3
则△H3=_________;反应②在________条件下(填“高温”、“低温”或“任何温度”)能自发进行。
(2)在密闭容器中投入足量的 MnCO3,在一定条件下发生反应:MnCO3(s) ![]() Mno(s)+CO2(g) △H1=+116.6kJ/mol。一定温度下,达到平衡状态时p(CO2)=bMPa
Mno(s)+CO2(g) △H1=+116.6kJ/mol。一定温度下,达到平衡状态时p(CO2)=bMPa
①温度、压强对碳酸锰平衡分解率的影响如图所示。图中Y1____Y2(填“>”、“<”或“=”)。
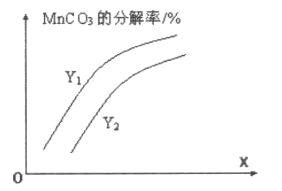
②保持温度不变,将体积扩大至原来的3倍,则容器内压强p(CO2)的变化范围为_______。
③若温度不变,将容器体积压缩至原来的一半,达到新平衡时,与原平衡状态相比,下列物理量一定不变的是________ (填字母)
A.CO2的质量 B. MnCO3的质量 C.MnCO3的分解率
D.化学平平衡常数 E.CO2的物质的量浓度
(3)在4L恒容密闭容器中,充入足量量的MnCO3(s)和a molO2(g),在一定温度下发生反应:MnCO3(s)+O2(g) ![]() 2MnO2(s)+2CO2(g),经过5min该反应刚好达到平衡状态,且该段时间内CO2的化学反应速率为0.2molL-1·min-1若该条件该反应的化学平衡常数K=0.5,则a=____。
2MnO2(s)+2CO2(g),经过5min该反应刚好达到平衡状态,且该段时间内CO2的化学反应速率为0.2molL-1·min-1若该条件该反应的化学平衡常数K=0.5,则a=____。
(4)现以铅蓄电池为电源,用石墨为电极,电解MnSO4和H2SO4混合液来制备MnO2,装置如图所示,阳极的电极反应式为___________,当蓄电池中有2mol H+被消耗时,则理理论上能生成MnO2________g
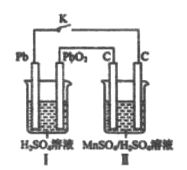
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学一一选修修5:有机化学基础】光刻胶是一种应用广泛的光敏材料,它的一种合成路线如下(部分试剂和产物略去):
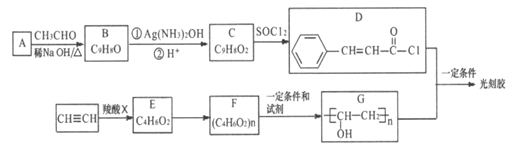
已知:
I.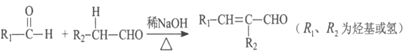
II.![]()
回答下列问题
(1)C中所含官能团的名称是________,G的化学名称为_______________。
(2)乙快和羧酸X加成生成E,E的核磁共振氢谱为三组峰,且峰面积比为3:2:1,E能发生水解反应,则E的结构简式为_________,E→F的反应类型是___________。
(3)B与Ag(NH3)2OH反应的化学方程式为_________________。
(4)D+G→光刻胶的化学方程式_________________________________。
(5)某芳香族有机物H是C的同系物,相对分子质量比C大14,则该有机物H的苯环上只含有两条侧链的同分异构体有______________种。(不考虑立体异构)
(6)根据已有知识并结合相关信息,写出以CH2CH2OH为原料制备CH2CH2CH2COOH的合成路线流程图(无机试剂任用) ______________________。合成路线流程图示例如下:

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是资源的宝库。占地球上储量99%的溴分步在海洋中,我国目前是从食盐化工的尾料中提取溴,反应原理是:Cl2+2Br-→2Cl-+Br2。
(1)氯原子最外层电子轨道表示式是______________,氯气属于________分子(填写“极性”或“非极性”)。
(2)已知溴水中存在如下化学平衡:Br2+H2O![]() H++Br-+HBrO。取少量溴水于一支试管中,向试管中滴加氢氧化钠溶液,溶液颜色变浅。请用平衡移动的观点解释颜色变浅的原因_____________。
H++Br-+HBrO。取少量溴水于一支试管中,向试管中滴加氢氧化钠溶液,溶液颜色变浅。请用平衡移动的观点解释颜色变浅的原因_____________。
(3)氟和溴都属于卤族元素,HF和地壳内SiO2存在以下平衡:4HF(g)+ SiO2(s) ![]() SiF4(g)+2H2O(g)+148.9kJ。该反应的平衡常数表达式K=_________________。如果上述反应达到平衡后,降低温度,该反应会_____________(填写“向正反应方向移动”或“向逆反应方向移动”),在平衡移动时逆反应速率先_______后_______(填写“增大”或“减小”)。
SiF4(g)+2H2O(g)+148.9kJ。该反应的平衡常数表达式K=_________________。如果上述反应达到平衡后,降低温度,该反应会_____________(填写“向正反应方向移动”或“向逆反应方向移动”),在平衡移动时逆反应速率先_______后_______(填写“增大”或“减小”)。
(4)若反应的容器容积为2.0 L,反应时间8.0min,容器内气体的质量增加了0.24g,在这段时间内HF的平均反应速率为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯、玉米淀粉等发酵制得。A的钙盐是人们喜爱的补钙剂之一。A在某种催化剂的存在下被氧化,其产物不能发生银镜反应。在浓硫酸存在下, A可发生如下所示的反应。

(1)A含有的官能团名称为_____________________,A→F的反应类型为 __________。
(2)写出一种和B具有相同官能团的同分异构体的结构简式___________________________。
(3)写出A→D的化学方程式_______________________________________________________。
(4)有机物C3H6O含有醛基,一定条件下和H2反应生成CH3CH2CH2OH。检验该有机物是否完全转化的操作是_______________________________________________________________。
(5)有机物E可以由CH2=CHCH2OH得到,改变条件它也可以制得其他产物。设计一条由CH2=CHCH2OH合成CH3CH2COOH的路线_____________。
合成路线流程图示例如下:CH3CH2OH![]() CH2=CH2
CH2=CH2![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【题目】生产上用过量烧碱溶液处理某矿物(含Al2O3、MgO),过滤后得到滤液用NaHCO3溶液处理,测得溶液pH和Al(OH)3生成的量随加入NaHCO3溶液体积变化的曲线如下:

下列有关说法不正确的是
A. 原NaHCO3溶液中c(H2CO3)+c(HCO3-)+c(CO32-)=0.8moL/L
B. a点水的电离程度小于c点水的电离程度
C. a点溶液中存在:c(Na+)+c(H+)=c(AlO2-)+(OH-)
D. 生成沉淀的离子方程式为:HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境污染已成为人类面临的重大威胁,下列对应关系不正确的是( )
环境问题 | 造成环境问题的主要物质 | |
A | 酸雨 | 二氧化硫 |
B | 温室效应 | 二氧化碳 |
C | 白色污染 | 二氧化硅 |
D | 光化学烟雾 | 二氧化氮 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com