
【题目】海洋是资源的宝库。占地球上储量99%的溴分步在海洋中,我国目前是从食盐化工的尾料中提取溴,反应原理是:Cl2+2Br-→2Cl-+Br2。
(1)氯原子最外层电子轨道表示式是______________,氯气属于________分子(填写“极性”或“非极性”)。
(2)已知溴水中存在如下化学平衡:Br2+H2O![]() H++Br-+HBrO。取少量溴水于一支试管中,向试管中滴加氢氧化钠溶液,溶液颜色变浅。请用平衡移动的观点解释颜色变浅的原因_____________。
H++Br-+HBrO。取少量溴水于一支试管中,向试管中滴加氢氧化钠溶液,溶液颜色变浅。请用平衡移动的观点解释颜色变浅的原因_____________。
(3)氟和溴都属于卤族元素,HF和地壳内SiO2存在以下平衡:4HF(g)+ SiO2(s) ![]() SiF4(g)+2H2O(g)+148.9kJ。该反应的平衡常数表达式K=_________________。如果上述反应达到平衡后,降低温度,该反应会_____________(填写“向正反应方向移动”或“向逆反应方向移动”),在平衡移动时逆反应速率先_______后_______(填写“增大”或“减小”)。
SiF4(g)+2H2O(g)+148.9kJ。该反应的平衡常数表达式K=_________________。如果上述反应达到平衡后,降低温度,该反应会_____________(填写“向正反应方向移动”或“向逆反应方向移动”),在平衡移动时逆反应速率先_______后_______(填写“增大”或“减小”)。
(4)若反应的容器容积为2.0 L,反应时间8.0min,容器内气体的质量增加了0.24g,在这段时间内HF的平均反应速率为_____________________。
【答案】 ![]() 非极性 滴加氢氧化钠溶液,OH-和H+结合,导致H+浓度降低,平衡向右移动,溶液颜色变浅 [SiF4][H2O]2/[HF]4 向正反应方向移动 减小 增大 0.0010mol/(L·min)
非极性 滴加氢氧化钠溶液,OH-和H+结合,导致H+浓度降低,平衡向右移动,溶液颜色变浅 [SiF4][H2O]2/[HF]4 向正反应方向移动 减小 增大 0.0010mol/(L·min)
【解析】(1)Cl原子最外层有7个电子,最外层电子排布式为3s23p5;最外层电子轨道表示式是![]() ;氯气属于非极性分子;(2)已知溴水中存在如下化学平衡:Br2+H2O
;氯气属于非极性分子;(2)已知溴水中存在如下化学平衡:Br2+H2O![]() H++Br-+HBrO。取少量溴水于一支试管中,向试管中滴加氢氧化钠溶液,OH-和H+结合,导致H+浓度降低,平衡向右移动,溶液颜色变浅;(3)反应4HF(g)+ SiO2(s)
H++Br-+HBrO。取少量溴水于一支试管中,向试管中滴加氢氧化钠溶液,OH-和H+结合,导致H+浓度降低,平衡向右移动,溶液颜色变浅;(3)反应4HF(g)+ SiO2(s) ![]() SiF4(g)+2H2O(g)的平衡常数表达式K=[SiF4][H2O]2/[HF]4;反应4HF(g)+ SiO2(s)
SiF4(g)+2H2O(g)的平衡常数表达式K=[SiF4][H2O]2/[HF]4;反应4HF(g)+ SiO2(s) ![]() SiF4(g)+2H2O(g)+148.9kJ为放热反应,达到平衡后,降低温度,平衡向正反应方向移动;在平衡移动时逆反应速率先减小后由于体系温度升高反应速率增大;(4)若反应的容器容积为2.0 L,反应时间8.0min,容器内气体的质量增加了0.24g,则二氧化硅减少了0.24g,在这段时间内HF消耗了
SiF4(g)+2H2O(g)+148.9kJ为放热反应,达到平衡后,降低温度,平衡向正反应方向移动;在平衡移动时逆反应速率先减小后由于体系温度升高反应速率增大;(4)若反应的容器容积为2.0 L,反应时间8.0min,容器内气体的质量增加了0.24g,则二氧化硅减少了0.24g,在这段时间内HF消耗了![]() ,HF的平均反应速率为
,HF的平均反应速率为 =0.0010 mol/(L·min)。
=0.0010 mol/(L·min)。


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
【题目】1,2二溴乙烷的制备原理是:CH3CH2OH![]() CH2=CH2+H2O CH2=CH2+Br2→ Br2CH2一CH2Br
CH2=CH2+H2O CH2=CH2+Br2→ Br2CH2一CH2Br
某课题小组用下图所示的装置制备1,2-二溴乙烷。

回答下列问题
(1)组装仪器后进行该实验前必须进行的操作是_________。
(2)装置B的作用是_______。
(3)三颈烧瓶内加入一定量的乙醇一浓硫酸混合液和少量粗砂,其加入粗砂目的是_______,仪器E的名称是_________________。
(4)装置C内发生的主要反应的离子方程式为__________________________。
(5)加热三颈烧瓶前,先将C与D连接处断开,再将三颈烧瓶在石棉网上加热,待温度升到约120℃时,连接C与D,并迅速将A内反应温度升温至160-180℃,从滴液漏斗中慢慢滴加乙醇一浓硫酸混合液,保持乙烯气体均匀地通入装有3.20ml液溴(![]() 3g/cm3)和3ml水的D中试管,直至反应结束。
3g/cm3)和3ml水的D中试管,直至反应结束。
①将C与D连接处断开的原因是_____________________,
②判断反应结束的现象是______________________________。
(6)将粗品移入分液漏斗,分别用水、氢氧化钠溶液、水洗涤,产品用无水氯化钙干燥,过滤后蒸馏收集129-133℃馏分,得到7.896g1,2-二溴乙烷。1,2-二溴乙烷的产率为___________。
(7)下列操作中,不会导致产物产率降低的是________ (填正确答案的标号)
a.乙烯通入溴水时速率太快 b.装置E中的NaOH溶液用水代替.
c.去掉装置D烧杯中的水 d.实验时没有C装置 e. D中的试管里不加水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是100mg CaC2O4H2O受热分解时,所得固体产物的质量随温度变化的曲线.试利用图中信息结合所学的知识,回答下列各问题: 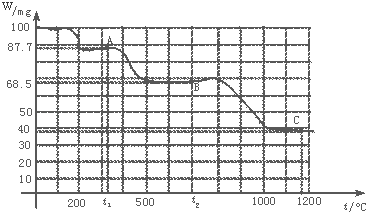
(1)温度分别为t1和t2时,固体产物的化学式A是 , B是 .
(2)由CaC2O4H2O得到A的化学方程式为 .
(3)由A得到B的化学方程式为 .
(4)由图计算产物C的相对分子质量,并推断C的合理的化学式.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将NH4HCO3在试管中加热,使放出的气体依次通过盛有足量过氧化钠的干燥管、足量浓硫酸的洗气瓶,最后得到的气体是( )
A.NH3B.O2C.H2OD.CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨电极电解CuSO4和KNO3的混合溶液500mL,经一段时间电解后,两极都得到11.2L气体(标准状况),此混合液中Cu2+的物质的量浓度为( )
A.0.5mol/L
B.0.8mol/L
C.1mol/L
D.1.5mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】井水冒泡、有异味和变浑浊是地震的常见征兆,其中可能涉及地下硫铁矿(FeS2)发 生的反应:FeS2+H2O=Q+S+H2S↑ (已配平),则物质Q是
A. Fe2O3 B. FeO C. Fe(OH)2 D. Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关常温下pH均为3的醋酸溶液和盐酸的说法正确的是( )
A.两种溶液中,由水电离出的氢离子浓度均为l×10﹣11 molL﹣1
B.分别加水稀释100倍后,两种溶液的pH仍相等
C.中和同体积的这两种酸溶液所需要NaOH物质的量也相等
D.分别加入足量锌片,两种溶液生成H2的体积相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com