
【题目】下列生产、生活中的事例不属于氧化还原反应的是( )
A. 钢铁的腐蚀
B. 大理石雕像被酸雨腐蚀毁坏
C. 食物腐败
D. 燃放烟花
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.s区、d区、ds区都是金属元素
B.p区都是主族元素
C.所有族中IIIB中元素种类最多
D.最外层电子数为2的元素都分布在s区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在固定体积的密闭容器中发生下列反应:2HI(g)H2(g)+I2(g).若c(HI)由0.1mol/L 降到0.07mol/L时,需要15s,那么c(HI)由0.07mol/L 降到0.05mol/L时,所需反应的时间为( )
A.等于5 s
B.等于10 s
C.大于10 s
D.小于10 s
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸钾和亚硫酸氢钾能发生氧化还原反应:ClO3﹣+3HSO3﹣=3SO42﹣+Cl﹣+3H+ , 已知该反应的速率随溶液酸性的增强而加快.如图为用ClO3﹣在单位时间内的物质的量浓度的变化来表示该反应速率的速率﹣时间图象.下列说法不正确的是( ) 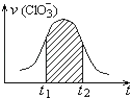
A.反应开始时速率增大可能是c(H+)增大引起的
B.纵坐标为v(H+)的速率﹣时间曲线与图中曲线不能完全重合
C.后期反应速率下降的主要原因是反应物浓度减小
D.图中阴影部分“面积”为t1至t2时间内的ClO3﹣的物质的量的减小值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当浓度恒定时,A、B两种物质在不同温度下进行反应:A+3B3C.10℃时,反应率v(B)=0.3mol/(Ls);50℃时,反应速率v(A)=25.6mol/(Ls).若该反应温度升高10℃反应速率增至原来的n倍,则n值为( )
A.4
B.3
C.3.5
D.2.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能达到实验目的的是( )

A. 用图1装置将硫酸铜溶液直接蒸干得到胆矾 B. 图2装置可用于收集氨气并进行尾气吸收
C. 用图3装置电解精炼铝 D. 图4装置可以用于实验室制备Fe(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是一种重要的化工产品,是氮肥工业、有机合成工业以及制造硝酸、铵盐和纯碱等的原料.
(1)以氨为燃料,氧气为氧化剂可以设计制造氨燃料电池,因产物无污染,在很多领域得到广泛应用.若电极材料均为惰性电极,KOH溶液作电解质溶液,则该电池负极电极反应式为;正极分压式为 .
(2)下列措施可以加快合成氨反应速率的是 .
A.通过缩小容器的容积增大压强
B.及时将氨液化分离出去
C.适当升温
D.添加合适的催化剂
E.恒温恒容时,再充入一定体积的氮气
(3)某化学研究性学习小组模拟工业合成氨的反应.在容积固定为2L的密闭容器内充入1mol N2和3mol H2 , 加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
则从反应开始到25min时,①以N2表示的平均反应速率为;②H2的平衡转化率为;
(4)以CO2与NH3为原料合成尿素[化学式为CO(NH2)2]的主要反应如下,已知:
①2NH3(g)+CO2(g)═NH2CO2NH4(s);△H=﹣159.47kJmol﹣1
②NH2CO2NH4(s)═CO(NH2)2(s)+H2O(g);△H=+116kJmol﹣1
③H2O(l)═H2O(g);△H=+44kJmol﹣1
写出CO2与NH3合成尿素和液态水的热化学反应方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应N2(g)+3H2(g)2NH3(g),500℃时在容积为10L的密闭容器中进行,开始时加入1mol N2和6mol H2 , 则达到平衡时,NH3的浓度不可能达到( )
A.0.1 molL﹣1
B.0.2 molL﹣1
C.0.05 molL﹣1
D.0.15 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水.当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热.已知:0.4mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256.652kJ的热量.
(1)反应的热化学方程式为;
(2)又已知H2O(l)=H2O(g);△H=+44kJ/mol,则16g液态肼和液态双氧水反应生成液态水时放出的热量是;
(3)此反应用于火箭推进,除释放大量的热和快速产生大量气体外还有一个很大的优点是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com