



科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
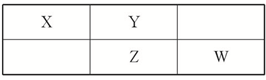 四种短周期元素在周期表中的相对位置如表所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
四种短周期元素在周期表中的相对位置如表所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.查看答案和解析>>
科目:高中化学 来源: 题型:
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期元素R、Q、M、T在元素周期表中的相对位置如下表,已知R原子最外层电子数与次外层电子数之比为2:1.
短周期元素R、Q、M、T在元素周期表中的相对位置如下表,已知R原子最外层电子数与次外层电子数之比为2:1.| R | Q | ||
| M | T |
| +x |
| +x |
| 化合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化钡溶液中滴加少量稀硫酸:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B、次氯酸钙溶液中通入过量二氧化碳:ClO-+H2O+CO2=HCO3-+HClO |
| C、向碳酸氢钠溶液中滴入过量澄清石灰水:Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O |
| D、NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1L水中溶解了58.5g NaCl,该溶液的物质的量浓度为1mol/L |
| B、从1L 2mol/L的H2SO4溶液中取出0.5L,该溶液的浓度为1mol/L |
| C、中和100mL 1mol/L的H2SO4溶液,需NaOH为4g |
| D、配制500mL 0.5mol/L的CuSO4溶液,需62.5g胆矾 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com