
已知短周期元素的离子 aA2+、bB+、cC2-、dD- 都具有相同的电子层结构,则下列叙述正确的是
A.原子半径 A>B>D>C B.原子序数 d>c>b>a
C.离子半径 C2->D->B+>A2+ D.单质的还原性 A>B>D>C
科目:高中化学 来源: 题型:
花青苷是引起花果呈现颜色的一种花色素, 广泛存在于植物中。它的主要结构在不同pH条件下有以下存在形式:


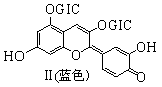 (GIC——葡萄糖基)
(GIC——葡萄糖基)
下列有关花青苷说法不正确的是 :
A.花青苷可作为一种酸碱指示剂 B.I和II中均含有二个苯环
C.I和II中除了葡萄糖基外,所有碳原子可能共平面
D.I和II均能与FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)右图所示的原电池装置中,其负极材料是 ,正极上能够观察到的现象是 ,正极的电极反应式是 。
原电池工作一段时间后,若消耗锌6.5g,则放出气体__________g。
(2)铅蓄电池是常用的化学电源,其电极材料是Pb和PbO2,电解液为稀硫酸。工作时该电池总反应式为PbO2+Pb+2H2SO4===2PbSO4+2H2O,据此判断:铅蓄电池的负极材料是________。工作时,电解质溶液的酸性________(填“增大”、“减小”或“不变”)。工作时,电解质溶液中阴离子移向_______极(填“正”或“负”)。电子流动方向为从_______极流向_______极(填“正”或“负”)。

查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.强电解质溶液的导电能力一定强于弱电解质溶液
B.将氢氧化钠和氨水各稀释一倍,两者的氢氧根浓度均减少到原来的1/2
C.物质的量相同的磷酸钠溶液和磷酸溶液中所含磷酸根物质的量相同
D.溶液中有已电离的离子和未电离的分子能说明该物质是弱电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
学生用铝片分别和稀盐酸、稀硫酸反应发现:铝片与稀盐酸反应现象非常明显,而和稀硫酸几乎不反应。为排除因试剂变质等因素造成的影响,该学生在教师的指导下重新进行下列实验,验证是否存在上述现象。
铝与酸反应的情况。结果如下:
反应进程(分钟) 1 2 5 15 20
3.0mol/L盐酸 少量气泡 较多气泡 大量气泡 反应剧烈 铝片耗尽
1.5mol/L硫酸 均无明显现象(无气泡产生)
3.0mol/L硫酸 均无明显现象(无气泡产生)
通过上述实验可知,无论是用1.5mol/L 硫酸还是3.0mol/L 硫酸,均无明显的现象,而3.0mol/L盐酸与铝片反应的现象却十分明显。
(1)反应1~15min 内,铝与盐酸的反应速率逐渐加快,其主要原因是
__________________________ 。
(2)根据以上探究“铝与稀盐酸和稀硫酸反应差异的原因”,你能对问题原因作出哪些假设或猜想(列出两种即可)?
假设一:_________________________________________________________________
假设二:_________________________________________________________________
(3)通过你的思考,教材中H2O2的分解所用的催化剂(FeCl3和CuSO4)这个实验(关于催化剂对化学反应速率的影响)也需要改进,才具有说服力,应怎样改进
________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列表述正确的是( )。
A.化学方程式为:2M N
N
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com