
【题目】下列说法正确的是
A. ![]() 的名称为3-甲基丁烷
的名称为3-甲基丁烷
B. 淀粉和纤维素的化学式均为(C6H10O5)n,故两者互为同分异构体
C. ![]() 和
和![]() 为同一种物质
为同一种物质
D. HCOOH与OHCCH2OH属于同系物
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,下列不能用勒夏特列原理解释的是( )
A.H2、I2、HI混合气体加压后颜色变深
B.合成氨时将氨液化分离,可提高原料的利用率
C.向氯水中缓慢加入硝酸银固体,氯水颜色变浅
D.使用MnO2作催化剂能加速H2O2的分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,下列说法正确的是( )
A.向氨水中加入氯化铵固体,会使溶液的pH增大
B.常温时,向CaCO3的饱和溶液中加入Na2CO3固体,则CaCO3的溶度积常数增大
C.常温下,浓度均为0.1mol·L-1的①醋酸、②盐酸、③醋酸钠溶液,水的电离程度的顺序为③>①>②
D.NaHCO3饱和水溶液中c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生研究小组欲探究CuSO4溶液与Na2CO3溶液混合产生的蓝绿色沉淀组成,小组进行下列实验探究。
【提出假设】
假设1:沉淀为Cu(OH)2
假设2:沉淀为
假设3:沉淀为碱式碳酸铜[化学式可表示为nCuCO3mCu(OH)2]
【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水)。
【物质成分探究】
步骤1:将所得悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤
步骤2:甲同学取一定量固体,用气密性良好的右图装置(夹持仪器未画出)进行定性实验。

请回答下列问题:
(1)假设2中的沉淀为 。
(2)假设1中沉淀为Cu(OH)2的理论依据是 。
(3)无水乙醇洗涤的目的____ __。
(4)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设______(填写序号)成立。
(5)乙同学认为只要将上图中B装置的试剂改用 试剂后,便可验证上述所有假设。
(6)乙同学更换B试剂后验证假设3成立的实验现象是 。
(7)在假设3成立的前提下,某同学考虑用Ba(OH)2代替Ca(OH)2,测定蓝绿色固体的化学式,若所取蓝绿色固体质量为27.1g,实验结束后装置B的质量增加2.7g,C中的产生沉淀的质量为19.7g。则该蓝绿色固体的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷与氯气发生取代反应的副产品生产盐酸的设想在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,所设计的装置如图所示:
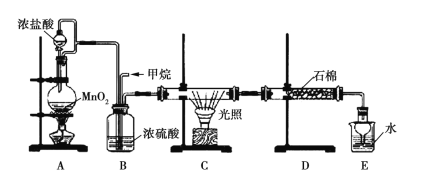
(1)A中制取Cl2的反应的化学方程式是_________________________。
(2)B装置的作用:①______;②______;③______。
(3)D装置中的石棉上吸附着潮湿的KI,其作用是________________。
(4)E装置的作用是_____(填序号)。
A.收集气体 B.吸收氯气 C.吸收氯化氢
(5)E装置中除了有盐酸生成外,还含有有机物,从E中分离出盐酸的最佳方法是______________。
(6)将1 mol CH4与Cl2发生取代反应,测得4种有机取代产物的物质的量相等,则消耗的氯气的物质的量是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是廉价的碳资源,其综合利用具有重要意义。
(1)CO2与CH4经催化重整反应CH4(g)+CO2(g)2CO(g)+2H2(g)△H=+120kJ·mol-1可以制得合成气。
已知上述反应中相关物质所含化学键键能数据如下:
化学键 | C-H | C=O | H-H | C≡O(CO) |
键能/kJ·mol-1 | a | b | c | x |
①x=___。
②分别在恒温密闭容器A(恒容)、B(恒压,体积可变)中,加入CH4和CO2各1mol的混合气体,起始体积均为VL。相同温度下两容器中反应达平衡后吸收热量较多的是___ (填“A”或“B”)。保持A容器的体积和B容器压强不变,写出一种能使A、B两容器中各物质的体积分数相同的方法:___。
③某温度下,在体积为2L的恒容密闭容器中加入2molCH4、1molCO2以及催化剂进行反应,达到平衡时CO2的体积分数为![]() ,该温度下反应的平衡常数为___。
,该温度下反应的平衡常数为___。
(2)CO2可以被NaOH捕获。所得溶液中含碳微粒的分布百分数随pH的变化如图所示。H2CO3的二级电离平衡常数Ka2=___。pH=5.4时,φ(A):φ(B)=___。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)物质的量浓度相同的下列物质的溶液①NH4Cl ②NH4HSO4③CH3COONH4,c(NH4+)由小到大的顺序是_______________(填序号)。
(2)同浓度的下列溶液:①CH3COONH4②NH4Cl ③Na2CO3④NaHCO3,其中pH由大到小的顺序 是_________________。
(3)物质的量浓度相同的 ①盐酸、②硫酸溶液、 ③醋酸(CH3COOH)溶液各100 mL分别与足量的Zn反应,在相同的条件下,产生H2的体积分别为V1、V2、V3,它们由大到小的顺序是____________。
(4)CH3COONa溶液呈_____性(填“酸”、“碱”或“中”),其原因是______(用离子方程式表示)。
(5)常温时,若10体积pH1=a的盐酸溶液与1体积pH2=b的氢氧化钠溶液混合后溶液呈中性,则混合前该强酸的pH1与强碱的pH2之间应满足的关系是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器中,起始投入4molN2和6molH2在一定条件下生成NH3,平衡时仅改变温度测得的数据如表所示(已知:T1<T2)
温度/K | 平衡时NH3的物质的量/mol |
T1 | 3.6 |
T2 | 2 |
(1)则K1__K2,(填“>”、“<”或“=”)原因:___。
(2)在T2下,经过10s达到化学平衡状态,则平衡时H2的转化率为__。若再同时增加各物质的量为1 mol,该反应的平衡v正__v逆,(>或=或<)平衡常数将___(填“增大”、“减小”或“不变”)
(3)下列能说明该反应已达到平衡状态的是__。
A.3v正(H2)=2v逆(NH3) B.容器内气体压强不变
C.混合气体的平均相对分子质量不再改变的状态 D.c(H2)=c(NH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用![]() 表示阿伏加德罗常数的值.下列叙述正确的是
表示阿伏加德罗常数的值.下列叙述正确的是
A.![]() 与足量
与足量![]() 反应,共生成
反应,共生成![]() ,转移电子的数目为
,转移电子的数目为![]()
B.室温下,![]() 的
的![]() 溶液中,由水电离的
溶液中,由水电离的![]() 离子数目为
离子数目为![]()
C.![]() 聚丙烯中含有双键的数目为
聚丙烯中含有双键的数目为![]()
D.含![]() 的饱和溶液最多可形成胶体粒子数为
的饱和溶液最多可形成胶体粒子数为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com