
����Ŀ���״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ����
��CH3OH(g)+H2O(g)=CO2(g)+3H2(g)�� ��H= + 49.0 kJ��mol-1
��CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g)�� �� H=��192.9 kJ��mol-1
����˵����ȷ����
A. CH3OH ����ֵΪ192.9/32 (kJ��g-1)
B. ��Ӧ���е������仯��ͼ��ʾ

C. CH3OHת���H2�Ĺ���һ��Ҫ��������
D. ��������֪��Ӧ��CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g) ����H>��192.9kJ��mol��1
���𰸡�D
��������A�����ݷ�Ӧ��CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g)�� �� H=��192.9 kJ��mol-1�������ܹ�����ȼ�շų����������CH3OH ����ֵ����192.9/32 (kJ��g-1)����A����B����Ӧ�ٵ���H��0����ͼʾ����H=������������-��Ӧ����������0����B����C������֪��֪����Ӧ��Ϊ���ȷ�Ӧ������Ӧ��Ϊ���ȷ�Ӧ����C����D��ͬ���ʵ�����ͬ�����ʣ���̬������ߣ����Һ̬��������̬������ͣ��ɢ���֪��Ӧ��CH3OH(l)+ ![]() O2(g)=CO2(g)+2H2(g)����H��-192.9kJmol-1����D��ȷ����ѡD��
O2(g)=CO2(g)+2H2(g)����H��-192.9kJmol-1����D��ȷ����ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������ֻ��A��B��C���ֵ��ʣ�A����ɫ��ӦΪ��ɫ����Ҫ��G��ʽ�����ں�ˮ�У�F��һ�ֵ���ɫ�Ĺ��壬H��һ�ֳ�������ɫҺ�壬I���������ЧӦ�ġ�Ԫ�ס��������ʼ��ת����ϵͼ���£�
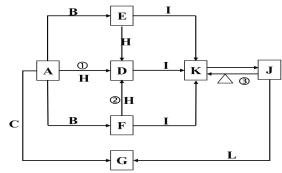
�ش��������⣺
��1��A�ǣ�_____��C�ǣ�_____��L�ǣ�______��I�ǣ�____���ѧʽ����
��2��д����Ӧ�٢ڢ۵Ļ�ѧ��Ӧ����ʽ��
�٣�____________________________________��
�ڣ�____________________________________��
�ۣ�____________________________________��
��3��F����Ϊ����ɴ��еĹ�����ʹ�ã���Ҫ�Ƶ���������Ϊ25%�Ŀ���89.6 L�������������ҪF������Ϊ_____g����Ӧ��ת�Ƶ��ӵĸ���Ϊ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ������֪���ʵ���Ũ�ȵ��������ⶨδ֪���ʵ���Ũ�ȵ�NaOH��Һʱ��ѡ�������ָʾ��������д���пհף�
��1����ͼ��______������A������B�����Ǽ�ʽ�ζ��������и�ʵ��ĵ�һ��������____________________��
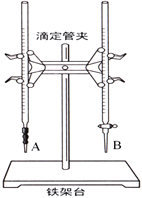
��2���ñ�������ζ������NaOH��Һʱ����������ʽ�ζ��ܵĻ���������ҡ����ƿ���۾�ע����ƿ����Һ��ɫ�仯��ֱ�������һ���������_____________________________��������������˵���ﵽ�ζ��յ㡣
��3�����в����п���ʹ����NaOH��Һ��Ũ����ֵƫ�͵�����____��
A����ʽ�ζ���δ�ñ�������ϴ��ֱ��ע�������
B���ζ�ǰʢ��NaOH��Һ����ƿ������ˮϴ����û�и���
C����ʽ�ζ����ڵζ�ǰ�����ݣ��ζ���������ʧ
D����ȡ�������ʱ����ʼ���Ӷ������ζ�����ʱ���Ӷ���
��4�����ζ���ʼ�ͽ���ʱ����ʽ�ζ����е�Һ����ͼ��ʾ��������������Һ�����Ϊ________mL��
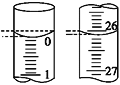
��5��ijѧ������3��ʵ��ֱ��¼�й��������±���
�ζ����� ����NaOH��Һ�����/mL | 0.100 0 mol��L��1��������/mL | ||
�ζ�ǰ�̶� | �ζ���̶� | ||
��һ�� | 25.00 | 0.00 | 26.11 |
�ڶ��� | 25.00 | 1.56 | 30.30 |
������ | 25.00 | 0.22 | 26.31 |
�����ϱ�������ʽ������NaOH��Һ�����ʵ���Ũ�ȣ�д����Ҫ���̣���______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������̪��һ�����Ƽ�����ȱѪ��ҩ�������ֺϳ��������¡�����˵����ȷ����(����)

A. ������X��Y�Ͷ���̪���ַ����и�����1������̼ԭ��
B. ������Y���Է���ȡ�����ӳɺͼӾ۷�Ӧ
C. ����Na2CO3��Һ������X�ͻ�����Y
D. ������X��Y�Ͷ���̪��1 mol�������NaOH������Ϊ1 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ִ���ᣬ����Խ��Խ��ע��ʳ�е�Ӫ���ɷ֡�ϺƤ�������Ͷ�����ʳ�ﺬ�зḻ�ĸƣ�����ĸ�Ӧ����Ϊ�� ��
A.����B.����C.Ԫ��D.ͬλ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����ѧ��ѧ�г����ڻ����ķ�����ᴿ��װ�ã������װ�ûش����⣺
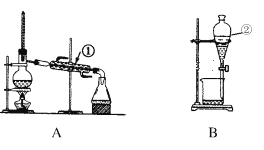

��1�����Ȼ�����Һ�еõ��Ȼ��ع��壬ѡ��װ��________ (�����װ��ͼ����ĸ����ͬ)����ȥ����ˮ�е�Cl�������ʣ�ѡ��װ��________��
��2����������Ȼ�̼��Һ��ˮ���뿪ѡ���װ����___________�������ǽ��иò����IJ��裬��ȷ��˳����____________��
�ٽ�����ﵹ���Һ©���У�����������̨����Ȧ�Ͼ��ã��ֲ㣻
�ڴӷ�Һ©���Ͽڵ����ϲ���Һ
�۽���Һ©���IJ�������ʹ�������ϵİ��۶�©��������С��
�ܷ�Һ©�����浼�ܽ����ձ��ڱڣ��������������ձ�������Һ
�ݼ���Һ©�������;����IJ������Ƿ�©ˮ
��3��װ��A�Тٵ�������______________����ˮ�ķ����Ǵ�________�ڽ�ˮ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬ��ͬѹ��,�������� SO2����� SO3������Ƚ�,��ȷ��˵����
A. �ܶȱ�Ϊ 4:5 B. ���ʵ���֮��Ϊ 4:5
C. �����Ϊ 1:1 D. ԭ����֮��Ϊ 3:4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʾһ��ԭ���ڵ������Ӳ�����10�����ӿ���д�� �� ��
A. 310 B. 3d10 C. 3s23p64s2 D. 3s23p63d2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com