
【题目】X、Y、Z三种主族元素的单质在常温下都是常见的无色气体,在适当条件下,三者之间可以两两发生反应生成分别是双核、三核和四核的甲、乙、丙三种分子,且乙、丙分子中含有X元素的原子个数比为2∶3。请回答下列问题:
(1)元素X的名称是________,丙分子的电子式为________。
(2)若甲与Y单质在常温下混合就有明显现象,则甲的化学式为________。丙在一定条件下转化为甲和乙的反应方程式为___________________________。
(3)化合物丁含X、Y、Z三种元素,丁是一种常见的强酸,将丁与丙按物质的量之比1∶1混合后所得物质戊的晶体结构中含有的化学键为________(选填序号)。
a.只含共价键 b.只含离子键 c.既含离子键,又含共价键
 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源: 题型:
【题目】在容积为2升的密闭容器中,有反应mA(g)+nB(g)![]() pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为A减少了a mol·L-1,B的平均反应速度VB=a/15mol·L-1·min-1,C增加了2a/3 mol·L-1,这时若增加系统压强,发现A与C的百分含量不变,则m︰n︰p︰q为( )
pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为A减少了a mol·L-1,B的平均反应速度VB=a/15mol·L-1·min-1,C增加了2a/3 mol·L-1,这时若增加系统压强,发现A与C的百分含量不变,则m︰n︰p︰q为( )
A.3︰1︰2︰2 B.1︰3︰2︰2
C.1︰3︰2︰1 D.1︰1︰1︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的短周期主族元素,其原子半径与最外层电子数的关系如下图1。E原子最外层上的电子数是D原子最外层电子数的4倍,D离子核外电子排布与C2-相同。

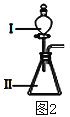
试回答:
(1)元素E在元素周期表中的位置是___________________。
(2)与元素D离子所含电子数和质子数均相同的微粒是________________。(用化学式作答,下同)
(3)B和E最高价氧化物对应的水化物,酸性较弱的_________________。若用上图2中装置验证这两种酸的酸性强弱,则在装置中加入的试剂分别为:Ⅰ___________,Ⅱ__________,观察到的实验现象是________________________。
(4)由以上五种元素组成的物质,其组成和结构信息如下表:
物质 | 组成和结构信息 |
a | 含有A、C、D的盐 |
b | C、D组成的化合物,且原子数之比为1∶1 |
c | 化学组成为AC2 |
①a含有的化学键有___________________________________;
②b与c反应的化学方程式为_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用氯气消毒的自来水配制下列溶液时,会使配得的溶液变质的是( )
①NaOH ②AgNO3 ③Na2CO3 ④NaBr ⑤FeCl2
A.只有②④ B.只有④⑤
C.只有②④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去粗盐中的Ca2+、Mg2+、SO42﹣及泥沙,可将粗盐溶于水,然后进行下列五项操作.其中正确的是①过滤 ②加过量的NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过BaCl2溶液( )
A.①④②⑤③
B.④①②⑤③
C.②⑤④①③
D.②④①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式正确的是
A.甲烷的标准燃烧热为890.3 kJ·mol1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)![]() CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol1
CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol1
B.500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g) 2NH3(g)ΔH=-38.6 kJ·mol1
2NH3(g)ΔH=-38.6 kJ·mol1
C.S(s)+O2(g)=SO2(g) ΔH=-269.8 kJ·mol1
D.2NO2=O2+2NO ΔH=+116.2 kJ·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定的温度下,向一个容积为2 L的恒容密闭容器中(事先装入催化剂),充入2molN2和3molH2, 3min后测得密闭容器内的压强是起始时的0.9倍。在这段时间内,用H2表示该反应的平均反应速率是
A. 0.125mol·L-1·min-1 B. 0.100 mol·L-1·s-1
C. 0.200 mol·L-1·min-1 D. 0.375 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为短周期元素,A和B是同周期相邻的两种元素,A和C是同主族相邻的两种元素,A、B、C三种元素的原子序数之和为31,D元素与A、B、C三种元素既不同周期,也不同主族,请回答:
(1)C元素在元素周期表中的位置是_____________________________;
(2)A、B、D可组成一种离子化合物,是常见的化肥,其化学式为_________________;
(3)A2和D2两种物质可以构成一种新型的原电池,若原电池中电解质溶液为KOH溶液,则正极的电极反应式为_____________________________;
(4)若将一充满20 mlBA2和A2混合气体的大试管倒立于D2A中,充分反应后,在相同条件下,测得试管中余下5mL无色气体,则原混合气体中BA2和A2物质的量之比为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com