
| T/K | T1 | T2 | T3 |
| K | 1.00��107 | 2.45��105 | 1.88��103 |
| a |
| 2 |
| 2-n |
| 2 |
| a |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����еĸ��ֽⷴӦ���Ƿ�������ԭ��Ӧ |
| B�������ᷴӦ�������һ���Ǽ��������� |
| C��ͬһԪ�ز����ܼȱ��ֽ����ԣ��ֱ��ַǽ����� |
| D���Թ��ۼ��γɵĵ�����ֻ���ڷǼ��Լ����Թ��ۼ��γɵĻ�������ֻ���ڼ��Լ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ca2+��K+��CO32-��Cl- |
| B��K+��NH4+��HCO3-��OH- |
| C��H+��Fe2+��ClO-��SO42- |
| D��Na+��Ba2+��OH-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��PM2.5����ֱ��Լ��ԭ��ֱ����2.5�� |
| B�����ۡ����ǡ���������һ���������ܷ���ˮ�ⷴӦ |
| C��ֲ����ͨ���ܺ�����������Һ������Ӧ |
| D��Ӧ�ó����ֹ����ɫʳƷ�������κλ�ѧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
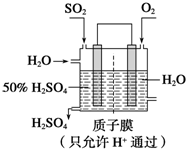
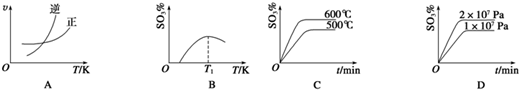
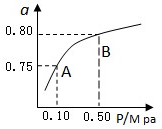
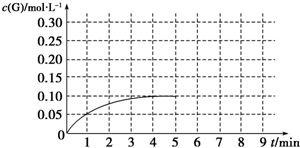
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
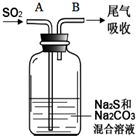 ���ȼ��仯�����й㷺����;��
���ȼ��仯�����й㷺����;��| ���ϣ�25��ʱ | |
| H2CO3 | Ki1=4.4��10-7 |
| H2S | Ki1=1.3��10-7 |
| H2SO3 | Ki1=1.54��10-2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
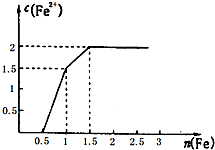 ͨ����ģ�͡�ͼ�Ρ�ͼ���Ĺ۲죬�ܻ�ȡ�й���Ϣ�ǻ�ѧѧϰ��һ����Ҫ��������Ҫ��ش��������⣮
ͨ����ģ�͡�ͼ�Ρ�ͼ���Ĺ۲죬�ܻ�ȡ�й���Ϣ�ǻ�ѧѧϰ��һ����Ҫ��������Ҫ��ش��������⣮| Ԫ�ر��/Ԫ������ | �� | �� | �� | �� | �� | �� | �� | �� | �� | |
| X | 3.44 | 2.55 | 0.98 | 2.04 | 2.19 | 3.16 | 0.93 | 3.04 | 1.61 | |
| �������ϼ� | ��� | +4 | +1 | +3 | +1 | +3 | ||||
| ��ͼ� | -2 | -4 | -3 | -1 | -3 | |||||
| ����/20��ʱ�ܽ�ȣ�g/100g�ܼ��� | AgNO3 | Ba��NO3��2 | AgCl | BaCl2 |
| ˮ�� | 216 | 9.02 | 1.9��10-14 | 35.8 |
| Һ�� | 86 | 97.2 | 0.8 | 0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com