
| A、PM2.5颗粒直径约是原子直径的2.5倍 |
| B、淀粉、蔗糖、氨基酸在一定条件都能发生水解反应 |
| C、植物油通常能和氢氧化钠溶液发生反应 |
| D、应该倡议禁止向绿色食品中添加任何化学物质 |


 每课必练系列答案
每课必练系列答案科目:高中化学 来源: 题型:
| A、反应后溶液中ClO-的个数为0.1NA |
| B、原NaOH浓度为1mol/L |
| C、参加反应的氯气分子为0.1NA |
| D、转移电子为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4种 | B、6种 |
| C、10种 | D、12种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
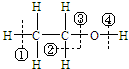 在化学反应中断键位置说法错误的是( )
在化学反应中断键位置说法错误的是( )| A、乙醇在铜催化下与氧气反应,在②④位置断裂,所以只有与羟基直接相连的碳原子上有氢原子才能发生催化氧化 |
| B、乙醇与钠反应,在④位置断裂 |
| C、乙醇与浓硫酸在140℃时,在③或④位置断裂,该反应属于取代反应 |
| D、乙醇与浓硫酸在170℃时,在②③位置断裂,以水分子的形式消去,属于消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,pH=7的任何溶液中含有OH-数目均为10-7NA |
| B、23g乙醇中含有C-H键的数目为3NA |
| C、4.8g O2和O3以任何比例组成的混合气体中含有的氧原子数目均为0.3NA |
| D、常温常压下,2.24L Cl2与足量铁粉充分反应,转移的电子数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
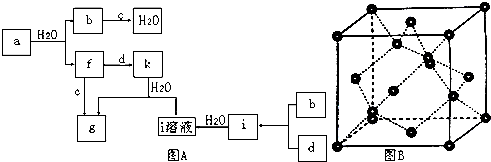
查看答案和解析>>
科目:高中化学 来源: 题型:
| T/K | T1 | T2 | T3 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com