
【题目】磷及其化合物在生产、生活中有重要的用途。回答下列问题:
(1)直链聚磷酸是由n个磷酸分子通过分子间脱水形成的,常用于制取阻燃剂聚磷酸铵。
①写出磷酸主要的电离方程式 。
②直链低聚磷酸铵的化学式可表示为(NH4)(n+2)PnOx,x= (用n表示)。
(2)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式。
□H2PO2-+□Ag+ + □ = □PO43-+ □Ag +□
(3)由工业白磷(含少量砷、铁、镁等)制备高纯白磷(熔点44℃,沸点280℃),主要生产流程如下
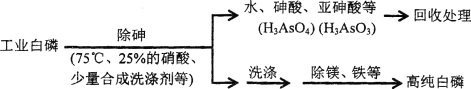
①除砷过程在75℃下进行,其合理的原因是_______(填字母)。
a.温度不宜过高,防止硝酸分解 b.适当提高温度,加快化学反应速率
c.使白磷熔化,并溶于水 d.降低白磷的毒性
②硝酸氧化除砷时被还原为NO,若氧化产物为等物质的量的亚砷酸与砷酸,则化学反应方程式为_______________
【答案】(10分)(1)①H3PO4![]() H++H2PO4-(2分)②3n+1(2分)
H++H2PO4-(2分)②3n+1(2分)
(2)H2PO2-+4Ag++6OH-=PO43-+4Ag+4H2O(2分)
(3)①cd(2分)②8HNO3+6As+5H2O=3H3AsO4+3H3AsO3+8NO↑(2分)
【解析】
试题解析: (1)①H3PO4是三元弱酸,其电离是逐步进行的,主要是第一步电离,磷酸主要的电离方程式是H3PO4![]() H++H2PO4-;②在磷酸通过分子间脱水形成直链聚磷酸中,n越大,分子中含有的羟基就越少,得到的直链聚磷酸铵的水溶性越小;(2)该反应是氧化还原反应,同时也是离子反应,根据电子守恒、电荷守恒及原子守恒,可得反应的方程式是:H2PO2-+4Ag++6OH-=PO43-+4Ag+4H2O。(3) ①除砷过程在75 ℃下进行,其合理的原因是使白磷熔化,提高反应活性;适当提高温度,增大反应速率;温度不宜过高,防止硝酸分解,所以选项是acd。②生产过程在高纯氮气保护下进行,原因是白磷非常活泼,容易与空气中的氧气发生反应;在氮气的环境中,其目的是防止白磷被空气中氧气氧化;③除砷过程中,合成洗涤剂起到乳化作用。④硝酸氧化除砷时被还原为NO,砷被氧化为砷酸,根据电子守恒、原子守恒,可得砷转化为砷酸的化学方程式:3As+5HNO3+2H2O=3H3AsO4+5NO↑;氧化相同质量的砷,当转化为亚砷酸的量越多,得到的电子就越少,则反应消耗硝酸的量越少;⑤根据图示可知,砷的脱除率从a点到b点降低,原因是硝酸浓度变大,氧化性增强,有较多的硝酸用于氧化白磷,脱砷率降低。
H++H2PO4-;②在磷酸通过分子间脱水形成直链聚磷酸中,n越大,分子中含有的羟基就越少,得到的直链聚磷酸铵的水溶性越小;(2)该反应是氧化还原反应,同时也是离子反应,根据电子守恒、电荷守恒及原子守恒,可得反应的方程式是:H2PO2-+4Ag++6OH-=PO43-+4Ag+4H2O。(3) ①除砷过程在75 ℃下进行,其合理的原因是使白磷熔化,提高反应活性;适当提高温度,增大反应速率;温度不宜过高,防止硝酸分解,所以选项是acd。②生产过程在高纯氮气保护下进行,原因是白磷非常活泼,容易与空气中的氧气发生反应;在氮气的环境中,其目的是防止白磷被空气中氧气氧化;③除砷过程中,合成洗涤剂起到乳化作用。④硝酸氧化除砷时被还原为NO,砷被氧化为砷酸,根据电子守恒、原子守恒,可得砷转化为砷酸的化学方程式:3As+5HNO3+2H2O=3H3AsO4+5NO↑;氧化相同质量的砷,当转化为亚砷酸的量越多,得到的电子就越少,则反应消耗硝酸的量越少;⑤根据图示可知,砷的脱除率从a点到b点降低,原因是硝酸浓度变大,氧化性增强,有较多的硝酸用于氧化白磷,脱砷率降低。


科目:高中化学 来源: 题型:
【题目】下列物质:① 干燥的氯气 ② 过氧化钠粉末 ③ 漂白粉 ④ 活性炭,其中能使红墨水褪色的是 ( )
A. ①④ B. ②③④ C. ①②③ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组将下图所示装置按一定顺序连接,在实验室里制取一定量的FeCl3(所通气体过量并充分反应)。请回答下列问题:
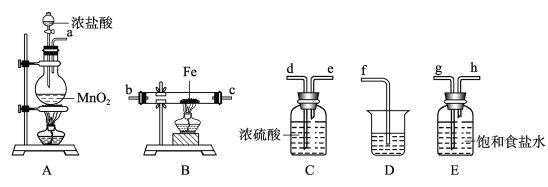
(1)A中发生反应的化学方程式为____________________________。
(2)各装置的正确连接顺序为(填写装置代号)A→_______→_______→_______→D。
(3)装置E的作用是___________________。写出装置D(D中所盛溶液为KOH)中反应的化学方程式___________________
(4)工业上生产氯气的方程式为________________________。
(5)随着反应的进行,发现分液漏斗中的浓盐酸逐渐滴不下去,其原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是 ( )
① 钠、氢气都能在氯气中燃烧生成白色烟雾
② 铜丝在氯气中燃烧,生成蓝绿色的氯化铜
③ 液氯就是氯气的水溶液,它能使干燥的有色布条退色
④ 久置的氯水,因氯气几乎完全挥发掉,剩下的只有水
A. ① B. ①② C. ①④ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既是氧化还原反应,又是吸热反应的是
A.灼热的炭与CO2反应 B.铝片与稀H2SO4反应
C.Ba(OH)2·8H2O与NH4Cl的反应 D.甲烷在O2中的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应:Fe(s) + CO2(g)![]() FeO(s) + CO(g) ΔH>0。反应过程中CO2气体和CO气体的浓度与时间的关系如下图所示:
FeO(s) + CO(g) ΔH>0。反应过程中CO2气体和CO气体的浓度与时间的关系如下图所示:

下列说法不正确的是
A.该反应的平衡常数表达式为![]()
B.升高温度后达新平衡时,![]() 增大
增大
C.3分钟时,CO和CO2的浓度相等,反应达到平衡状态
D.8分钟内CO的平均反应速率v(CO)= 0.0625 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g) ΔH=Q kJ/mol(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是
Si(s)+4HCl(g) ΔH=Q kJ/mol(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol, 则达平衡时,吸收热量为Q kJ
C.反应至4 min时,若HCl浓度为0. 12 mol/L,则H2的反应速率为0.03 mol/(L·min)
D.当反应吸收热量0.025Q kJ时,生成的HCl通入含0. 1 mol NaOH的溶液恰好反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含 SO32-、Fe2+、Br-、I-各 0.1 mol 的溶液中通入标准状况下的 Cl2,通入 Cl2的体积和溶液中相关离子的物质的量的关系图正确的是
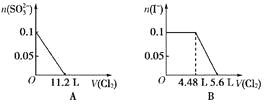
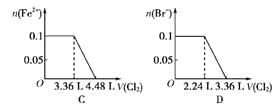
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com