
| A、乙烯的结构简式CH2CH2 |
B、基态氧原子L层电子排布图: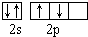 |
C、甲基的电子式 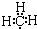 |
| D、HClO的结构式:H-Cl-O |
 故B错误;
故B错误;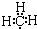 ,故C正确;
,故C正确;

科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用氨水清洗试管内壁附着的银镜 |
| B、将NH4Cl溶液蒸干制备NH4Cl固体 |
| C、制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 |
| D、可用K3[Fe(CN)6]溶液鉴定FeCl3溶液中是否存在Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②④⑤⑥ | B、①② |
| C、②③⑤ | D、②⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:

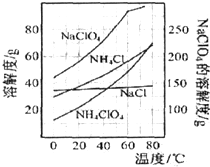
| A、制得粗产品的反应原理为:NH4Cl+NaClO4=NaCl+NH4ClO4↓ |
| B、上述流程中操作Ⅰ为冷却结晶,操作Ⅱ为重结晶 |
| C、洗涤粗产品时,宜用冷水洗涤 |
| D、上述流程中蒸发浓缩时,蒸发至剩余少量溶液时,应停止加热,利用余热将其蒸干,防止晶体飞溅 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 混合物 | 化学方程式 |
| (1) | Na2CO3固体(NaHCO3) | |
| (2) | Fe2O3固体(Al2O3) | |
| (3) | NaHCO3溶液(Na2CO3) | |
| (4) | FeCl2溶液(FeCl3) | |
| (5) | CO2(HCl) |
查看答案和解析>>
科目:高中化学 来源: 题型:
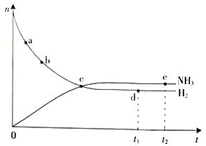 合成氨工业对国民经济和社会发展具有重要的意义.根据已学知识回答下列问题:
合成氨工业对国民经济和社会发展具有重要的意义.根据已学知识回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
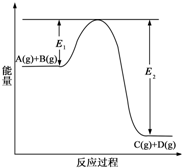 (1)反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列问题.
(1)反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生铁中含有碳,抗腐蚀能力比纯铁强 |
| B、铁与盐溶液所发生的反应都是置换反应 |
| C、铁与稀硫酸反应,铁与浓硫酸不能反应 |
| D、工业上可以用铝热反应的方法制取少量的铁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com