
【题目】固体聚合硫酸铁(SPFS)是一种重要的无机高分子絮凝剂,极易溶于水,其化学组成可表示为Fex(OH)y(SO4)znH2O。
Ⅰ.SPFS的工业制备:
用绿矾(FeSO4·7H2O)与NaClO3溶液在酸性介质中充分反应,经水解、聚合、减压蒸发可得到聚合硫酸铁
Ⅱ.SPFS的组成测定:
取8.19g某固体聚合硫酸铁溶解于水,向其中加入过量的BaCl2溶液到沉淀完全,经过滤、洗涤、干燥得到9.32g白色沉淀;向滤液中加入NH3·H2O,调节溶液pH=6,经过滤、洗涤、干燥、灼烧得到4.00 g固体Fe2O3。
(1)从FeSO4溶液中得到绿矾的实验操作为 ___________________________。
(2)Ⅰ中绿矾与NaClO3溶液反应的离子方程式为______________________。
(3)Ⅱ中当溶液pH=6时,c(Fe3+)=_______。(已知:Ksp[Fe (OH) 3]=4.0×10-38)
(4)该SPFS的化学式为______________(写出计算过程)。
【答案】 蒸发浓缩、冷却结晶 6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O 4.0×10-14 molL-1 Fe5(OH)7(SO4)4·2H2O
【解析】本题主要考查关于物质的量的计算。
(1)从FeSO4溶液中得到绿矾的实验操作为蒸发浓缩、冷却结晶。
(2)Ⅰ中绿矾与NaClO3溶液反应中Fe2+被ClO3-氧化为6Fe3+,同时得到还原产物Cl-,反应的离子方程式为6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O。
(3)Ⅱ中当溶液pH=6时,c(OH-)=1×10-8mol/L,c3(OH-)c(Fe3+)=Ksp[Fe (OH) 3]=4.0×10-38,得到c(Fe3+)=4.0×10-14 molL-1。
(4)9.32g白色沉淀是硫酸钡,其物质的量为0.04mol,其中![]() 的质量为3.84g;4.00 g固体Fe2O3的物质的量为0.025mol,其中含Fe3+0.05mol即2.8g;根据电荷守恒可得n(OH-)=0.15mol-0.08mol=0.07mol即1.19g;m(H2O)=(8.19-3.84-2.8-1.19)g=0.36g,n(H2O)=0.02mol。因此,该SPFS的化学式为Fe5(OH)7(SO4)4·2H2O。
的质量为3.84g;4.00 g固体Fe2O3的物质的量为0.025mol,其中含Fe3+0.05mol即2.8g;根据电荷守恒可得n(OH-)=0.15mol-0.08mol=0.07mol即1.19g;m(H2O)=(8.19-3.84-2.8-1.19)g=0.36g,n(H2O)=0.02mol。因此,该SPFS的化学式为Fe5(OH)7(SO4)4·2H2O。


科目:高中化学 来源: 题型:
【题目】下列电子排布式或轨道表示式正确的是
A. C原子的轨道表示式:![]()
B. Ca原子的电子排布式:1s22s22p63s23p63d2
C. N原子的轨道表示式:![]()
D. Br-的电子排布式[Ar] 3d104s24p6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C为短周期元素,在周期表中所处的位置如表所示.
A | C | |
B |
A、C两元素的原子核外电子数之和等于B原子的质子数.
(1)写出B,C元素的名称、 .
(2)B位于元素周期表中第周期第族.
(3)用石墨为电极,电解B元素的最高价氧化物的水化物的水溶液,当电路中转移0.4mol电子时,在阴极收集到的产物是 , 质量为g,电解的总反应方程式为;
(4)写出A的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
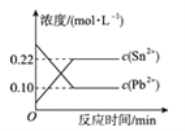
【题目】25 ℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq) ![]() Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )
A. 往平衡体系中加入金属铅后,c(Pb2+)增大
B. 升高温度,平衡体系中c(Pb2+)增大,说明该反应ΔH>0
C. 25 ℃时,该反应的平衡常数K=2.2
D. 往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在指定溶液中一定能大量共存的是( )
A. 纯碱溶液中:Al3+、Ba2+、Cl-、NO3-
B. 室温下,pH=1的溶液中:K+、Fe2+、MnO4-、I-
C. 能使甲基橙变为黄色的溶液中:Na+、Al3+、Cl-
D. 室温下,![]() =1×10-12的溶液中:K+、Na+、CO32-、NO3-
=1×10-12的溶液中:K+、Na+、CO32-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列所述有关离子浓度之间的关系错误的是
A. 将0.2mol/L NaHCO3溶液与0.1mol/L KOH溶液等体积混合:3c(K+) +c(H+)=c(OH-) +c(HCO3-) +2c(CO32-)
B. 浓度均为0.1mol/L 的CH3COOH 与CH3COONa溶液等体积混合后,pH=5,则混合溶液中:c(CH3COO-)-c(CH3COOH)=2×(10-5-10-9) mol/L
C. 将CO2通入0.1mol/L Na2CO3溶液至中性,溶液中2c (CO32-) + c (HCO3-)=0.1mol/L
D. Ka(CH3COOH)=Kb(NH3·H2O) =1.8×10-5,则常温下0.1mol/L CH3COONH4中c(CH3COO-):c(NH3·H2O)=180
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com