
【题目】下列物质中属于纯净物的是( )
A.Na2CO3·10H2O
B.水泥
C.纯净的盐酸
D.普通玻璃
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】丙烯和乙烯都是石油化工最重要的基础原料,可用于生产多种重要的有机化工产品。主要的工业生产途径如下:
途径I:CH3CH2CH3(g) ![]() CH2=CHCH3(g)+H2(g) △H1
CH2=CHCH3(g)+H2(g) △H1
途径II :nCH3OH(g) ![]() CnH2n(g)+nH2O(g)(n为2或3) △H2<0
CnH2n(g)+nH2O(g)(n为2或3) △H2<0
回答下列问题:
(1)已知:丙烷、丙烯、氢气的燃烧热分别为2219.9 kJ·mol-1 、2056.5 kJ·mol-1 和285.8 kJ·mol-1 ,则△H1=________ kJ·mol-1 。
(2)途径I制备丙烯,要提高丙烯的产率最好采用____________条件。(填“高压”或“低压”)
(3)途径II控制适当的条件(温度、压强、催化剂等)可以调节N(N=n(乙烯)/n(丙烯))在0~1.5之向变化,回答下列问题:
①要大幅度提高丙烯在最终产物中的比率,需要控制的适当条件是______________________。
②在体积为1m3的反应器中投入0.64t甲醇,1h 后,反应器中的压强增加了30%,则甲醇的转化率为______(用N=1进行计算)。
(4)以丙烷为燃料制作新型燃料电池,电池的正极通入O2 和CO2,负极通入丙烷,电解质是熔融碳酸盐。
①写出该电池负极的电极反应式:_____________,CO32-移向电池的___极 (填“正”或“负”)。
②当电池消耗0.005mol C3H8时,正极消耗气体的总体积为_____L (标准状况下)。
③用该电池电解1000mL1mol/L的AgNO3溶液、此电解池的总反应方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组的同学用图所示的实验装置进行电解反应,电解槽内装有KI﹣淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.
已知:3I2+6OH﹣═IO3﹣+5I﹣+3H2O
回答下列问题:
(1)左侧为电源极.(填“正”或“负”)
(2)请用方程式及必要的文字解释左侧溶液变蓝色的原因? .
(3)写出右侧发生的有关电极反应的反应式: .
(4)电解反应结束时,左侧溶液中还I﹣ . (填“有”或“没有”)
(5)写出电解槽内发生反应的总化学方程式: .
(6)如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学反应 . (填“变”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次氯酸钠稳定性远髙于次氯酸钠,也可用于杀菌消毒。制备次氯酸钠方法较多,常用的一种合成路线如下:

已知:1.次氯酸叔丁酯((CH3)3COCl),相对分子质量为108.5,是具有挥发性的黄色油状液体,密度为0.802g/mL,且有强烈刺激性臭味;2.(CH3)3COCl+LiOH=LiClO+(CH3)3COH
请回答:
(1)实验第一步的反应装置如图所示(夹持装置省略),B装置中支管的作用是___________;浓盐酸逐滴滴加而不是一次性加入的原因是_______________。

(2)请写出在装置A中发生反应的化学方程式___________________。
(3)对于操作1,下列说法不正确的是__________。
A.可以选用250mL规格的分液漏斗
B.操作1须在通风橱内进行
C.进行分液时,可提早关闭旋塞,以防止次氯酸叔丁酯从下口流出
D.装置B不合适进行操作1
(4)进行操作3时,并不是直接加热蒸发溶液,而是选择在40°C下缓慢蒸发溶液,试解释其原因 __________。
(5)该实验中次氯酸锂的产率为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成.某校课外兴趣小组以两条途径分别对X进行如下实验探究: 途径a: 
途径b: 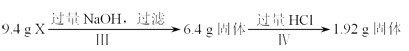
下列有关说法不正确的是( )
A.1.92g固体只含Cu
B.由Ⅰ可知X中一定存在Fe2O3和Cu
C.原混合物中m(Fe2O3):m(Cu)=1:1
D.原混合物X至少含Al2O3和SiO2中的一种,但不能进一步确认二者的存在与否
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、X均为短周期元素形成的无机物,存在下图所示转化关系(部分生成物和反应条件略去);已知A由短周期非金属元素组成,B具有漂白性且光照易分解。请回答以下问题:

(1)若A为单质,且C为一元强酸。
①组成单质A的元素在元素周期表中的位置为__________。
②写出一种工业制备单质A方法的离子方程式: __________。
③X可能为________(填字母代号)。
a.NaOH b. AlCl3 c.Na2CO3 d.NaAlO2
(2)若A为两种元素形成的化合物,且E与水反应生成的G的浓溶液遇C有白烟产生。
①A的电子式为__________。
②A与H2O反应的化学方程式为__________。
③G的浓溶液遇C产生白烟的化学方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10﹣5molL﹣1 | K1=4.4×10﹣7molL﹣1 K2=5.6×10﹣11molL﹣1 | 3.0×10﹣8 molL﹣1 |
请回答下列问题:
(1)同浓度的CH3COO﹣、HCO3﹣、CO32﹣、ClO﹣结合H+的能力由强到弱的顺序为_____。
(2)常温下0.1molL﹣1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是_______(填字母序号,下同).
A.c(H+) B.![]() C.c(H+)c(OH﹣)
C.c(H+)c(OH﹣)
D.![]() E.
E. 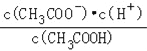
若升高该溶液温度(不考虑醋酸挥发),上述5种表达式的数据增大的是_____.
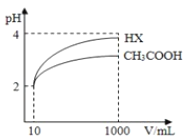
(3)体积为10mL pH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH变化如图:则HX的电离平衡常数_____(填“大于”、“等于”或“小于”)醋酸的平衡常数.稀释后,HX溶液中水电离出来的c(H+)_____(填“大于”、“等于”或“小于”)醋酸的溶液中水电离出来的c(H+),理由是_____.
(4)已知100℃时,水的离子积为1×10﹣12,该温度下测得某溶液PH=7,该溶液显_____(填“酸”、“碱”或“中”)性.将此温度下PH=1的H2SO4溶液aL与PH=11的NaOH溶液bL混合,若所得混合液PH=2,则a:b=_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图1为甲烷和O2构成的燃料电池示意图,电解质溶液为KOH溶液;图2为电解AlCl3溶液的装置,电极材料均为石墨。用该装置进行实验,反应开始后观察到x电极附近出现白色沉淀。下列说法正确的是

A. b电极为负极
B. 图1中电解质溶液的pH增大
C. a电极反应式为CH4-8e-+8OH-=CO2+6H2O
D. 图2中电解AlCl3溶液的总反应式为: 2AlCl3+6H2O ![]() 2Al(OH)3↓+3Cl2↑+3H2↑
2Al(OH)3↓+3Cl2↑+3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体聚合硫酸铁(SPFS)是一种重要的无机高分子絮凝剂,极易溶于水,其化学组成可表示为Fex(OH)y(SO4)znH2O。
Ⅰ.SPFS的工业制备:
用绿矾(FeSO4·7H2O)与NaClO3溶液在酸性介质中充分反应,经水解、聚合、减压蒸发可得到聚合硫酸铁
Ⅱ.SPFS的组成测定:
取8.19g某固体聚合硫酸铁溶解于水,向其中加入过量的BaCl2溶液到沉淀完全,经过滤、洗涤、干燥得到9.32g白色沉淀;向滤液中加入NH3·H2O,调节溶液pH=6,经过滤、洗涤、干燥、灼烧得到4.00 g固体Fe2O3。
(1)从FeSO4溶液中得到绿矾的实验操作为 ___________________________。
(2)Ⅰ中绿矾与NaClO3溶液反应的离子方程式为______________________。
(3)Ⅱ中当溶液pH=6时,c(Fe3+)=_______。(已知:Ksp[Fe (OH) 3]=4.0×10-38)
(4)该SPFS的化学式为______________(写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com