
【题目】A,B,C为短周期元素,在周期表中所处的位置如表所示.
A | C | |
B |
A、C两元素的原子核外电子数之和等于B原子的质子数.
(1)写出B,C元素的名称、 .
(2)B位于元素周期表中第周期第族.
(3)用石墨为电极,电解B元素的最高价氧化物的水化物的水溶液,当电路中转移0.4mol电子时,在阴极收集到的产物是 , 质量为g,电解的总反应方程式为;
(4)写出A的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式 .
【答案】
(1)硫;氟
(2)3;ⅥA
(3)H2;0.4;2H2O ![]() 2H2↑+O2↑
2H2↑+O2↑
(4)NH3+HNO3═NH4NO3
【解析】解:(1)由以上分析可知B为氧元素,C为氟元素,所以答案是:硫;氟;(2)B为S元素,位于周期表第三周期ⅥA族,所以答案是:3;ⅥA;(3)用石墨为电极,电解硫元素的最高价氧化物的水化物的水溶液,阳极生成氧气,阴极生成氢气,总方程式为2H2O ![]() 2H2↑+O2↑,当电路中转移0.4mol电子时,以及生成0.2mol氢气,质量为0.4g,所以答案是:H2;0.4;2H2O
2H2↑+O2↑,当电路中转移0.4mol电子时,以及生成0.2mol氢气,质量为0.4g,所以答案是:H2;0.4;2H2O ![]() 2H2↑+O2↑;(4)N的气态氢化物为氨气,与其最高价氧化物对应的水化物硝酸反应生成硝酸铵,反应的化学方程式为NH3+HNO3═NH4NO3 , 所以答案是:NH3+HNO3═NH4NO3 .
2H2↑+O2↑;(4)N的气态氢化物为氨气,与其最高价氧化物对应的水化物硝酸反应生成硝酸铵,反应的化学方程式为NH3+HNO3═NH4NO3 , 所以答案是:NH3+HNO3═NH4NO3 .


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成.某校课外兴趣小组以两条途径分别对X进行如下实验探究: 途径a: 
途径b: 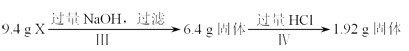
下列有关说法不正确的是( )
A.1.92g固体只含Cu
B.由Ⅰ可知X中一定存在Fe2O3和Cu
C.原混合物中m(Fe2O3):m(Cu)=1:1
D.原混合物X至少含Al2O3和SiO2中的一种,但不能进一步确认二者的存在与否
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有四种不同堆积方式的金属晶体的晶胞如图所示,下列有关说法正确的是( )
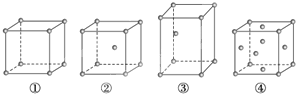
A. ①为简单立方堆积,②为镁型,③为钾型,④为铜型
B. 每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个
C. 晶胞中原子的配位数分别为:①6,②8,③8,④12
D. 空间利用率的大小关系为:①<②<③<④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物用途非常广泛,如二茂铁可用作火箭燃料添加剂,铁酸锶用于直流电机永久陶瓷磁铁。用环戊二烯钠法制备二茂铁(如图)的原理为:C5H6+NaOH→C5H5Na+H2O;2C5H5Na+FeCl2→(C5H5)2Fe+2NaCl。
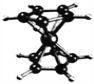
(1)铁元素的基态价电子排布式为________________。
(2)基态Na原子中,核外电子占据的最高能级的符号是________,占据该能层电子的电子云轮廓图形状为________。Na和K属于同一主族,但金属Na的熔点比金属K高,原因是________________________________________。
(3)(C5H5)2Fe中阴离子![]() 中的σ键总数为____个。分子中的大π键可用符号πmn表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π66),则
中的σ键总数为____个。分子中的大π键可用符号πmn表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π66),则![]() 中的大π键应表示为________________。
中的大π键应表示为________________。
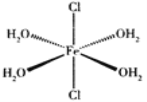
(4)用二乙胺法合成二茂铁的原料有(C2H5)2NH、FeCl2·4H2O及C5H6。FeCl2·4H2O是一种配合物,其结构如图所示,Fe2+与配体之间形成的化学键称为____________。
(5)铁酸锶的晶胞结构如下图所示:
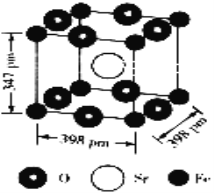
①晶胞中距离最近的两个氧原子的距离为________________cm(列出计算表达式即可)。
②该晶体的密度为_______________________g·cm-3(列出计算表达式即可)。(相对原子质量:Fe:56 Sr:88 O:16)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体聚合硫酸铁(SPFS)是一种重要的无机高分子絮凝剂,极易溶于水,其化学组成可表示为Fex(OH)y(SO4)znH2O。
Ⅰ.SPFS的工业制备:
用绿矾(FeSO4·7H2O)与NaClO3溶液在酸性介质中充分反应,经水解、聚合、减压蒸发可得到聚合硫酸铁
Ⅱ.SPFS的组成测定:
取8.19g某固体聚合硫酸铁溶解于水,向其中加入过量的BaCl2溶液到沉淀完全,经过滤、洗涤、干燥得到9.32g白色沉淀;向滤液中加入NH3·H2O,调节溶液pH=6,经过滤、洗涤、干燥、灼烧得到4.00 g固体Fe2O3。
(1)从FeSO4溶液中得到绿矾的实验操作为 ___________________________。
(2)Ⅰ中绿矾与NaClO3溶液反应的离子方程式为______________________。
(3)Ⅱ中当溶液pH=6时,c(Fe3+)=_______。(已知:Ksp[Fe (OH) 3]=4.0×10-38)
(4)该SPFS的化学式为______________(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L容器中A,B两种物质间的转化反应中,A,B物质的量随时间变化的曲线如图所示,由图中数据分析得: 
(1)该反应的化学方程式为
(2)反应开始至4min时,A的平均反应速率为 .
(3)4min时,反应是否达到平衡状态?(填“是”或“否”), 8min时,v(正)v(逆)(填“>”、“<”或“=”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图甲和图乙表示的是短周期部分或全部元素的某种性质的递变规律,下列说法正确的是( ) 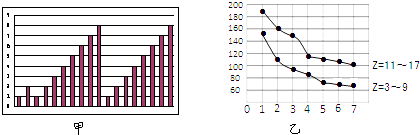
A.图甲横坐标为原子序数,纵坐标表示元素的最高正价
B.图甲横坐标为核电荷数,纵坐标表示元素的原子半径(单位:pm)
C.图乙横坐标为最高正价,纵坐标表示元素的原子半径(单位:pm)
D.图乙横坐标为最外层电子数,纵坐标表示元素的原子半径(单位:pm)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com