
【题目】图甲和图乙表示的是短周期部分或全部元素的某种性质的递变规律,下列说法正确的是( ) 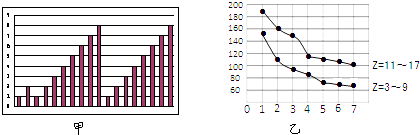
A.图甲横坐标为原子序数,纵坐标表示元素的最高正价
B.图甲横坐标为核电荷数,纵坐标表示元素的原子半径(单位:pm)
C.图乙横坐标为最高正价,纵坐标表示元素的原子半径(单位:pm)
D.图乙横坐标为最外层电子数,纵坐标表示元素的原子半径(单位:pm)
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
(1)将钠、铝、钾各 1mol 分别投入到足量的相同浓度的盐酸中,试预测实验结果:与盐酸 反应最剧烈的单质是 , 与盐酸反应产生的气体最多的是 .
(2)向 Na2S 溶液中通入氯气出现黄色浑浊,可证明 Cl 的非金属性比 S 强,反应离子方程式 为 .
(3)利用如图装置可验证同主族元素非金属性的变化规律:仪器 A 的名称为 , 装置 D 的作用为; 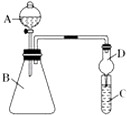
①若要证明非金属性:Cl>I,则 A 中加浓盐酸,B 中加 KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C 中加淀粉碘化钾混合溶液,观察到 C 中溶液的现象,即可证明.从环境保护的观点考虑,此装置缺少尾气处理装置,可用溶液吸收尾气.
②若要证明非金属性:C>Si,则在 A 中加盐酸、B 中加 CaCO3、C 中加 Na2SiO3 溶液,观察到 C 中溶液的现象,即可证明.但有的同学认为盐酸具有挥发性,可进入 C 中干扰实验,应在两装置间添加装有溶液的洗气瓶.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C为短周期元素,在周期表中所处的位置如表所示.
A | C | |
B |
A、C两元素的原子核外电子数之和等于B原子的质子数.
(1)写出B,C元素的名称、 .
(2)B位于元素周期表中第周期第族.
(3)用石墨为电极,电解B元素的最高价氧化物的水化物的水溶液,当电路中转移0.4mol电子时,在阴极收集到的产物是 , 质量为g,电解的总反应方程式为;
(4)写出A的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq) ![]() Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )
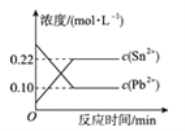
A. 往平衡体系中加入金属铅后,c(Pb2+)增大
B. 升高温度,平衡体系中c(Pb2+)增大,说明该反应ΔH>0
C. 25 ℃时,该反应的平衡常数K=2.2
D. 往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通常用下列方法治理含氮化合物的污染.
(1)用稀土等催化剂能将汽车尾气中的CO、NOx、碳氢化合物转化成无毒物质,从而减少汽车尾气污染.写出NOx与CO催化转化成N2和CO2的化学方程式______.
(2)用NH3还原NOx生成N2和H2O.现有NO、NO2的混合气3L,可用同温同压下3.5L的NH3恰好使其完全转化为N2,则原混合气体中NO和NO2的物质的量之比为______.
(3)电化学降解治理水中硝酸盐污染.在酸性条件下,电化学降解NO的原理如图1,阴极反应式为______.

(4)科研小组研究铁屑对地下水脱氮的反应原理.
①pH=2.5时,用铁粉还原KNO3溶液,相关离子浓度、pH随时间的变化关系如图2(部分副反应产物曲线略去).请根据图中信息写出t1时刻前发生反应的离子方程式______,t1时刻后,反应仍在进行,溶液中NH4+的浓度在增大,Fe2+的浓度却没有增大,可能的原因是______.
②pH=2.5时,将铁屑和活性炭同时加入硝酸钾溶液中,可以加快脱氮速率,其原因是______.通常地下水中含有CO32﹣,会降低脱氮效果,其原因为____________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在指定溶液中一定能大量共存的是( )
A. 纯碱溶液中:Al3+、Ba2+、Cl-、NO3-
B. 室温下,pH=1的溶液中:K+、Fe2+、MnO4-、I-
C. 能使甲基橙变为黄色的溶液中:Na+、Al3+、Cl-
D. 室温下,![]() =1×10-12的溶液中:K+、Na+、CO32-、NO3-
=1×10-12的溶液中:K+、Na+、CO32-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知4NH3(g)+5O2(g)4NO(g)+6H2O(g)△H<0,下列有关叙述正确的( )
A.上述反应的化学反应速率关系:2 v(NH3)=3 v(H2O)
B.若在2L的密闭容器中反应,经过3min后NH3的物质的量由10mol变为7mol 则v (NH3)=0.5molL﹣1s﹣1
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.若降低温度,反应速率将会减小且平衡将被破坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A. 0.1mol/L氨水中,c(OH-)=c(NH4+)
B. 在常温下,10mL 0.02mol/L HCl溶液与10mL 0.02mol.LBa(OH)2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=12
C. 新制氯水中c(Cl-)=c(ClO-)+c(HClO)
D. 0.1mol/L KHC2O4溶液显酸性,溶液中c(K+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(H2C2O4)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com