
【题目】用一种阴、阳离子双隔膜三室电解槽处理废水中的![]() ,模拟装置如图所示。下列说法正确的是
,模拟装置如图所示。下列说法正确的是

A.阳极室溶液由无色变成棕黄色
B.阴极的电极反应式为4OH4e![]() 2H2O+O2↑
2H2O+O2↑
C.电解一段时间后,阴极室溶液中的pH升高
D.电解一段时间后,阴极室溶液中的溶质一定是(NH4)3PO4
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】25℃,向40 mL 0.05 mol/L的FeCl3溶液中加入10 mL 0.15 mol/L的KSCN溶液,发生反应,混合溶液中c(Fe3+)与反应时间(t)的变化如图所示。

(1)该反应的离子方程式为:_________________;
(2)E点对应的坐标为(0,____),t1~t2段v(SCN-)=______mol/(L.min)(用相应字母表示);
(3)关于A、B、C、D四点,下列说法正确的是____________(填序号)
①A点处Fe3+的消耗速率小于B点处Fe(SCN)3的消耗速率
②平均反应速率最小的时间段是t2~t3段
③D点处c(Fe3+)/c[Fe(SCN)3]比值不变
④t4时向溶液中加入50 mL 0.1 mol/L KCl溶液,平衡逆向移动
(4)该反应的平衡常数K值=___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,将O2与NO按3:4的体积比充满一个干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升后,最后烧瓶内溶液的物质的量浓度为( )
A.0.045molL﹣1
B.0.036molL﹣1
C.0.026molL﹣1
D.0.030molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各反应无论反应物的用量多少,只生成一种有机产物的是
A. 甲苯与溴混合后再加入铁粉时发生的反应
B. ![]() 与
与![]() 在四氯化碳溶液里发生加成反应
在四氯化碳溶液里发生加成反应
C. ![]() 与
与![]() 在四氯化碳溶液里发生加成反
在四氯化碳溶液里发生加成反
D. ![]() 与
与![]() 发生加成反应
发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中医书籍《本草衍义》中记载张仲景治伤寒,对茵陈嵩的使用有以下描述: “方用山茵陈、山栀子各三分,秦艽、升麻各四钱,末之。每用三钱,水四合,煎及二合,去滓,食后温服,以知为度。”文中没有涉及到的操作方法是
A.称量B.结晶C.过滤D.蒸发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C,D均为中学化学中常见的单质或化合物,它们之间的关系如图所示(部分产物已略去). 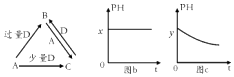
(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为 .
(2)若A为强碱,D为气态氧化物.常温时,将B的水溶液露置于空气中,其pH随时间 t变化可能如上图的图b或图c所示(不考虑D的溶解和水的挥发). ①若图b符合事实,则D的化学式为;
②若图c符合事实,则其pH变化的原因是(用离子方程式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知丙烷的燃烧热△H=-2215KJ·mol-1,若一定量的丙烷完全燃烧后生成1.8g水,则放出的热量约为( )
A. 55 kJ B. 220 kJ C. 550 kJ D. 1108 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由反应物X转化为Y和Z的能量变化如图所示。下列说法错误的是( )
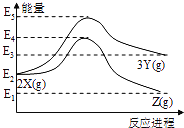
A. 由![]() 反应的ΔH >0
反应的ΔH >0
B. 由![]() 反应的ΔH = (E2-E1) kJ/mol
反应的ΔH = (E2-E1) kJ/mol
C. 降低压强有利于提高Y的产率
D. 降低温度有利于提高Z的产率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com