
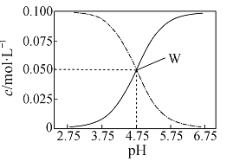
【题目】有c(CH3COOH)+c(CH3COO-)= 0.1 mol·L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH 的关系如图所示。下列有关溶液中离子浓度关系的叙述正确的是( )
A.pH=5. 5 的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
B.W 点所表示的溶液中:c(Na+)+c(H+)= c(CH3COOH)+c(OH-)
C.pH =3.5的溶液中:c(CH3COOH) + c(CH3COO-)= c(Na+)
D.向W点所表示的1.0L溶液中通入0.05molHCl气体(溶液体积变化可忽略):c(H+)=c(CH3COOH)+c(OH-)
【答案】B
【解析】
碱性越强CH3COOH的浓度应越小,CH3COO-的浓度越大,所以图中虚线表示CH3COOH的浓度变化,实线表示CH3COO-的浓度变化。
A.由图可知,pH=4.75时,c(CH3COOH)=c(CH3COO-)=0.05mol/L,pH=5.5时,酸性减弱,结合图象可知,溶液中c(CH3COOH)降低,溶液中c(CH3COO-)增大,则所以c(CH3COO-)>c(CH3COOH),故A错误;
B.由图可知,W点所表示的溶液中c(CH3COOH)=c(CH3COO-)=0.05mol/L,溶液中电荷守恒c(Na+)+c(H+)=c(CH3COO-)+c(OH-),所以c(Na+)+c(H+)=c(CH3COOH)+c(OH-),故B正确;
C.当溶液中的溶质全部为醋酸钠时,有物料守恒c(CH3COOH)+c(CH3COO-)=c(Na+),此时溶液呈碱性,所以pH=3.5时溶液中的溶质为醋酸钠和醋酸,所以c(CH3COOH) + c(CH3COO-)>c(Na+),故C错误;
D.W点原溶液中存在电荷守恒:c(Na+)+c(H+)=c(CH3COO-)+c(OH-),c(CH3COO-)=0.05mol/L,c(H+)=10-4.75mol/L,c(OH-)=10-9.25mol/L,则c(Na+)=0.05mol/L+10-9.25mol/L-10-4.75mol/L,略小于0.05mol/L,也就是此时溶液中溶质醋酸钠的物质的量略小于0.05mol/L,通入0.05molHCl气体后溶液中的溶质为CH3COOH、NaCl以及极少量的HCl,主要以CH3COOH的电离为主,而醋酸是弱电解质,所以c(CH3COOH)>> c(H+),故D错误;
答案选B。


科目:高中化学 来源: 题型:
【题目】工业上处理含苯酚废水的过程如下。回答下列问题:
Ⅰ.测定废水中苯酚的含量。
测定原理:![]() +3Br2→
+3Br2→ ↓+3HBr
↓+3HBr
测定步骤:
步骤1:准确量取![]() 待测废水于
待测废水于![]() 锥形瓶中。
锥形瓶中。
步骤2:将![]()
![]() 浓溴水(量)迅速加入到锥形瓶中,塞紧瓶塞,振荡。
浓溴水(量)迅速加入到锥形瓶中,塞紧瓶塞,振荡。
步骤3:打开瓶塞,向锥形瓶中迅速加入![]()
![]()
![]() 溶液(过量),塞紧瓶塞,振荡。
溶液(过量),塞紧瓶塞,振荡。
步骤4:滴入2~3滴指示剂,再用![]()
![]() 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗![]() 溶液
溶液![]() (反应原理:
(反应原理:![]() )。待测废水换为蒸馏水,重复上述步骤(即进行空白实验),消耗
)。待测废水换为蒸馏水,重复上述步骤(即进行空白实验),消耗![]() 溶液
溶液![]() 。
。
(1)“步骤1”量取待测废水所用仪器是________。
(2)为了防止溴的挥发,上述步骤中采取的措施包括迅速加入试剂和________。
(3)“步骤4”滴定终点的现象为________。
(4)该废水中苯酚的含量为________![]() (用含
(用含![]() 、
、![]() 的代数式表示)。如果空白实验中“步骤2”忘记塞紧瓶塞,则测得的废水中苯酚的含量________(填“偏高”“偏低”或“无影响”,下同);如果空白实验中“步骤4”滴定至终点时俯视读数,则测得的废水中苯酚的含量________。
的代数式表示)。如果空白实验中“步骤2”忘记塞紧瓶塞,则测得的废水中苯酚的含量________(填“偏高”“偏低”或“无影响”,下同);如果空白实验中“步骤4”滴定至终点时俯视读数,则测得的废水中苯酚的含量________。
Ⅱ.处理废水。采用![]() 基
基![]() 为阳极,不锈钢为阴极,含苯酚的废水为电解液,通过电解,阳极上产生羟基(·
为阳极,不锈钢为阴极,含苯酚的废水为电解液,通过电解,阳极上产生羟基(·![]() ),阴极上产生
),阴极上产生![]() 。通过交排列的阴阳两极的协同作用,在各自区域将苯酚深度氧化为
。通过交排列的阴阳两极的协同作用,在各自区域将苯酚深度氧化为![]() 和
和![]() 。
。
(5)写出阳极的电极反应式:________。
(6)写出苯酚在阴极附近被![]() 深度氧化的化学方程式:________。
深度氧化的化学方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于氧化反应的是( )
A.CH2=CH2+H2O![]() CH3CH2OH
CH3CH2OH
B.CH3Cl+Cl2![]() CH2Cl2+HCl
CH2Cl2+HCl
C.2CH3CHO+O2![]() 2CH3COOH
2CH3COOH
D.![]() +Br2
+Br2![]() +HBr
+HBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】给定条件下,下列选项中所示的物质间转化均能一步实现的是( )
A.粗硅![]() SiCl4
SiCl4![]() Si
Si
B.Mg(OH)2![]() MgCl2(aq)
MgCl2(aq)![]() Mg
Mg
C.Fe2O3![]() FeCl3(aq)
FeCl3(aq)![]() 无水FeCl3
无水FeCl3
D.AgNO3(aq)![]() [Ag(NH3)2]OH(aq)
[Ag(NH3)2]OH(aq)![]() Ag
Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种以石墨和过渡金属氧化物做电极材料、以固态有机高聚物做电解质溶剂的锂离子电池,其工作原理如图1所示,图2是合成有机高聚物的单体的结构简式。下列说法中,正确的是

A.放电时,外电路电子由金属氧化物电极流向石墨电极
B.充电时,石墨电极作阳极,过渡金属氧化物作阴极
C.图2所示的两种单体可通过缩聚反应生成有机高聚物溶剂
D.有机高聚物溶剂分子中含醚键和酯基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知短周期元素的离子![]() A2+、
A2+、![]() B+、
B+、![]() C2-、
C2-、![]() D- 都具有相同的电子层结构,则下列叙述中正确的是
D- 都具有相同的电子层结构,则下列叙述中正确的是
A.原子序数d > c > b > aB.离子半径:C2- > D- > B+ > A2+
C.单质的还原性:A > BD.非金属性:D < C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,3-二异丙烯基苯是工业上常用的交联剂,可用于制备高性能超分子聚合物,其结构如图所示。下列有关1,3-二异丙烯基苯的说法错误的是

A.能发生加聚反应
B.与液溴混合后加入铁粉可发生取代反应
C.分子中所有碳原子可能处于同一平面
D.其一氯代物有6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁被称为“第一金属”,铁及其化合物在生产、生活中有广泛用途。
(1)铁原子核外电子发生跃迁时会吸收或释放不同的光,可以用___________摄取铁元素的原子光谱。
(2)FeCl3的熔点为306℃,沸点为315℃。由此可知FeCl3属于______晶体。FeSO4常作净水剂和补铁剂,SO42-的立体构型是____________。
(3) 铁氰化钾K3[Fe(CN)6]是检验Fe2+的重要试剂。
①基态N原子的轨道表示式为___________。
②写出一种与铁氰化钾中配体互为等电子体的极性分子的化学式_______。
③铁氰化钾中,所涉及的元素的第一电离能由大到小的顺序为____________。
④铁氰化钾中,不存在___________(填字母标号)。
A.离子键 B. σ键 C. π键 D.氢键 E.金属键
(4)有机金属配位化合物二茂铁[(C5H5)2Fe]是汽油中的抗震剂。分子中的大 π键可用符号πmn表示,其中m代表参与形成大π键的原子数, n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π66),则![]() 中的大π键应表示为________,其中碳原子的杂化方式为________。
中的大π键应表示为________,其中碳原子的杂化方式为________。
(5)羰基铁[Fe(CO)5]可用作催化剂、汽油抗爆剂等。1mol [Fe(CO)5]分子中含_____molσ键。
(6)某种磁性氮化铁的结构如图所示,N随机排列在Fe构成的正四 面体空隙中。其中铁原子周围最近的铁原子个数为_____;六棱柱底边长为acm,高为c cm,阿伏加德罗常数的值为NA,则该磁性氮化铁的晶体密度为_________g/cm3(列出计算式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含苯酚的工业废水的处理流程如图所示。

(1)①流程图设备Ⅰ中进行的是操作________(填写操作名称)。实验室里这一步操作可以用_______(填仪器名称)进行。
②由设备Ⅱ进入设备Ⅲ的物质A是______________(填化学式,下同)。由设备Ⅲ进入设备Ⅳ的物质B是___________。
③在设备Ⅲ中发生反应的化学方程式为_____________________。
④在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和______。通过 _________________(填操作名称)操作,可以使产物相互分离。
⑤图中,能循环使用的物质是_______、_____________C6H6和CaO。
(2)为了防止水源污染,用简单而又现象明显的方法检验某工厂排放的污水中有无苯酚,此方法是____________。
从废水中回收苯酚的方法是①用有机溶剂萃取废液中的苯酚;②加入某种药品的水溶液使苯酚与有机溶剂脱离;③加入某物质又析出苯酚。试写出②、③两步的反应方程式:_________________________。
(3)为测定废水中苯酚的含量,取此废水100 mL,向其中加入浓溴水至不再产生沉淀为止,得到沉淀0.331 g,求此废水中苯酚的含量____________(mg·L-1)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com