
【题目】NA表示阿佛加德罗常数,下列说法正确的是( )
A.17g NH3含有电子数为10NA
B.标况下,4.48LH2O中所含的分子数是0.2NA
C.0.1mol/L的K2SO4溶液中,K+的数目为0.2NA
D.30 g乙烷(C2H6)所含的原子数目为NA
科目:高中化学 来源: 题型:
【题目】下列关于金属晶体的叙述正确的是
A.用铂金做首饰不能用金属键理论解释
B.固态和熔融时易导电,熔点在1000℃左右的晶体可能是金属晶体
C.Li、Na、K的熔点逐渐升高
D.金属导电和熔融电解质(或电解质溶液)导电的原理一样。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室使用的浓盐酸的溶质质量分数为36.5%,密度为1.19 g·cm-3,则该盐酸的物质的量浓度是( )
A.11.9 B.11.9 mol·L-1 C.0.012 mol·L-1 D.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知ΔH 表示反应热(ΔH>0表示吸热,ΔH<0表示放热),下列描述正确的是( )
A.伴随有能量变化的物质变化都是化学变化。
B.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同。
C.已知相同条件下2SO2(g)+O2(g)![]() 2SO3(g) ΔH1,反应2SO2(s)+O2(g)
2SO3(g) ΔH1,反应2SO2(s)+O2(g)![]() 2SO3(g) ΔH2,则ΔH1>ΔH2。
2SO3(g) ΔH2,则ΔH1>ΔH2。
D.在稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol,若将含0.5 mol H2SO4的浓H2SO4与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图为实验室制取少量乙酸乙酯的装置图。下列关于该实验的叙述中,不正确的是
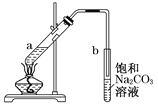
A. 向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸
B. 试管b中导气管下端管口不能浸入液面的目的是防止实验过程中产生倒吸现象
C. 实验时加热试管a的目的之一是及时将乙酸乙酯蒸出,使反应向生成乙酸乙酯的方向移动
D. 试管b中饱和Na2CO3溶液的作用是吸收随乙酸乙酯蒸出的少量乙酸和乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是 ( )
A. 丙烯性质与乙烯相似
B. 饱和一元羧酸的性质与乙酸相似
C. 苯与甲苯都能使酸性高锰酸钾溶液褪色
D. 所有醇都能与羧酸在一定条件下发生酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列空白:
⑴印刷电路板是由高分子材料和铜箔复合而成.刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2.请写出反应的离子方程式 。
⑵请写出在碱性溶液中,ClO![]() 与Fe2+反应的离子方程式为: 。
与Fe2+反应的离子方程式为: 。
⑶NaAlH4是重要的还原剂。请写出NaAlH4与水发生氧化还原反应的化学方程式: 。
⑷+6价铬的化合物毒性较大,常用NaHSO3将酸性废液中的Cr2O72-还原成Cr3+,请写出该反应的离子方程式: 。
⑸亚氯酸钠(NaClO2)溶液可作为烟气的吸收剂,并对烟气进行脱硫、脱硝。在装有亚氯酸钠溶液的鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×103mol·L1。反应一段时间后溶液中离子浓度的分析结果如下表。
离子 | SO | SO | NO | NO | Cl |
c/(mol·L1) | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
写出NaClO2溶液脱硝过程中主要反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应方程式是化学学习的基本工具,本期在化学反应与化学平衡章节学过几个重要的化学方程式,请你按要求写出:
(1)硫代硫酸钠与稀硫酸溶液反应的离子方程式:
(2)碘化钾的稀硫酸溶液与空气中氧气反应的离子方程式:
(3)在重铬酸钾的硫酸溶液中的Cr2O72—与CrO42—之间转化的离子方程式:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com