
【题目】可由N物质通过以下路线合成天然橡胶和香料柑青酸甲酯衍生物F。

已知:

(1)用系统命名法对N命名________.
(2)①试剂a的名称是________。②C→D中反应i的反应类型是________。
(3)E的结构简式是_____________。
(4)关于试剂b的下列说法不正确是________(填字母序号)。
a. 存在顺反异构体 b. 难溶于水c. 能发生取代、加成和氧化反应 d. 不能与NaOH溶液发生反应
(5)写出A生成B的反应方程式_________。
(6)分子中含有![]() 结构的D的所有同分异构共有________种(含顺反异构体),写出其中任意一种含反式结构的结构简式________。
结构的D的所有同分异构共有________种(含顺反异构体),写出其中任意一种含反式结构的结构简式________。
【答案】(1)2—甲基丙烯(或2—甲基—1—丙烯)(2)①甲醛 ②氧化反应
(3)![]() (4)ad
(4)ad
(5)![]()

(6)9  或
或 
【解析】
试题分析:A发生加聚反应合成天然橡胶,所以A为![]() ,对比N CH2=C(CH3)和A的结构,结合信息①可知试剂a为HCHO,A与试剂b发生取代反应生成B,对比B和F的结构可知E为
,对比N CH2=C(CH3)和A的结构,结合信息①可知试剂a为HCHO,A与试剂b发生取代反应生成B,对比B和F的结构可知E为![]() ,D和甲醇发生酯化反应生成E,则D为
,D和甲醇发生酯化反应生成E,则D为![]() ,CH2=C(CH3)氧化得到C,C与银氨溶液反应得到D,则C为
,CH2=C(CH3)氧化得到C,C与银氨溶液反应得到D,则C为![]() .
.
(1)N为CH2=C(CH3),名称为2—甲基丙烯,故答案为:2—甲基丙烯(或2—甲基—1—丙烯)
(2)①(2)由上述分析可知,试剂a的结构简式是HCHO,名称为甲醛,故答案为:甲醛;
②C为![]() ,与银氨溶液的反应为氧化反应,故答案为:氧化反应;
,与银氨溶液的反应为氧化反应,故答案为:氧化反应;
(3)E为![]() ,故答案为:
,故答案为:![]() ;
;
(4)根据b的结构简式可知,a.碳碳双键中其中一个不饱和碳原子连接2个甲基,不存在顺反异构体,故a错误;b.属于卤代烃,难溶于水,故b正确;c.b中有碳碳双键,可以发生加成反应、氧化反应,含有氯原子,能发生取代,故c正确;d.利用氯原子,能与NaOH溶液发生取代反应,故d错误;故答案为:ad;(5)A为![]() ,与试剂b发生取代反应生成B,反应的化学方程式为
,与试剂b发生取代反应生成B,反应的化学方程式为![]()
 ,故答案为:
,故答案为:![]()

(6)D为![]() ,分子中含有
,分子中含有![]() 和
和![]() 结构的D的所有同分异构为CH2=CHCH2COOH、CH3CH=CHCOOH(2种)、CH2=CHCOOCH3、HCOOCH2CH=CH2、HCOOCH=CHCH3(2种)、CH3COOCH=CH2、HCOOC(CH3)=CH2,共有9种,故答案为:9;
结构的D的所有同分异构为CH2=CHCH2COOH、CH3CH=CHCOOH(2种)、CH2=CHCOOCH3、HCOOCH2CH=CH2、HCOOCH=CHCH3(2种)、CH3COOCH=CH2、HCOOC(CH3)=CH2,共有9种,故答案为:9; 或
或  。
。


科目:高中化学 来源: 题型:
【题目】市售一次电池品种很多,碱性锌锰电池在日常生活中用量很大。回收废旧锌锰电池并进行重新处理,可以获得MnO2及其他副产品,其工艺流程如下:

已知:“锰粉”的主要成分有MnO2、Zn(OH)2、MnOOH、碳粉,还含有少量铁盐和亚铁盐。常温下,生成氢氧化物沉淀的pH如下表:
物质 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 | Mn(OH)2 / Mn(OH)3 |
开始沉淀pH | 2.7 | 7.6 | 5.7 | 8.3 |
完全沉淀pH(c≤1.0×10-5mol/L) | 3.7 | 9.6 | 8.0 | 8.8 |
(1)加入NaOH溶液调节pH=8.0,目的是___________________________________;计算常温下Zn(OH)2的溶度积常数Ksp[Zn(OH)2]=____________________。
(2)滤液1中加入H2O2的作用是________________________________________。
(3)写出滤液2中的Mn2+变成MnO2的离子方程式_______________________________。
(4)写出滤渣B与稀硫酸在pH=5时反应的化学方程式_____________________________。
(5)工艺中还可以将滤液4进行_____________、_____________、_____________、洗涤得到含结晶水的硫酸盐晶体。
(6)MnO2常用来制取KMnO4。在一定条件下将MnO2氧化为K2MnO4,然后用铁作阴极、铂作阳极电解K2MnO4溶液得到KMnO4。电解K2MnO4溶液阳极电极反应式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如下图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是

A. 有O2放电的a极为电池的负极
B. O2-移向电池的正极
C. b极对应的电极反应为2H2-4e-+2O2-=2H2O
D. a极对应的电极反应为O2+2H2O+4e-=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2 L的密闭容器中,加入1 mol X(g)和2 mol Y(g)发生反应:X(g)+mY(g)![]() 3Z(g)。平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1 mol Z(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
3Z(g)。平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1 mol Z(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
A.m=2
B.第二次平衡时,Z的浓度为0.4 mol·L-1
C.两次平衡的平衡常数相同
D.X与Y的平衡转化率之比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】著名丹麦物理学家尼·玻尔(N·Bohr)将他钟爱的金制诺贝尔奖章用王水溶解成“金溶液”,化学方程式可简单表示为:Au+HNO3+3HCl===AuCl3+NO↑+2H2O,AuCl3+HCl===HAuCl4(四氯合金酸)。纳粹分子对这种溶液“愚笨”得视而不见、毫无所知。战争结束后,物理学家又根据以下反应,炼出黄金并铸出更加灿烂夺目的奖章:2HAuCl4![]() 2HCl↑+3Cl2↑+2Au。表现出伟大科学家对祖国的无比热爱和非凡智慧。下列叙述中正确的是( )
2HCl↑+3Cl2↑+2Au。表现出伟大科学家对祖国的无比热爱和非凡智慧。下列叙述中正确的是( )
A.王水能溶解黄金,但不能溶解白金
B.HAuCl4具有很强的氧化性
C.盐酸有很强的还原性
D.浓盐酸和浓硝酸按照体积比1:3能配成王水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业上常用下列方法制备H2:
方法①:C(s)+2H2O(g)![]() CO2(g)+2H2(g)
CO2(g)+2H2(g)
方法②:CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
(1)已知①C(石墨)+O2(g)═CO2(g)△H=-394kJmol-1
②2C(石墨)+O2(g)═2CO2(g)△H=-222kJmol-1
③2H2(g)+O2(g)═2H2O(g)△H=-484kJmol-1
试计算25℃时由方法②制备1000gH2所放出的能量为______kJ。
(2)在一定的条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器,发生反应:C(s)+2H2O(g)![]() CO2(g)+2H2(g)其相关数据如下表所示:
CO2(g)+2H2(g)其相关数据如下表所示:

①T1______T2(填“>”、“=”或“<”);T1℃时,该反应的平衡常数K=______。
②乙容器中,当反应进行到1.5min时,H2O(g)的物质的量浓度范围是______。
③在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是______。
A.V逆CO2)=2V正H2)
B.混合气体的密度保持不变
C.c(H2O):c(CO2):c(H2)=2:1:2
D.混合气体的平均摩尔质量保持不变
④某同学为了研究反应条件对化学平衡的影响,测得逆反应速率与时间的关系如图所示:

在t1、t3、t5、t7时反应都达了到平衡状态,如果t2、t4、t6、t8时都只改变了一个反应条件,则t6时刻改变的条件是________________________,从t1到t8哪个时间段H2O(g)的平衡转化率最低______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己二酸 是一种工业上具有重要意义的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用,能够发生成盐反应、酯化反应等,并能与二元醇缩聚成高分子聚合物等,己二酸产量居所有二元羧酸中的第二位.实验室合成己二酸的反应原理和实验装置示意图如下:
是一种工业上具有重要意义的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用,能够发生成盐反应、酯化反应等,并能与二元醇缩聚成高分子聚合物等,己二酸产量居所有二元羧酸中的第二位.实验室合成己二酸的反应原理和实验装置示意图如下:
![]()

可能用到的有关数据如下:
物质 | 密度(20℃) | 熔点 | 沸点 | 溶解性 | 相对分子质量 |
环己醇 | 0.962g/cm3 | 25.9℃ | 160.8℃ | 20℃时水中溶解度3.6g,可混溶于乙醇、苯 | 100 |
乙二酸 | 1.36g/cm3 | 152℃ | 337.5℃ | 在水中的溶解度:15℃时,1.44g,25℃时2.3g,易溶于乙醇,不溶于苯 | 146 |
实验步骤如下:
I、在三口烧瓶中加入16mL50%的硝酸(密度为1.31g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4mL环己醇。
Ⅱ、水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间。
Ⅲ、当环己醇全部加入后,将混合物用80℃~90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止。
IV、趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤得粗产品。
V、粗产品经提纯后称重为5.7g。
请回答下列问题:
(1)滴液漏斗的细支管a的作用是_____________,仪器b的名称为_____________。
(2)已知用NaOH溶液吸收尾气时发生的相关反应方程式为:
2NO2+2NaOH═NaNO2+NaNO3+H2O,NO+NO2+2NaOH═2NaNO2+H2O;如果改用纯碱溶液吸收尾气时也能发生类似反应,则相关反应方程式为:_____________、_____________。
(3)向三口烧瓶中滴加环己醇时,要控制好环己醇的滴入速率,防止反应过于剧烈导致温度迅速上升,否则。可能造成较严重的后果,试列举一条可能产生的后果:_____________。
(4)为了除去可能的杂质和减少产品损失,可分别用冰水和_____________洗涤晶体。
(5)粗产品可用_____________法提纯(填实验操作名称).本实验所得到的己二酸产率为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修5有机化学基础】有机物H是一种具有很强的亲水性高分子化合物。其合成路线如下:
![]()

已知:
①R—CHO+![]()
![]()

![]()
![]() ;
;
②![]()
![]()
![]() ;
;
③B的核磁共振氢谱有两个峰,且峰面积之比为1∶2。
请回答下列问题:
(1)A的名称是____________;B的官能团名称是______________________;
D的结构简式是____________________。
(2)反应⑤的反应类型是__________。
(3)反应④的化学方程式为______________________________。
(4)C的同分异构体中含有![]() 的有_________种。其中能与NaHCO3反应产生气体的同分异构体的结构简式是_________________________________。
的有_________种。其中能与NaHCO3反应产生气体的同分异构体的结构简式是_________________________________。
(5)根据已有知识并结合相关信息,仿上述流程,有机物以结构简式来表示,写出以甲苯和乙醛为原料制备肉桂醛( )的合成路线流程图(无机试剂任用):
)的合成路线流程图(无机试剂任用):
______________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学中常见有机物转化关系(部分相关物质和反应条件已略去)
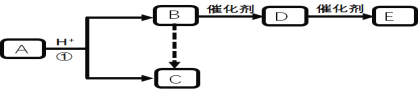
已知:Ⅰ. C的相对分子质量为60,且分子中碳元素的质量分数为40% 。
Ⅱ.B、 C、D分子含碳原子个数相同;E为高分子化合物。
回答下列问题:
(1)B中含有的官能团名称为 。
(2)E中链节为 。
(3)写出反应①的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com