
【题目】CO2是一种廉价的碳资源,其综合利用具有重要意义。
(一)CO2的化学捕获:
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为___(写含碳粒子符号)。(室温下,H2CO3的Ka1=4.3×10﹣7;Ka2=5.6×10﹣11)
(2)固体氧化物电解池(SOEC)用于高温共电解CO/H2,既可实现CO2的减排又可高效制备合成气(CO/H2),其工作原理如图。写出电极A发生的电极反应式___。

(二)CO2的综合利用
(1)CO2与CH4经催化重整制得合成气:
反应Ⅰ.CH4(g)H+CO2(g)2CO(g)+2H2(g)△H1
已知氢气、一氧化碳和甲烷的标准燃烧热(25℃)如表所示
物质 | H2(g) | CO(g) | CH4(g) |
标准燃烧热△H/kJmol﹣1 | ﹣285.8 | ﹣283.0 | ﹣890.3 |
则反应I的△H=___kJmol﹣1。
(2)用CO2催化加氢制取二甲醚的反应为:反应Ⅱ.2CO2(g)+6H2(g)CH3OCH3(g)+3H2O(g),在10L恒容密闭容器中,均充入2mol CO2和6moH2,分别以铱(Ir)和铈(Ce)作催化剂,反应进行相同的时间后测得的CO2的转化率α(CO2)随反应温度的变化情况如图1。

①根据图1,下列说法不正确的是___。
A.反应Ⅱ的△H<0,△S<0
B.用Ir和Ce作催化剂时,反应Ⅱ的活化能更低的是Ce
C.状态d时,v(正)<v(逆)
D.从状态b到d,α(CO2)先增大后减小,减小的原因可能是温度升高平衡逆向移动
②状态e(900K)时,α(CO2)=50%,则此时的平衡常数K=___。
③若H2和CO2的物质的量之比为n:1,900K时相应平衡体系中二甲醚的物质的量分数为x,请在图2中绘制x随n变化的示意图。_______
【答案】CO32﹣ CO2+2e﹣═CO+O2﹣、H2O+2e﹣=H2+O2﹣ +247.3 BC ![]() 或23.15
或23.15 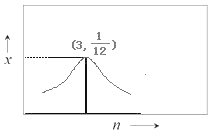
【解析】
(一)(1)K2=![]() =5×10﹣11,当溶液的pH=13,c(H+)=10-13,有
=5×10﹣11,当溶液的pH=13,c(H+)=10-13,有![]() =
=![]() =500,即c(CO32﹣)>>c(HCO3﹣);
=500,即c(CO32﹣)>>c(HCO3﹣);
(2)电解池中,根据O2-移动方向可知:A电极为阴极,该电极上发生还原反应,CO2、H2O分别在A极得到电子发生还原反应生成CO、H2,同时生成O2-;
(二)(1)写出H2、CO、CH4燃烧热的热化学方程式:①H2(g)+![]() O2(g)=H2O(g)△H=﹣285.8kJmol﹣1、②CO(g)+
O2(g)=H2O(g)△H=﹣285.8kJmol﹣1、②CO(g)+![]() O2(g)=CO2(g)△H=﹣283.0kJmol﹣1、③CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=﹣890.3kJmol﹣1,再利用盖斯定律求出CH4(g)H+CO2(g)=2CO(g)+2H2(g)的△H1;
O2(g)=CO2(g)△H=﹣283.0kJmol﹣1、③CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=﹣890.3kJmol﹣1,再利用盖斯定律求出CH4(g)H+CO2(g)=2CO(g)+2H2(g)的△H1;
(2)①A.反应2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g)正向是体积减小的反应,△S<0;由图1可知,状态d是用Ce作催化剂的平衡状态,随着温度的升高,反应物CO2的转化率降低,说明反应正向放热;
B.催化剂能降低反应物的活化能,加快反应速率,使可逆反应快速达到平衡,用Ce作催化剂时,CO2的转化率小、且比用Ir作催化剂后达到平衡,即反应速率小;
C.状态d是使用两种催化剂时一定温度下,某一时刻的平衡状态,反应速率不变;
D.状态b到d是用Ir作催化剂的平衡体系,平衡状态d相对开始平衡(750℃左右)时,α(CO2)减小主要由温度影响,可能平衡逆向移动;
②α(CO2)=50%,则c(CO2)的变化量为0.2mol·L-1×50%=0.1mol·L-1,利用三段式列式,求出平衡量,再求出平衡常数k;
③H2和CO2的物质的量之比为n:1,随着H2的增加,即H2和CO2的物质的量之比增大,平衡体系中CO2的转化率增大,二甲醚的物质的量分数x也增大,当n:1=6:2=3:1时,x值最大;当n:1>3:1时,x值逐渐减小;当n=3时,x=1/12。
(一)(1)K2=![]() =5×10﹣11,当溶液的pH=13,c(H+)=10﹣13,有
=5×10﹣11,当溶液的pH=13,c(H+)=10﹣13,有![]() =
=![]() =500,即c(CO32﹣)>>c(HCO3﹣),所以该溶液中含碳粒子以阴离子CO32﹣为主;
=500,即c(CO32﹣)>>c(HCO3﹣),所以该溶液中含碳粒子以阴离子CO32﹣为主;
(2)根据电解池中O2﹣移动方向推断:A电极为阴极,该电极上发生还原反应,CO2、H2O分别在A极得到电子发生还原反应生成CO、H2,同时生成O2,所以CO2在A极反应式为:CO2+2e﹣═CO+O2﹣,H2O在A电极反应式为:H2O+2e﹣=H2+O2﹣;
(二)(1)H2、CO、CH4燃烧热的热化学方程式分别为:①H2(g)+![]() O2(g)=H2O(g)△H=﹣285.8kJmol﹣1、②CO(g)+
O2(g)=H2O(g)△H=﹣285.8kJmol﹣1、②CO(g)+![]() O2(g)=CO2(g)△H=﹣283.0kJmol﹣1、③CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=﹣890.3kJmol﹣1,再利用盖斯定律、依据总反应有:③﹣2×②﹣2×①,△H1=﹣890.3kJmol﹣1﹣(﹣283.0kJmol﹣1)﹣2×(﹣285.8kJmol﹣1)=+247.3kJmol﹣1;
O2(g)=CO2(g)△H=﹣283.0kJmol﹣1、③CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=﹣890.3kJmol﹣1,再利用盖斯定律、依据总反应有:③﹣2×②﹣2×①,△H1=﹣890.3kJmol﹣1﹣(﹣283.0kJmol﹣1)﹣2×(﹣285.8kJmol﹣1)=+247.3kJmol﹣1;
(2)①A.反应2CO2(g)+6H2(g)CH3OCH3(g)+3H2O(g)正向是体积减小的反应,△S<0;由图1可知,随着温度的升高,反应物CO2的转化率降低,说明平衡逆向移动,逆反应吸热,则反应正向放热,故A正确;
B.催化剂能降低反应物的活化能,使可逆反应快速达到平衡,用Ce作催化剂时,CO2的转化率小、且比用Ir作催化剂后达到平衡,说明用Ir作催化剂时反应物的活化能高、反应速率小,故B错误;
C.状态d是800℃时某一时刻的平衡状态,反应速率不变,v(正)=v(逆),故C错误;
D.用Ir作催化剂的平衡体系,不平衡状态b到d平衡状态,α(CO2)先增大后减小,状态d相对开始平衡(750℃左右)时,α(CO2)减小的主要是温度升高,可能平衡逆向移动,故D正确;
故选:BC;
②α(CO2)=50%,则c(CO2)的变化量为0.2mol/L×50%=0.1mol/L,三段式列式为:
2CO2(g)+6H2(g)CH3OCH3(g)+3H2O(g)
初始浓度:0.2 0.6 0 0
变化浓度:0.1 0.3 0.05 0.15
平衡浓度:0.1 0.3 0.05 0.15
K=![]() =
=![]() =
=![]() ≈23.15;
≈23.15;
③H2和CO2的物质的量之比为n:1,随着H2的增加,即H2和CO2的物质的量之比增大,平衡体系中CO2的转化率增大,二甲醚的物质的量分数x也增大,当n:1=6:2=3:1时,x值最大;当n:1>3:1时,x值逐渐减小;当n=3时,x=![]() ;故答案为:
;故答案为: 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,将1mol PCl5通入一个容积固定不变的密闭容器中,发生反应:PCl5(g) ![]() PCl3(g) + Cl2(g),反应达到平衡时,测得PCl5为0.4mol,此时再向容器中通入1mol PCl5,同样温度下再达到平衡时,测得PCl5为amol,下列判断正确的是
PCl3(g) + Cl2(g),反应达到平衡时,测得PCl5为0.4mol,此时再向容器中通入1mol PCl5,同样温度下再达到平衡时,测得PCl5为amol,下列判断正确的是
A. Cl2的体积分数增大 B. PCl5的分解率增大
C. a = 0.8 D. a > 0.8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知同温同压下,下列反应的焓变和平衡常数分别表示如下,有关说法正确的是( )
(1)2SO2(g)+O2(g) ![]() 2SO3(g) △Hl=-197 kJ/mol K1=a
2SO3(g) △Hl=-197 kJ/mol K1=a
(2)2NO(g)+O2(g) ![]() 2NO2(g) △H2=-144 kJ/mol K2=b
2NO2(g) △H2=-144 kJ/mol K2=b
(3)NO2(g)+SO2(g) ![]() SO3(g)+NO(g) △H3=m kJ/mol K3=c
SO3(g)+NO(g) △H3=m kJ/mol K3=c
A. m=26.5 c2= a/b B. m--26.5 2c=a-b C. m=-170.5 2c=a-b D. m=53 c2=a/b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象与实验操作不相匹配的是
实验操作 | 实验现象 | |
A | 向盛有高锰酸钾酸性溶液的试管中通入足量的乙烯后静置 | 溶液的紫色逐渐褪去,静置后溶液分层 |
B | 将镁条点燃后迅速伸入集满CO2的集气瓶 | 集气瓶中产生浓烟并有黑色颗粒产生 |
C | 向盛有饱和硫代硫酸钠溶液的试管中滴加稀盐酸 | 有刺激性气味气体产生,溶液变浑浊 |
D | 向盛有FeCl3溶液的试管中加过量铁粉,充分振荡后加1滴KSCN溶液 | 黄色逐渐消失,加KSCN后溶液颜色不变 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解质溶液说法错误的是( )
A.室温下,pH相同的NaOH溶液和![]() 溶液,水的电离程度后者大
溶液,水的电离程度后者大
B.向![]()
![]()
![]() 溶液中加入少量水,溶液中的所有离子的浓度都减小
溶液中加入少量水,溶液中的所有离子的浓度都减小
C.![]() 的
的![]() 和
和![]() 的NaOH溶液以任意比例混合:
的NaOH溶液以任意比例混合:![]()
D.pH相同的a.![]() 溶液
溶液![]() 溶液c.
溶液c.![]() 溶液的溶液中
溶液的溶液中![]() 的大小顺序是a>b>c
的大小顺序是a>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钒钛磁铁矿炼钢后剩余的尾渣中含有V2O3、MgO、Al2O3、Fe2O3、SiO2等,现从该
钒渣中回收V2O3的工艺流程如下:

(1)滤液I的成分是NaVO3、NaAlO3和_________(写化学式)。
(2)检验滤渣I中是否含有Fe2O3的方法是_________________。
(3)用离子方程式表示NaAlO3溶液具有碱性的原因_________________。
(4)加入硫酸铵溶液后溶液的pH会有所降低,已知常温时氨水的电离平衡常数Kb=2×10-5;则0.1 mol·L-1 (NH4)2SO4溶液的PH约为__________。
(5)在沉钒操作中,选择使用(NH4)2SO4比使用(NH4)2CO3的沉钒效率高,其原因为___________。
(6)NH4VO3和Na2SO4的混合液需要经过蒸发浓缩、趁热过滤、冷却结晶和过滤等操作得到NH4VO3晶体,结合下图,分析为了得到较纯净的NH4VO3晶体和较高的晶体析出率,应选择最适宜的结晶温度,为a、b、c、d四点中______点对应的温度。

(7)最后制备V2O3时煅烧的温度不宜过高,当温度在1000℃时,偏钒酸铵(NH4VO3)会分解生成V2O3>和N2以及其他常见的氧化物,请写出偏钒酸铵在1000℃时分解的化学方程式:___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
物质 | Al | Al2O3 | Fe | Fe2O3 |
熔点/℃ | 660 | 2054 | 1535 | 1462 |
沸点/℃ | 2467 | 2980 | 2750 | -- |
I.该同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是:该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金。请你设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是_______,反应的离子方程式为____________________________。
Ⅱ. 实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。试回答下列问题:
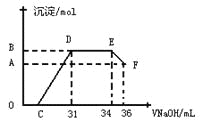
(1)图中OC段没有沉淀生成,此阶段发生反应的离子为:___________________。
(2)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方为_________。
(3)当c=13mL时,原溶液中Fe3+与Al3+的物质的量之比为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会对环境造成严重影响。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160 kJ/mol
则甲烷直接将NO2还原为N2的热化学方程式为______________。
(2)脱碳。将CO2转化为甲醇的热化学方程式为:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
①该反应的平衡常数表达式为_____________。
②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如右图所示。
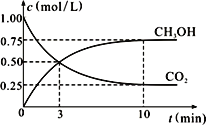
试回答:0~10 min内,氢气的平均反应速率为______________mol/(L·min)。
(3)脱硫。
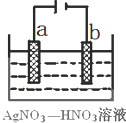
①有学者想利用如图所示装置用原电池原理将SO2转化为重要的化工原料,A、B是惰性电极。
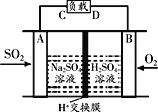
A极的电极反应式为_____________。
②某种脱硫工艺中将废气处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物,可作为化肥。硫酸铵和硝酸铵的水溶液pH<7,常温下,向一定物质的量浓度的硝酸铵溶液中滴加适量的氨水溶液,使溶液中的NO3-和NH4+的物质的量浓度相等,则溶液的pH__________7(填写“>”“=”或“<”)。
(4)金属冶炼和金属化合物处理常涉及氧化还原反应。
若用惰性电极电解饱和NaCl溶液一段时间当阳极产生56 mL(标准状况下)气体,电解后溶液体积为500 mL时,求所得溶液在25℃时的pH =__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能使H2O+H2O![]() H3O++OH-电离平衡向正反应方向移动,且所得溶液呈酸性的是
H3O++OH-电离平衡向正反应方向移动,且所得溶液呈酸性的是
A.在水中加Na2CO3固体B.在水中加入CuCl2固体
C.在水中加入稀硫酸D.将水加热到99℃,其中c(H+)=1×10-6mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com