
| A.CO32-+H2O?HCO3-+OH-用热的纯碱溶液清洗油污 |
| B.Al3++3H2O?Al(OH)3(胶体)+3H+:明矾净水 |
| C.Al3++3HCO3-?Al(OH)3↓+3CO2↑:泡沫灭火器灭火 |
| D.SnCl2+H2O?Sn(OH)Cl↓+HCl配制氯化亚锡溶液时加入氢氧化钠溶液 |
科目:高中化学 来源:不详 题型:问答题
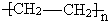 的单体是______.
的单体是______.查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.某些铁盐溶于水生成的Fe(OH)3胶体,可除去水中的悬浮颗粒等杂质 |
| B.维生素C高温时容易被破坏,所以不宜热锅爆炒蔬菜 |
| C.构成人体蛋白质的20多种氨基酸都能通过人体自身合成 |
| D.可用燃烧的方法鉴别真丝围巾和合成纤维围巾 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.明矾溶于水形成的Al(0H)3胶体能吸附水中悬浮物,可用于水的净化 |
| B.用氧化铝坩埚加热熔化氢氧化钠固体 |
| C.二氧化硅可以用于制造光导纤维 |
| D.硅用作太阳能电池材料 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.均存在电离平衡和水解平衡 |
| B.存在的粒子种类相同 |
| C.c(OH-)前者小于后者 |
| D.分别加入NaOH固体,恢复到原温度,c(CO32-)均增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
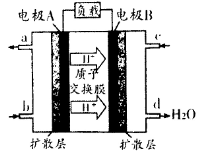
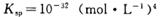 ,当Cr3+浓度小于10
,当Cr3+浓度小于10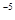 mol
mol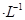 时可认为完全沉淀,电解完全后,测得溶液的pH=6,则该溶液过滤后为___________(填“能”或“否”)直接排放。
时可认为完全沉淀,电解完全后,测得溶液的pH=6,则该溶液过滤后为___________(填“能”或“否”)直接排放。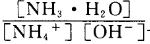 ________(填“增大”“减小”或“不变”);25
________(填“增大”“减小”或“不变”);25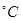 时,NH3?H2O的电离平衡常数
时,NH3?H2O的电离平衡常数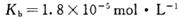 ,该温度下,1mol
,该温度下,1mol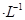 的NH4Cl溶液中
的NH4Cl溶液中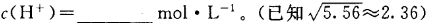
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com