
���� ��1��ʵ�����ü����Ȼ�����������Ʒ�����ȡ������
��2���ٰ�������������һ��������ˮ��
�ڰ�������������һ��������ˮ������������ˮ��Ӧ���������һ��������һ�������������ɶ�������������һ����������ѭ��ʹ�ã����������ᷴӦ��������泥�������Ӽ������ۼ������жϣ�
��ͭ��ϡ���ᷴӦ��������ͭ��һ��������ˮ��
��3���ټ��ȵ�����Ʒ�����������壬����һ��������ʹʪ��ĺ�ɫʯ����ֽ������������Ϊ������˵������笠����ӣ���һ��������ʹ����ʯ��ˮ����ǣ�˵��̼������ӻ�̼��������ӣ���ȡ�����õ�����Ʒ����ˮ������������BaCl2��Һ��û�����Ա仯��˵��û��̼��������ӣ��ɴ��Ƶ������ʵ���Ҫ�ɷ֣�
��� �⣺��1��ʵ�����Ʊ������������Ȼ�狀��������ƹ�����������Ȼ��ơ�������ˮ����Ӧ�Ļ�ѧ����ʽΪ��2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��
�ʴ�Ϊ��2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��
��2���ٰ�������������һ��������ˮ������ʽ��4NH3+5O2$\frac{\underline{\;����\;}}{��}$4NO+6H2O���ʴ�Ϊ��4NH3+5O2$\frac{\underline{\;����\;}}{��}$4NO+6H2O��
�ڰ�������������һ��������ˮ������������ˮ��Ӧ���������һ��������һ�������������ɶ�������������һ����������ѭ��ʹ�ã����������ᷴӦ��������泥�笠����������������ͨ�����Ӽ���ϣ�笠������е�ԭ������ԭ�ӣ�����������е�ԭ������ԭ��ͨ�����ۼ���ϣ�����������к������Ӽ������ۼ���
�ʴ�Ϊ��NO�����Ӽ������ۼ���
��ͭ��ϡ���ᷴӦ��������ͭ��һ��������ˮ�����ӷ���ʽ��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��
�ʴ�Ϊ��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��
��3���ټ��ȵ�����Ʒ�����������壬����һ��������ʹʪ��ĺ�ɫʯ����ֽ������������Ϊ������˵������笠����ӣ���һ��������ʹ����ʯ��ˮ����ǣ�˵��̼������ӻ�̼��������ӣ���ȡ�����õ�����Ʒ����ˮ������������BaCl2��Һ��û�����Ա仯��˵��û��̼��������ӣ�˵�����к���笠����Ӻ�̼������ӣ����Ե��ʵ���Ҫ�ɷ�NH4HCO3�����ʵ���Һ������NaOH��Һ�ڼ��������·�Ӧ�����ӷ���ʽΪ��NH4++HCO3-+2OH-=NH3��+CO32-+2H2O��
�ʴ�Ϊ��NH4HCO3��NH4++HCO3-+2OH-=NH3��+CO32-+2H2O��
���� ����Ϊ�ۺ��⣬�����˰������Ʊ���������Ʊ������ʼ��飬��Ϥ��������ε������ǽ���ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��� | B�� | �ٸ��� | C�� | �ڸ��� | D�� | ���ж� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
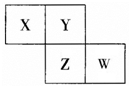 X��Y��Z��W��Ϊ������Ԫ�أ�������Ԫ�����ڱ������λ����ͼ��ʾ����֪Wԭ�ӵ��������������ڲ��������3 ��������˵����ȷ���ǣ�������
X��Y��Z��W��Ϊ������Ԫ�أ�������Ԫ�����ڱ������λ����ͼ��ʾ����֪Wԭ�ӵ��������������ڲ��������3 ��������˵����ȷ���ǣ�������| A�� | �������Ӧˮ��������W��Zǿ | |
| B�� | Y������Z���⻯��ˮ��Һ��Ӧ���г������� | |
| C�� | X����������ǿ��Y���� | |
| D�� | �����ӵİ뾶��Z��W |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
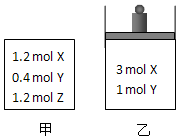 ���¶ȡ���ʼ�ݻ���ͬ�������ܱ������У�����ͬ��ʽͶ�뷴Ӧ���ͼ��ʾ�����������·�Ӧ��3X��g��+Y��g��?2Z��g����H��0�������¶Ȳ��䣬���ƽ��ʱ���й��������������˵����ȷ���ǣ�������
���¶ȡ���ʼ�ݻ���ͬ�������ܱ������У�����ͬ��ʽͶ�뷴Ӧ���ͼ��ʾ�����������·�Ӧ��3X��g��+Y��g��?2Z��g����H��0�������¶Ȳ��䣬���ƽ��ʱ���й��������������˵����ȷ���ǣ������� | ���������� | ��ѹ������ | |
| X�����ʵ�����mol�� | n1 | n2 |
| Z��������� | ��1 | ��2 |
| A�� | ƽ��ʱ�����ҵ��ݻ�һ���ȷ�ӦǰС | |
| B�� | ƽ��ʱ������ѹǿһ���ȷ�ӦǰС | |
| C�� | n2��n1 | |
| D�� | ��2����1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Q3��Q2��Q1 | B�� | Q1��Q3��Q2 | C�� | Q1=Q2=Q3 | D�� | Q2��Q3��Q1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
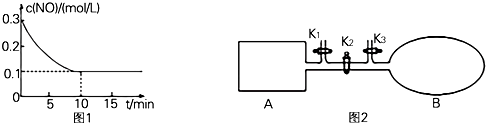
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com