
| 实验操作 | 实验目的 | |
| A | 取某溶液少许,依次加入BaCl2和稀盐酸 | 确定该溶液中含有SO42- |
| B | 向甲酸钠溶液中加新制的Cu(OH)2并加热 | 确定甲酸钠中含有醛基 |
| C | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中滴加稀盐酸有气泡产生. | 确定常温下BaCO3的溶解度比BaSO4小 |
| D | 将溴乙烷与氢氧化钠溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 | 检验水解产物中的溴离子 |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
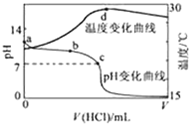 室温下,将1.000mol?L-1盐酸滴入20.00mL 1.000mol?L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )
室温下,将1.000mol?L-1盐酸滴入20.00mL 1.000mol?L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )| A、a点由水电离出的c(H+)=1.0×10-14mol/L |
| B、a、b之间可能出现:c(NH3?H2O)>c(NH4+)>c(OH-)>c(Cl-)>c(H+) |
| C、c点:c(Cl-)═c(NH4+) |
| D、d点后,溶液温度略下降的主要原因是NH3?H2O电离吸热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| △ |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、14CO和14N2 |
| B、O3和SO2 |
| C、CO2和N2O |
| D、N2H4和C2H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使pH试纸显深红色的溶液:NH4+、Mg2+、Cl-、NO3- |
| B、能使淀粉碘化钾试纸显蓝色的溶液:NH4+、Cu2+、S2-、SO42- |
| C、0.1mol.L-1碱溶液:Al3+、Fe3+、SO42-、Cl2 |
| D、由水电离的c(H+)=10-12mol?L-1的溶液:K+、Na+、SiO32-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | C(I-)/mol?L | C(S2O82-)/mol?L | t/s |
| 1 | 0.040 | 0.040 | 88.0 |
| 2 | 0.080 | 0.040 | 44.0 |
| 3 | 0.080 | 0.080 | 22.0 |
| 4 | 0.160 | 0.020 | 44.0 |
| 5 | 0.120 | 0.040 | 29.3 |
| A、该实验的目的是研究 I- 与S2O82- 的浓度对反应速率的影响 |
| B、I-的浓度越大,反应速率越快 |
| C、S2O82- 的浓度越小,反应速率越快 |
| D、5个实验中,编号3对应浓度的实验,反应速率最快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、H2O的电子式为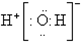 |
| B、4℃时,纯水的pH=7 |
| C、D216O中,质量数之和是质子数之和的两倍 |
| D、水分子在三种状态中,分子间的平均距离d:d(气态)>d(液态)>d(固态) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④ | B、①③⑤ |
| C、②④⑥ | D、③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com