
【题目】下列离子反应方程式正确的是
A.向NaAlO2溶液中通入过量CO2制Al(OH)3:2![]() +CO2+3H2O=2Al(OH)3↓+
+CO2+3H2O=2Al(OH)3↓+![]()
B.用硫酸酸化的淀粉碘化钾溶液在空气中变蓝:4I-+O2+4H+=2I2+2H2O
C.漂白粉溶液通入少量SO2:Ca2++2ClO-+SO2+H2O=2HClO+CaSO3↓
D.Na2O2溶于水产生O2:Na2O2+H2O=2Na++2OH-+O2↑
【答案】B
【解析】
A.向NaAlO2溶液中通入过量CO2制Al(OH)3,由于二氧化碳过量,生成氢氧化铝沉淀和碳酸氢钠,离子方程式为:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,故A错误;
B.用硫酸酸化的淀粉碘化钾溶液在空气中变蓝,碘离子具有还原性,被空气中的氧气氧化为单质碘,碘单质遇淀粉变蓝,反应的离子方程式为4I-+O2+4H+═2H2O+2I2,故B正确;
C.漂白粉溶液通入少量SO2,由于次氯酸根离子具有强的氧化性,能够氧化二氧化硫生成硫酸根离子,其离子方程式为:SO2+Ca2++3ClO-+H2O=CaSO4↓+2HClO+Cl-,故C错误;
D.Na2O2与水反应生成氢氧化钠和O2,正确的离子方程式为:2Na2O2+2H2O═4Na++4OH-+O2↑,题目中离子方程式氧原子个数不等,故D错误;
答案B。


科目:高中化学 来源: 题型:
【题目】某温度时,在体积为2 L的密闭容器中,气态物质A、B、E、F的物质的量n随时间t的变化情况如图甲所示,在一定条件下反应达到平衡状态,反应进程中正反应速率随时间的变化情况如图乙所示,在t2、t4时刻分别只改变一个条件(温度、压强或某反应物的量)。下列说法错误的是( )

A. 此温度下,该反应的化学方程式为2A(g)+E(g)![]() 2B(g)+F(g)
2B(g)+F(g)
B. 若平衡状态①和②对应的温度相同,则①和②对应的平衡常数K一定相同
C. t2时刻改变的条件是增大压强
D. t4时刻改变的条件是降低温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(ClNO)是有机合成中的重要试剂,可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+Cl2(g)![]() 2ClNO(g)。
2ClNO(g)。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:① 2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) K1;②4NO2(g)+2NaCl(s)
NaNO3(s)+ClNO(g) K1;②4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) K2;③2NO(g)+Cl2(g)
2NaNO3(s)+2NO(g)+Cl2(g) K2;③2NO(g)+Cl2(g)![]() 2ClNO(g) K3,则K1、K2、K3之间的关系为K3=_______________(用K1和K2表示);
2ClNO(g) K3,则K1、K2、K3之间的关系为K3=_______________(用K1和K2表示);
(2)已知几种化学键的键能数据如下表:(亚硝酰氯的结构为Cl—N==O)
化学键 | N≡O | Cl-Cl | Cl-N | N==O |
键能/(kJ·mol-1) | 630 | 243 | a | 607 |
则2NO(g)+Cl2(g)![]() 2ClNO(g)的反应的 △H和a的关系为 △H = ___kJ·mol-1。
2ClNO(g)的反应的 △H和a的关系为 △H = ___kJ·mol-1。
(3)300℃时,2NO(g)+Cl2 (g)![]() 2ClNO(g)的正反应速率表达式为v正 = k·cn (ClNO),测得速率和浓度的关系如下表:
2ClNO(g)的正反应速率表达式为v正 = k·cn (ClNO),测得速率和浓度的关系如下表:
序号 | c(ClNO)/(mol·L-1) | v/(mol·L-1·s-l) |
① | 0. 30 | 3. 60×10-9 |
② | 0. 60 | 1. 44×10-8 |
③ | 0. 90 | 3. 24×10-8 |
n = ___;k = ____。
(4)若向绝热恒容密闭容器中充入物质的量之比为2 : 1的NO和Cl2进行反应2NO(g)+Cl2(g)![]() 2ClNO(g),能判断反应已达到化学平衡状态的是__(填标号)。
2ClNO(g),能判断反应已达到化学平衡状态的是__(填标号)。
a.容器中的压强不变 b.2v正(NO) = v逆(Cl2)c.气体的平均相对分子质量保持不变 d.该反应平衡常数保持不变e.NO和Cl2的体积比保持不变
(5)25℃时,向体积为2 L且带气压计的恒容密闭容器中通入0.08 mol NO和0.04 mol Cl2发生反应:2NO(g)+Cl2 (g)![]() 2ClNO(g)△H。
2ClNO(g)△H。
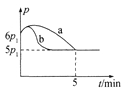
①若反应起始和平衡时温度相同,测得反应过程中压强(p)随时间(t)的变化如图甲曲线a所示,则 △H __(填“>”“<”或“不确定”)0;若其他条件相同,仅改变某一条件时,测得其压强(p)随时间(t)的变化如图甲曲线b所示,则改变的条件是______。
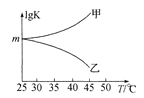
②图是甲、乙同学描绘上述反应平衡常数的对数值(lg K)与温度的变化关系,其中正确的曲线是____(填“甲”或“乙”),m值为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4·7H2O),过程如下:
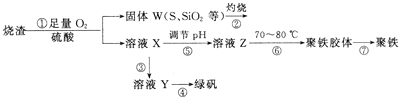
(1)将过程②中产生的气体通入下列溶液中,溶液不会褪色的是_____(填标号)。
A.品红溶液 B.紫色石蕊溶液 C.酸性KMnO4溶液 D.溴水
(2)过程①中,FeS和O2、H2SO4反应的离子方程式为_________。
(3)过程③中,需加入的物质是__________。
(4)实验室为测量所得到的聚铁样品中铁元素的质量分数,进行下列实验。①用分析天平称取2. 800 g样品;②将样品溶于足量的盐酸后,加入过量的氯化钡溶液;③过滤、洗涤、干燥,称量,得固体质量为3. 495 g。若该聚铁主要成分为[Fe(OH) (SO4)]n,则该聚铁样品中铁元素的质量分数为____________(假设杂质中不含铁元素和硫元素)。
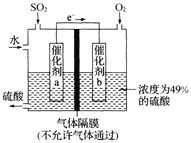
(5)如图是将过程②产生的气体SO2转化为重要的化工原料H2SO4的原理示意图,若得到的硫酸浓度仍为49%,则理论上参加反应的SO2与加入的H2O的质量比为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】因瓦合金俗称殷钢,是一种镍铁合金,由于其膨胀系数极小,又称不变合金,适合做测量元件。回答下列问题:
![]() 基态镍原子的价电子轨道表达式为____;铁的基态原子核外未成对电子数为___个。
基态镍原子的价电子轨道表达式为____;铁的基态原子核外未成对电子数为___个。
![]() 丁二酮肟
丁二酮肟![]() 分子式为
分子式为![]() 所含的碳、氮、氧三种元素中第一电离能最大的是_____
所含的碳、氮、氧三种元素中第一电离能最大的是_____![]() 填元素符号
填元素符号![]() 。在稀氨水介质中,
。在稀氨水介质中,![]() 与丁二酮肟
与丁二酮肟![]() 分子式为
分子式为![]() 反应可生成鲜红色沉淀,其分子结构如图所示,该结构中碳原子的杂化方式为_______;该结构中除含极性键、非极性键、配位键外,还含有__________。
反应可生成鲜红色沉淀,其分子结构如图所示,该结构中碳原子的杂化方式为_______;该结构中除含极性键、非极性键、配位键外,还含有__________。
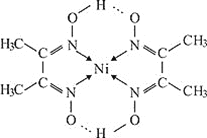
![]() 铁、镍易与CO作用形成羰基配合物
铁、镍易与CO作用形成羰基配合物![]() 、
、![]() 。1个
。1个![]() 分子中含有
分子中含有![]() 键数目为_______;已知
键数目为_______;已知![]() 分子为正四面体构型,下列溶剂能够溶解
分子为正四面体构型,下列溶剂能够溶解![]() 的是_______
的是_______![]() 填写字母
填写字母![]() 。
。
A.四氯化碳 ![]() 苯
苯 ![]() 水
水 ![]() 液氨
液氨
![]() 经查氯化亚铁的熔点为
经查氯化亚铁的熔点为![]() ,沸点为
,沸点为![]() ;而氯化铁的熔点为
;而氯化铁的熔点为![]() ,沸点为
,沸点为![]() 。二者熔沸点差异较大的原因是___________。
。二者熔沸点差异较大的原因是___________。
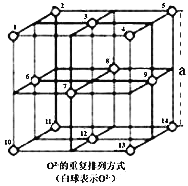
![]() 晶体中,
晶体中,![]() 的重复排列方式如图所示,该排列方式中存在着由如1、3、6、7的
的重复排列方式如图所示,该排列方式中存在着由如1、3、6、7的![]() 围成的正四面体空隙和3、6、7、8、9、12的
围成的正四面体空隙和3、6、7、8、9、12的![]() 围成的正八面体空隙;
围成的正八面体空隙;![]() 中有一半的
中有一半的![]() 填充在正四面体空隙中,另一半
填充在正四面体空隙中,另一半![]() 和
和![]() 填充在正八面体空隙中。则
填充在正八面体空隙中。则![]() 晶体中,正四面体空隙数与
晶体中,正四面体空隙数与![]() 数之比为_______。
数之比为_______。![]() 晶体密度为
晶体密度为![]() ,请计算
,请计算![]() _______
_______![]() 写出计算表达式即可
写出计算表达式即可![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A.无色透明的溶液中: Fe3+、Mg2+、SCN 、Cl
B.![]() =1×10-12的溶液中:K+、Na+、CO32、NO3
=1×10-12的溶液中:K+、Na+、CO32、NO3
C.![]() 的溶液中: K+、NH4+、MnO4、SO42-
的溶液中: K+、NH4+、MnO4、SO42-
D.能使甲基橙变红的溶液中: Na+、NH4+、SO42-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
A.  B.
B.  C.
C. 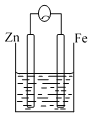
(1)A中反应的离子方程式为_____,B中Cu极电极反应式为______。
(2)C中被腐蚀的金属是____________,总反应方程式为____________,
(3)A、B、C中铁被腐蚀的速率,由大到小的顺序是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组为制备消毒液(主要成分是NaClO)设计了下列装置,并查阅下列资料:在温度较高情况下卤素单质和碱溶液能发生如下反应:3X2+6OH-![]() 5X-+XO3-+3H2O
5X-+XO3-+3H2O
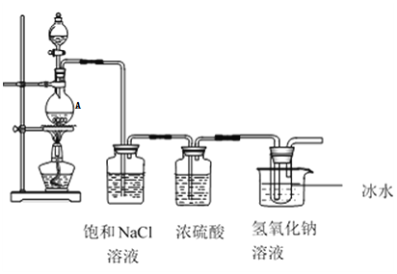
回答下列问题:
(1)仪器 A的名称为_______发生装置中反应的离子方程式为:____。
(2)饱和NaCl溶液的作用是______,能否省去盛有浓硫酸的洗气瓶_____,理由是______
(3)能否省去冰水冷却________,用化学方程式表示原因是:_______,大试管内发生反应的离子方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合硫酸铁[Fe2(OH)6-2n(SO4)n]m广泛用于水的净化。以FeSO4·7H2O为原料,经溶解、氧化、水解聚合等步骤,可制备聚合硫酸铁。
(1)将一定量的FeSO4·7H2O溶于稀硫酸,在约70 ℃下边搅拌边缓慢加入一定量的H2O2溶液,继续反应一段时间,得到红棕色黏稠液体。H2O2氧化Fe2+的离子方程式为________;水解聚合反应会导致溶液的pH________。
(2)测定聚合硫酸铁样品中铁的质量分数:准确称取液态样品3.000 g,置于250 mL锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的SnCl2溶液(Sn2+将Fe3+还原为Fe2+),充分反应后,除去过量的Sn2+。用5.000×102 mol·L1 K2Cr2O7溶液滴定至终点(滴定过程中![]() 与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00 mL。
与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00 mL。
①上述实验中若不除去过量的Sn2+,样品中铁的质量分数的测定结果将________(填“偏大”或“偏小”或“无影响”)。
②计算该样品中铁的质量分数(写出计算过程)_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com