
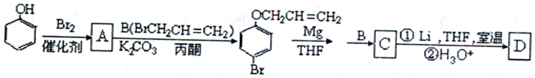
| Mg |
| THF |
| BrR2 |
| Li,THF室温 |
| H3O+ |
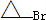 是化合物B的一种同分异构体,用核磁共振氢谱可以证明该化合物中有
是化合物B的一种同分异构体,用核磁共振氢谱可以证明该化合物中有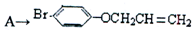 的有机反应类型
的有机反应类型| NaOH水溶液 |
| △① |
| HBr |
| ② |
| Cu,O2,△ |
| ③ |
| 新制Cu(OH)2 |
| △④ |
| 酸化 |
| ⑤ |
| -HBr |
| ⑥ |
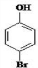 ,根据已知信息①可知C的结构简式是
,根据已知信息①可知C的结构简式是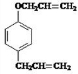 ,由信息②可知D的结构简式是
,由信息②可知D的结构简式是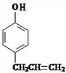 ,(4)中B的结构简式是CH2=CHCH2Br,B发生水解反应生成E为CH2=CHCH2OH,E和HBr发生加成反应生成F,则F是BrCH2CH2CH2OH,或CH3CH(Br)CH2OH,F氧化生成BrCH2CH2CHO或CH3CH(Br)CHO,继续被氧化、酸化生成BrCH2CH2COOH或CH3CH(Br)COOH,最后通过消去反应生成G,则G结构简式是CH2=CHCOOH.因为在氧化羟基的同时也易氧化碳碳双键所以为了保护碳碳双键,才设置反应②和⑥,G与甲醇反应生成的酯H,则H结构简式是CH2=CHCOOCH3,分子中含有碳碳双键,可发生加聚反应生成高聚物.
,(4)中B的结构简式是CH2=CHCH2Br,B发生水解反应生成E为CH2=CHCH2OH,E和HBr发生加成反应生成F,则F是BrCH2CH2CH2OH,或CH3CH(Br)CH2OH,F氧化生成BrCH2CH2CHO或CH3CH(Br)CHO,继续被氧化、酸化生成BrCH2CH2COOH或CH3CH(Br)COOH,最后通过消去反应生成G,则G结构简式是CH2=CHCOOH.因为在氧化羟基的同时也易氧化碳碳双键所以为了保护碳碳双键,才设置反应②和⑥,G与甲醇反应生成的酯H,则H结构简式是CH2=CHCOOCH3,分子中含有碳碳双键,可发生加聚反应生成高聚物. ,根据已知信息①可知C的结构简式是
,根据已知信息①可知C的结构简式是 ,由信息②可知D的结构简式是
,由信息②可知D的结构简式是 .
. ,C的结构简式为
,C的结构简式为 ,
, ;
; ;
; 是化合物B的一种同分异构体,用核磁共振氢谱可以证明该化合物中有2种氢处于不同的化学环境,
是化合物B的一种同分异构体,用核磁共振氢谱可以证明该化合物中有2种氢处于不同的化学环境, 转化中A中羟基中H原子被取代,属于取代反应,
转化中A中羟基中H原子被取代,属于取代反应,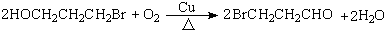 ,
,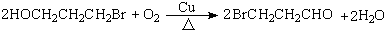 ;
; BrCH2CH2COOH+Cu2O↓+2 H2O,
BrCH2CH2COOH+Cu2O↓+2 H2O, BrCH2CH2COOH+Cu2O↓+2 H2O;
BrCH2CH2COOH+Cu2O↓+2 H2O;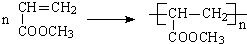 ,
, .
. )的同分异构体符合下列条件:①遇FeCl3溶液呈紫色,说明含有酚羟基;②苯环上有两个取代基,且苯环上的一氯代物有两种,两个不同的取代基处于对位,符合条件的同分异构体有:
)的同分异构体符合下列条件:①遇FeCl3溶液呈紫色,说明含有酚羟基;②苯环上有两个取代基,且苯环上的一氯代物有两种,两个不同的取代基处于对位,符合条件的同分异构体有: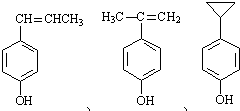 ,
, ;
;


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、1mol H2燃烧放出的热量为H2的燃烧热 |
| B、饱和石灰水中加入少量CaO,恢复至室温后溶液的c(Ca2+)不变 |
| C、铅蓄电池放电过程中,正极质量增加,负极质量减小 |
| D、为除去FeCl3溶液中的CuCl2,可通入H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、氯离子的结构示意图 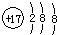 |
| B、HClO中Cl的化合价为:+1 |
| C、氯化钙的化学式:CaCl |
| D、硫酸的电离方程式:H2SO4=H2++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| 400℃ |
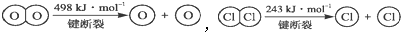 ,断开1molH-O键与断开1mol H-Cl键所需能量相差约为
,断开1molH-O键与断开1mol H-Cl键所需能量相差约为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(H+)=10-13mol/L的溶液中:NO3-、SO42-、K+、Na+ |
| B、澄清石灰水中:Na+、K+、CH3COO -、HCO3- |
| C、铁与稀硫酸反应后的溶液中:[Fe(CN)6]3-、NH4+、Cl-、NO3- |
| D、空气中:SO2、NO、N2、NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 制备并收集乙炔 |
B、 除去乙醇中溶有的少量乙酸 |
C、 制备少量乙酸乙酯 |
D、 石油的分馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 充电 |
| 放电 |
| A、该电池放电时,两极质量均增加 |
| B、放电时,正极的电极反应式为PbO2+4H++2e-═Pb2++2H2O |
| C、充电时,溶液中Pb2+向阳极移动 |
| D、充电时,阳极周围溶液的pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加水稀释过程中,c(H+):c(OH-) 的值增大 | ||
| B、根据以上信息,可推断NH3?H2O为弱电解质 | ||
C、与pH=11.12的 NaOH溶液相比,NaOH溶液中c(Na+) 大于氨水中c(NH
| ||
| D、加入少量NH4Cl 固体,溶液中水的电离平衡:H2O?H++OH-正向移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com