
【题目】下列除杂质的操作中不正确的是
A. Na2CO3 固体中混有少量NaHCO3:加热固体至质量恒定
B. NaHCO3溶液中混有少量Na2CO3:往该溶液中通入过量CO2气体
C. CO2中混有HCl:将其通过装NaOH溶液的洗气瓶
D. NaCl溶液中混有少量I2:加入适量CCl4,振荡,静置,分液
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】COCl2(g)![]() CO(g) + Cl2(g) ΔH > 0,当反应达到平衡时,改变一种反应条件,下列示意图正确的是 ( )
CO(g) + Cl2(g) ΔH > 0,当反应达到平衡时,改变一种反应条件,下列示意图正确的是 ( )

① ② ③ ④
A. ①表示随温度升高,平衡常数的变化
B. ②表示加入催化剂,反应速率随时间的变化
C. ③表示恒压条件下,反应物的转化率随充入惰性气体体积的变化
D. ④表示CO的体积分数随充入Cl2量的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1 L Na2SO4溶液中含Na+ 4.6 g, 则溶液中SO42- 浓度为
A. 0.1mol/LB. 0.4mol/L
C. 0.6mol/LD. 0.2mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸混合溶液200mL,平均分成甲、乙两份。向甲中逐渐加入铜粉,最多能溶解9.6克,向乙中逐渐加入铁粉,产生气体的量随铜粉质量的变化如下图所示(已知:Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O)。下列分析结果不正确的是( )

A. 原混合溶液中NO3一的物质的量浓度为4mol/L
B. AB段的反应为:Fe+2Fe3+=3Fe2+
C. C点时,乙中溶质为FeSO4
D. 标准状况下,OA、BC段产生的气体总体积约为4.48L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了图1置研究硝酸的性质.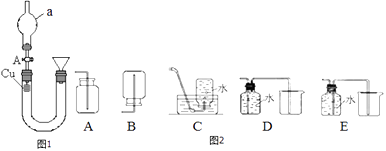
(1)实验一:甲组同学用图一装置来证实稀硝酸与铜反应生成NO.a.装置中a仪器的名称为 .
b.加入硝酸的操作:应先活塞A,然后从右管的漏斗中向U形管中逐渐注入稀硝酸.当注满后,应活塞A,此时观察到的现象 . 待反应一会后若打开活塞A,观察到的现象为 .
c.若要收集NO气体,如图2收集装置中合适的是(填序号) .
d.在100mL混合溶液中,HNO3和H2SO4的物质的量浓度分别是0.4mol/L、0.1mol/L向该混合液中加入1.92g铜粉,加热待充分反应后,所得溶液中Cu2+的物质的量浓度是 .
(2)实验二:乙组同学利用上述装置完成浓硝酸与铜的反应a.乙组同学发现实验室里有几瓶浓硝酸呈黄色,请用简单的文字和方程式解释这种现象 .
b.同学们发现浓硝酸与铜反应后的溶液呈绿色,而不显蓝色.甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了NO2气体所致.同学们分别设计了以下3个实验来判断两种看法是否正确.这些方案中可行的是 . (填序号,多选不给分)
①加热该绿色溶液,观察颜色变化
②加水稀释绿色溶液,观察颜色变化
③向该绿色溶液中通入氮气,观察颜色变化.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的废渣中混有少量的锌粉和氧化铜(其他成分不跟酸反应),跟大量废盐酸接触形成污水,产生公害。若向污水中撒入铁粉且反应后铁粉有剩余,此时污水中一定含有的金属离子是
A. Fe2+、Cu2+B. Zn2+、Fe2+C. Cu2+、 H+D. Zn2+ 、H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )。
A. 淀粉、油脂和蛋白质都是高分子化合物,且它们均为混合物
B. 煤、石油和天然气都是化石燃料,且它们均不能再生
C. 果糖、蔗糖和麦芽糖都能发生水解反应,且产物均为葡萄糖
D. 乙醛、乙酸和葡萄糖都能与新制的Cu(OH)2反应,且反应类型均为氧化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com