
(8分)五种短周期元素 A、B、C、D、E 的原子序数依次增大。A 的最高价氧化物与 B 的氢化物在水中反应得到的生成物既可与酸反应又可与碱反应。C、D 为金属元素,且 D 原子最外层电子数等于其 K 层电子数,而 C 的阳离子半径大于 D 的阳离子。若往 E 单质的水溶液中滴加少量紫色石蕊试液,能观察到先变红后褪色。请回答下列问题:
(1)C在元素周期表中的位置是 E的氢化物的电子式为
(2)B和 E 的氢化物相互反应得到的产物中含有化学键的类型是
(3)A、E 元素形成的化合物的结构式是
(4)D 单质能与A的最高价氧化物反应,写出反应的方程式
(1) 第三周期ⅠA族 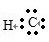 (2) 离子键、共价键 (3)
(2) 离子键、共价键 (3) 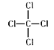
(4)2Mg + CO2 2MgO + C
2MgO + C
【解析】
试题分析:根据“C、D 为金属元素,且 D 原子最外层电子数等于其 K 层电子数”知道D是Mg,C 的阳离子半径大于 D 的阳离子,则C是Na;“往 E 单质的水溶液中滴加少量紫色石蕊试液,能观察到先变红后褪色”则E是Cl,A、B、C、D、E 的原子序数依次增大,那么A、B是第二周期的元素,A 的最高价氧化物与 B 的氢化物在水中反应得到的生成物既可与酸反应又可与碱反应,A、B应该是非金属,有这个现象的应该是CO2和NH3,所以A是C,B是N。(1)C是Na在元素周期表中的位置是第三周期ⅠA族, E 的氢化物为HCl的电子式为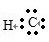 。(2))B和 E 的氢化物相互反应得到的产物NH4Cl,含有离子键和共价键。(3)A、E 元素形成的化合物是CCl4,结构式是
。(2))B和 E 的氢化物相互反应得到的产物NH4Cl,含有离子键和共价键。(3)A、E 元素形成的化合物是CCl4,结构式是 (4)D 单质能与A的最高价氧化物反应,就是Mg和CO2反应,反应的方程式为:2Mg + CO2
(4)D 单质能与A的最高价氧化物反应,就是Mg和CO2反应,反应的方程式为:2Mg + CO2 2Mg O + C
2Mg O + C
考点:元素在周期表中的位置的推断、电子式、结构式的书写。
考点分析: 考点1:物质的结构与性质 考点2:元素周期律与元素周期表 试题属性

科目:高中化学 来源:2014-2015学年河南省商丘市高三第一次模拟考试化学试卷(解析版) 题型:填空题
【选修2—化学与技术】(12分)水处理技术在生产、生活中应用广泛。
(1)工业上常用绿矾做混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理的水pH调到9左右,再加入绿矾。请解释这一做法的原因:_________。(用必要的离子方程式和文字描述)。
(2)根据水中Ca2+,Mg2+的多少,把天然水分为硬水和软水,硬水必须经过软化才能使用。
①硬水软化的方法通常有___________、__________和离子交换法。离子交换树脂使用了一段时间后,逐渐由NaR型变为CaR2(或MgR2)型,而失去交换能力。把CaR2(或MgR2)型树酯置于______________中浸泡一段时间,便可再生。
②当洗涤用水硬度较大时,洗衣粉与肥皂相比,___________洗涤效果较好,原因是______________。
(3)最近我国某地苯胺大量泄漏于生活饮用水的河道中,当地采取的应急措施之一是向河水中撒入大量的活性炭,活性炭的作用是___________________。
(4)若生活污水中含大量氮化合物,通常用生物膜脱氮工艺进行处理。首先在消化细菌作用下将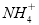 氧化为
氧化为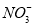 :_____
:_____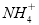 +______O2=______
+______O2=______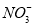 +_____H++______H2O。然后加入甲醇与
+_____H++______H2O。然后加入甲醇与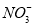 生成N2:______
生成N2:______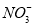 +______CH3OH=_______N2+______CO2+_________H2O+_______OH-(试配平以上两个离子方程式)。
+______CH3OH=_______N2+______CO2+_________H2O+_______OH-(试配平以上两个离子方程式)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省枣庄市高三下学期开学初检测试卷理综化学试卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式是
A.硫酸铝溶液中加入过量氨水 Al3++3OH-= Al(OH)3↓
B.碳酸钠溶液中加入澄清石灰水 Ca(OH)2+CO32-= CaCO3↓+2OH-
C.冷的氢氧化钠溶液中通入氯气 Cl2+2OH-= ClO-+Cl-+H2O
D.稀硫酸中加入铁粉 2Fe+6H+= 2Fe3++3H2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三第一次模拟考试理科综合化学试卷(解析版) 题型:选择题
有关下列图像的说法正确的是

A.图①可以表示,某化学平衡体系改变温度后反应速率随时间的变化
B.根据图②判断,物质A反应生成物质C的△H>O
C.图③表示向一定量的硫酸溶液中滴加一定浓度氢氧化钠溶液时的pH变化
D.图④中开关K置丁A或B处均可减缓铁的腐蚀
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省宁波市高三上学期期末考试化学试卷(解析版) 题型:填空题
(10分)将E 和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)  2G(g)。
2G(g)。
若忽略固体体积,平衡时 G 的体积分数随温度和压强的变化如下表所示。请填写下列空格:
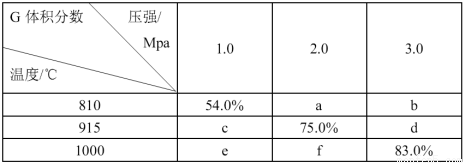
(1)表中数据b f。(选填“>”、“<”或“=”)
(2)该反应的熵变ΔS 0,ΔH 0。(选填“>”、“<”或“=”)
(3)根据表中数据,可计算求得915℃、2.0MPa时E 的转化率为 。
(4)上述反应达到平衡后,若保持体系温度不变,下列措施中能提高混合体系中气体E的体积分数的是
A.保持容器容积不变,充入一定量的气体 E
B.保持容器内压强不变,充入一定量的气体 G
C.加入少量固体F的粉末
D.保持容器容积不变,同时充入一定量的气体 E 和G
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省宁波市高三上学期期末考试化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.Na2CO3溶液中加入少量BaCl2晶体,CO32-水解程度减小,溶液的 pH 也减小
B.SO2能与HClO 反应生成H2SO4,则可以说明HClO 酸性比H2SO4强
C.向装有 Fe(NO3)2溶液的试管中加入稀 H2SO4,在试管口观察到红棕色气体,是因为HNO3分解产生了NO2
D.反应NH3(g)+HCl(g)=NH4C1(s)在室温下可自发进行,则该反应的△H<0
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省宁波市高三上学期期末考试化学试卷(解析版) 题型:选择题
已知某温度下纯水中的 ,对此下列说法正确的是
,对此下列说法正确的是
A.据此无法求算水中c(OH-)
B.该温度低于25℃
C.此温度下水的离子积为常温下的两倍
D.若向水中加入少量盐酸,则水的电离度减小
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省烟台市高三下学期一模诊断测试理科综合化学试卷(解析版) 题型:选择题
一定温度压强下,在容积可变的密闭容器中发生反应CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0,则下列说法不正确的是
CO2(g)+H2(g) ΔH<0,则下列说法不正确的是
A.其他条件不变,加催化剂与不加催化剂其ΔH 相同
B.当达到平衡,向体系中充入CO2其平衡向左移动
C.理论上该反应可设计成燃料电池,H2O(g)在正极上发生还原反应
D.平衡混合气体通入NaOH溶液恰好反应,升高温度溶液碱性增强,其pH一定增大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省江门市高三3月模拟考试理科综合化学试卷(解析版) 题型:简答题
(16分)某煤渣主要含有Al2O3、SiO2,可制备碱式硫酸铝[Al2(SO4)3·2Al(OH)3]溶液,用于烟气脱硫,减少SO2的排放,其制备流程:

已知:25℃,Ksp(CaCO3)=2.8×10-9 , Ksp(CaSO4)=9.1×10-6。
(1)操作①的名称 。
(2)酸浸时反应的离子方程式为 ;为了提高酸浸时铝元素的浸出率,可采取的措施____________________,___________________(写2条)。
(3)固体2的化学式是 ,试分析固体2生成的主要原因(用离子方程式结合文字简要说明) 。
(4)碱式硫酸铝溶液吸收SO2生成Al2(SO4)3·Al2(SO3)3,再向该溶液通入足量空气,生成一种硫酸盐,用于制备碱式硫酸铝溶液的循环使用,试写出有关反应的化学方程式: , 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com