
【题目】如图为一原电池的结构示意图,下列说法中,错误的是( ) 
A.Cu电极为正电极
B.原电池工作时,电子从Zn电极流出
C.原电池工作时的总反应为:Zn+Cu2+=Zn2++Cu
D.盐桥(琼脂﹣饱和KCl溶液)中的K+移向ZnSO4溶液
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】根据要求回答下列问题:
(1)已知恒温、恒容条件下发生反应:2NO2(g)+2C(s) ![]() N2(g)+2CO2(g)。
N2(g)+2CO2(g)。
①下列图像说明该反应进行到t1时刻未达平衡状态的是________(填选项字母)。
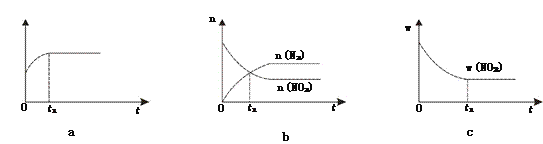
②1 molNO2和足量C发生反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示。

图中A、B、C三点NO2的转化率最高的是_____,该反应的平衡常数Kp=_______(Kp是用平衡分压代替平衡浓度的常数,分压=总压×物质的量分数)。
(2)已知:弱电解质的电离平衡常数为
物质 | H2CO | H2S | HNO2 |
电离平衡常数 (25℃) | Ka1=4.2×10-7 Ka2=5.61×10-11 | Ka1=1.3×10-7 Ka2=7.1×10-15 | Ka=5.1×10-4 |
①含有1L 2mol·L-1碳酸钠的溶液中加入1L 1mol·L-1的HNO2后,则溶液中CO32-、HCO3-和NO2-的离子浓度由大到小是_______。
②25℃时,在0.10 mol·L-1H2S溶液中,通人HCl气体或加入NaOH固体,溶液pH与c(S2-)关系如图所示(忽略溶液体积的变化、H2S的挥发)。pH=13时,溶液中的c(H2S)+c(HS-)=____mol·L-1;
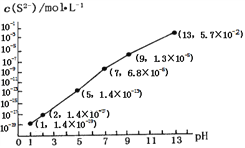
③向10.00mL0.10 mol·L-1的氢硫酸中滴加10.00mL0.1 mol·L-1NaOH溶液,溶液呈_____性,其定量依据是______________________ .
(3)已知:①CaSO4(s)+CO(g)![]() CaO(s)+SO2(g)+CO2(g)△H = +210.5kJmol-1
CaO(s)+SO2(g)+CO2(g)△H = +210.5kJmol-1
②CaSO4(s)+4CO(g)![]() CaS(s)+4CO2(g) △H= -189.2kJmol-1
CaS(s)+4CO2(g) △H= -189.2kJmol-1
则:CaO(s)+3CO(g)+SO2(g) ![]() CaS(s)+3CO2(g) △H=_______kJmol-1.
CaS(s)+3CO2(g) △H=_______kJmol-1.
【答案】 b A 2MPa c(HCO3- )>c(NO2- )>c(CO32-) 0.043或4.3×10-2 碱性 此时恰好生成NaHS溶液,Ka(HS-)=7.1×10-15<Kh(HS-)=KW/ Ka1(H2S)=10-14/(1.3×10-7)=7.7×10-8,即水解程度远大于电离程度,所以呈碱性 -399.7
【解析】(1)①根据“变量不变达平衡”判断,a、反应中碳是固体,恒容条件下的混合物的密度是变量,t1时刻密度不变说明反应已达平衡状态;b、t1时刻是n(N2)=n(NO2),是反应物量的特殊比例,且后面量的变化可看到各反应物的量还没恒定,还没达到平衡状态;c、t1时刻二氧化氮的质量分数不变,则反应物各物质的质量分数也应不变,反应达到平衡状态;答案选b;②A、B、C三点中达到平衡状态后A点NO2浓度最小,所以NO2的转化率最高;③由焦炭还原NO2的反应为:2NO2(g)+2C(s) ![]() N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生反应在C点时,NO2和CO2的物质的量浓度相等,可知此时反应体系中n(NO2)=0.5mol,n(N2)=0.25mol,n(CO2)=0.5mol,则三种物质的分压分别为:P(NO2)= P(CO2)=10MPa×
N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生反应在C点时,NO2和CO2的物质的量浓度相等,可知此时反应体系中n(NO2)=0.5mol,n(N2)=0.25mol,n(CO2)=0.5mol,则三种物质的分压分别为:P(NO2)= P(CO2)=10MPa×![]() =4MPa,P(N2)=2MPa,C点时该反应的压强平衡常数Kp(C)=
=4MPa,P(N2)=2MPa,C点时该反应的压强平衡常数Kp(C)= 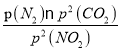 =
=![]() =2MPa;(2)①由亚硝酸的电离平衡常数Ka=5.1×10-4,H2CO的Ka1=4.2×10-7、Ka2=5.61×10-11可判断亚硝酸的酸性强于碳酸,因此向含有2mol碳酸钠的溶液中加入1mol的HNO2后生成1mol碳酸氢钠、1mol亚硝酸钠,另外还剩余1mol碳酸钠,水解程度大小顺序为CO32->NO2-,水解生成HCO3-,所以溶液中CO32-、HCO3-和NO2-离子的浓度大小关系为c(HCO3- )>c(NO2- )>c(CO32-);②根据物料守恒有c(H2S)+c(HS-)+c(S2-)=0.10 mol·L-1,而由图可知pH=13时,c(S2-)=5.7×10-2 mol·L-1,c(H2S)+c(HS-)=0.10 mol·L-1-c(S2-)=0.10 mol·L-1-5.7×10-2 mol·L-1= 4.3×10-2 mol·L-1;③向10.00mL0.10 mol·L-1的氢硫酸中滴加10.00mL0.1 mol·L-1NaOH溶液,溶液呈碱性,其定量依据是此时恰好生成NaHS溶液,Ka(HS-)=7.1×10-15<Kh(HS-)=KW/ Ka1(H2S)=10-14/(1.3×10-7)=7.7×10-8,即水解程度远大于电离程度,所以呈碱性;(3)已知:①CaSO4(s)+CO(g)
=2MPa;(2)①由亚硝酸的电离平衡常数Ka=5.1×10-4,H2CO的Ka1=4.2×10-7、Ka2=5.61×10-11可判断亚硝酸的酸性强于碳酸,因此向含有2mol碳酸钠的溶液中加入1mol的HNO2后生成1mol碳酸氢钠、1mol亚硝酸钠,另外还剩余1mol碳酸钠,水解程度大小顺序为CO32->NO2-,水解生成HCO3-,所以溶液中CO32-、HCO3-和NO2-离子的浓度大小关系为c(HCO3- )>c(NO2- )>c(CO32-);②根据物料守恒有c(H2S)+c(HS-)+c(S2-)=0.10 mol·L-1,而由图可知pH=13时,c(S2-)=5.7×10-2 mol·L-1,c(H2S)+c(HS-)=0.10 mol·L-1-c(S2-)=0.10 mol·L-1-5.7×10-2 mol·L-1= 4.3×10-2 mol·L-1;③向10.00mL0.10 mol·L-1的氢硫酸中滴加10.00mL0.1 mol·L-1NaOH溶液,溶液呈碱性,其定量依据是此时恰好生成NaHS溶液,Ka(HS-)=7.1×10-15<Kh(HS-)=KW/ Ka1(H2S)=10-14/(1.3×10-7)=7.7×10-8,即水解程度远大于电离程度,所以呈碱性;(3)已知:①CaSO4(s)+CO(g)![]() CaO(s)+SO2(g)+CO2(g)△H1= +210.5kJmol-1
CaO(s)+SO2(g)+CO2(g)△H1= +210.5kJmol-1
②CaSO4(s)+4CO(g)![]() CaS(s)+4CO2(g) △H2= -189.2kJmol-1
CaS(s)+4CO2(g) △H2= -189.2kJmol-1
根据盖斯定很,由②-①得反应:CaO(s)+3CO(g)+SO2(g) ![]() CaS(s)+3CO2(g) △H=△H2-△H1= -189.2kJmol-1-210.5kJmol-1=-399.7kJmol-1。
CaS(s)+3CO2(g) △H=△H2-△H1= -189.2kJmol-1-210.5kJmol-1=-399.7kJmol-1。
点睛:本题主要是考查了弱电解质的电离、弱电解质的水解以及反应热计算等。该题考查的知识点较多,侧重考查学生对知识的迁移应用,注意信息的理解和综合应用。难点是电离平衡常数以及盐类水解的应用。解答时要明确电离平衡常数与化学平衡常数一样,平衡常数越大弱电解质的电离程度越大,从而可以判断相应酸碱的相对强弱,进而可以判断相应的盐的水解程度大小。(2)②中的计算要注意灵活应用物料守恒,同时要注意结合图像进行分析与计算。
【题型】综合题
【结束】
9
【题目】三氯化硼是重要的化工原料。可用于制取乙硼烷(B2H6),也可作有机合成的催化剂。
【查阅资料】①BCl3的沸点为12.5℃,熔点为-107.3℃;
②2B+6HCl![]() BCl3+3H2 ,硼也能与强碱反应。
BCl3+3H2 ,硼也能与强碱反应。
某研究性学习小组用如下所示装置制备三氯化硼。回答下列问题:
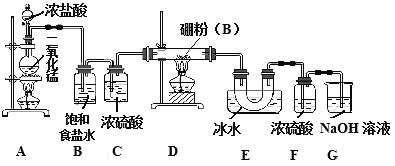
(1)A装置中反应的离子方程式_______________________。
(2)B装置的作用是____________;如果拆去B装置,可能的后果是__________________。
(3)D装置中发生反应的化学方程式_____________。
(4)G装置的作用是_____;为使实验装置简便,可用一个装置代替F和G装置。该装置所用仪器是___,所装试剂是____。
(5)A、D两处加热的先后顺序是_____________,其理由是_______________。
(6)检验制得的产品中是含有硼粉的实验操作是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法正确的是( ) 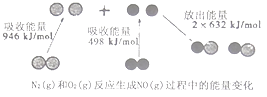
A.1molN2(g)和1molO2(g)反应放出的能量为180kJ
B.1molN2(g)和1molO2(g)具有的总能量小于2molNO(g)具有的总能量
C.通常情况下,N2(g)和O2混合能直接生成NO
D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在生产和生活中,人们广泛利用着化学反应释放的能量.下列说法正确的是( )
A.有能量变化的都是化学变化
B.物质发生化学变化并不一定都伴随着能量变化
C.用实验方法和理论方法研究反应热的化学称为热化学
D.任何反应中的能量变化都表现为热量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.热的浓HNO3能使蓝色石蕊试纸先变红后褪色
B.用HNO3和Na2S反应可以制得H2S气体
C.浓硫酸使蔗糖炭化,体现浓硫酸的的吸水性
D.热的浓硫酸可以用铁制器皿贮存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碲(Te)为第VIA元素,其单质凭借优良的性能成为制作合金添加剂、半导体、光电元件的主体材料,并被广泛应用于冶金、航空航天、电子等领域。可从精炼铜的阳极泥(主要成分为Cu2Te)中回收碲,工艺流程如下 :
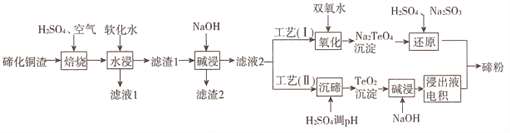
(1)“焙烧”后,碲主要以TeO2 形式存在,写出相应反应的化学方程式:_____________。
(2)为了选择最佳的焙烧工艺,进行了温度和硫酸加入量的条件试验,结果如下表所示:
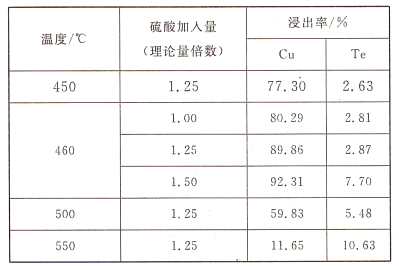
则实验中应选择的条件为_______________,原因为_______________。
(3)工艺( I)中,“还原”时发生的总的化学方程式为_______________。
(4)由于工艺(I)中“氧化”对溶液和物料条件要求高,有研究者采用工艺(II)获得碲。则“电积”过程中,阴极的电极反应式为_______________。
(5)工业生产中,滤渣2经硫酸酸浸后得滤液3和滤渣3。
①滤液3 与滤液1合并,进入铜电积系统。该处理措施的优点为________________。
②滤渣3中若含Au和Ag,可用__________将二者分离。(填字母)
A.王水 B.稀硝酸 C.浓氢氧化钠溶液 D.浓盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列水解反应离子方程式书写正确的是( )
A.CH3COOH+OH﹣CH3COO﹣+H2O
B.S2﹣+2H2OH2S+2OH﹣
C.CH3COOH+H2OCH3COO﹣+H3O+
D.CO32﹣+H2OHCO3﹣+OH﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 分散质微粒直径的大小关系:溶液>胶体>浊液
B. 利用丁达尔效应可以区别溶液与胶体
C. 胶体粒子比较小,可以通过半透膜
D. 电泳现象可证明胶体属于电解质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,单质A、B、C分别为固体、黄绿色气体与无色气体,在合适条件下,它们可以按下面的流程进行反应.又知E溶液是无色的.请回答: 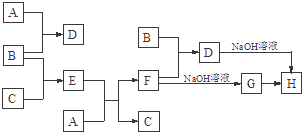
(1)写出E物质的化学式 .
(2)写出G→H的化学方程式 .
(3)写出B+F→D的离子方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com