
【题目】按要求书写下列化学方程式:
(1)丙烯的加聚________________________________________;
(2)1,3﹣丁二烯与等物质的量的单质溴在60℃时发生1,4﹣加成_________________________;
(3)1,2﹣二溴乙烷与氢氧化钠水溶液共热________________;
(4)乙醛的还原______________________________________________;
【答案】n CH2=CHCH3![]()
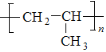
![]() +Br2
+Br2![]()
![]() CH2BrCH2Br+2NaOH
CH2BrCH2Br+2NaOH![]() CH2OHCH2OH+2NaBr CH3CHO+H2
CH2OHCH2OH+2NaBr CH3CHO+H2![]() CH3CH2OH
CH3CH2OH
【解析】
(1)丙烯分子中含有碳碳双键,可以发生加聚反应,反应方程式为:n CH2=CHCH3![]()
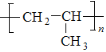 ,答案为:n CH2=CHCH3
,答案为:n CH2=CHCH3![]()
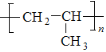 ;
;
(2)1,3﹣丁二烯分子内含有两个双键,当它与1分子溴发生加成时,有两种产物。1,4-加成是在1,4位碳碳双键上发生加成反应,反应方程式为:![]() +Br2
+Br2![]()
![]() ;答案为:
;答案为:![]() +Br2
+Br2![]()
![]() ;
;
(3)卤代烃在氢氧化钠水溶液加热条件下发生水解反应生成醇,故反应方程式为:CH2BrCH2Br+2NaOH![]() CH2OHCH2OH+2NaBr+2H2O。答案为:CH2BrCH2Br+2NaOH
CH2OHCH2OH+2NaBr+2H2O。答案为:CH2BrCH2Br+2NaOH![]() CH2OHCH2OH+2NaBr。
CH2OHCH2OH+2NaBr。
(4)乙醛的催化加氢反应也是还原反应,该反应为:CH3CHO+H2![]() CH3CH2OH。答案为:CH3CHO+H2
CH3CH2OH。答案为:CH3CHO+H2![]() CH3CH2OH。
CH3CH2OH。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】已知A为淡黄色固体,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀。
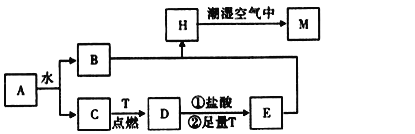
(1)物质A的化学式为___。
(2)H在潮湿空气中变成M的实验现象是__,化学方程式为___。
(3)A和水反应生成B和C的离子方程式为__,列出A的一种重要用途__。
(4)反应①的离子方程式为__,②加足量T的目的___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某小组运用工业上离子交换膜法制烧碱的原理,用如图所示装置电解K2SO4溶液。
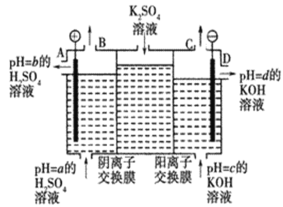
(1)该电解槽的阳极反应式为__________________________________,通过阴离子交换膜的离子数___________(填“>”“<”或“=”)通过阳离子交换膜的离子数
(2)图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为___________
(3)电解一段时间后,B口与C口产生气体的质量比为___________
Ⅱ.常温下用惰性电极电解200mLNaCl、CuSO4的混合溶液,所得气体的体积随时间变化如图所示,根据图中信息回答下列问题。(气体体积已换算成标准状况下的体积,且忽略气体在水中的溶解和溶液体积的变化)
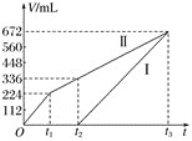
(1)曲线___________(填“Ⅰ”或“Ⅱ”)表示阳极产生气体的变化
(2)CuSO4的物质的量浓度为___________mol/L
(3)t1时所得溶液恢复到原来状态需加___________(物质名称)质量___________g
(4)t2时所得溶液的pH为___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列几组物质,请将序号填入下列空格内:
A、CH2=CH﹣COOH和油酸( C17H33COOH)
B、12C60和石墨
C.![]() 和
和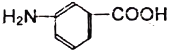
D.35Cl和37Cl
E.乙醇和乙二醇
(1)互为同位素的是_____。
(2)互为同系物的是_____。
(3)互为同素异形体的是:_____。
(4)互为同分异构体的是_____。
(5)既不是同系物,又不是同分异体,也不是同素异形体,但可看成是同一类物质的是_____
(6)写出乙醇的催化氧化方程式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是可逆反应A+2B![]() 2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况。由此可推断
2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况。由此可推断
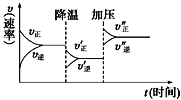
A.正反应是放热反应B.D可能是气体
C.逆反应是放热反应D.A、B、C、D均为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中物质的量浓度为1 mol/L的是( )
A.将40 g NaOH固体溶解于1 L水中
B.将22.4 L氯化氢气体溶于水配成1 L溶液
C.将1 L 10 mol/L的浓盐酸与9 L水混合
D.10 g NaOH固体溶解在水中配成250 mL溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)53克Na2CO3的物质的量是________,所含Na+和CO32-的物质的量各是_____________,
(2)在标准状况下,测得1.32 g某气体的体积为0.672 L。则此气体的摩尔质量_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个实验室制取氯气并以氯气为原料进行特定反应的装置:
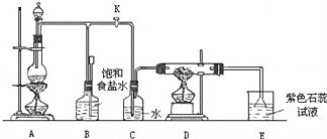
(1)A是氯气发生装置,其中反应的化学方程式为_____。
(2)实验开始时,先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处酒精灯,连接上E装置。Cl2通过C瓶后再进入D。D装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为CO2和HCl。试写出D中反应的化学方程式:_____。装置C的作用是_____。
(3)在E处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是_____。
(4)若将E处烧杯中溶液改为澄清石灰水,反应过程现象为_____(选填标号)。
A.有白色沉淀生成 B.无现象 C.先生成白色沉淀,而后白色沉淀消失
(5)D处反应完毕后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有Cl2产生,此时B中的现象是_____,B的作用是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下:
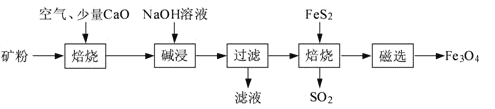
(1)粉碎高硫铝土矿石的目的是______。
(2)焙烧时发生氧化还原反应:______FeS2+______O2![]() ______Fe2O3+______SO2↑,配平该方程式。
______Fe2O3+______SO2↑,配平该方程式。
(3)碱浸时发生反应的化学方程式为______。
(4)过滤后向滤液中通入过量的CO2气体,反应的离子方程式为______。
(5)“过滤”得到的滤渣中含有大量的Fe2O3。Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(FeS2):n(Fe2O3)=______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com