
【题目】下列溶液中物质的量浓度为1 mol/L的是( )
A.将40 g NaOH固体溶解于1 L水中
B.将22.4 L氯化氢气体溶于水配成1 L溶液
C.将1 L 10 mol/L的浓盐酸与9 L水混合
D.10 g NaOH固体溶解在水中配成250 mL溶液
科目:高中化学 来源: 题型:
【题目】赤铜矿的成分是 Cu2O,辉铜矿的成分是 Cu2S,将赤铜矿与辉铜矿混合加热有以下反应:Cu2S + 2Cu2O![]() 6Cu + SO2↑,对于该反应的下列说法正确的是( )
6Cu + SO2↑,对于该反应的下列说法正确的是( )
A.该反应中的氧化剂只有 Cu2O
B.Cu2S 在反应中既是氧化剂又是还原剂
C.Cu 既是氧化产物又是还原产物
D.氧化产物与还原产物的物质的量之比为 6∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室在 500℃时,隔绝空气加热硫酸亚铁铵[(NH4)2Fe(SO4)2]至分解完全并确定分解产物成分的装置如图所示 (已知分解的固体产物可能有 FeO、Fe2O3 和 Fe3O4,气体产物可能有 NH3、N2、H2O、SO3 和 SO2)。下列说法正 确的是( )

A. 取①中固体残留物与稀硫酸反应并滴加 KSCN,溶液变红,则残留物一定为 Fe2O3
B. 装置②用于检验分解产物中是否有水蒸气生成,试剂 X 最好选用碱石灰
C. 装置③用于检验分解产物中是否有 SO3 气体生成并除去 SO3 和 NH3
D. 装置④用于检验分解产物中是否有 SO2 气体生成,装置⑤用于收集生成的 NH3 和 N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,取浓度相同的NaOH和HCl溶液,以3∶2体积比相混合,所得溶液的pH等于12,则原溶液的浓度为
A.0.01mol·L-1B.0.017mol·L-1
C.0.05mol·L-1D.0.50mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求书写下列化学方程式:
(1)丙烯的加聚________________________________________;
(2)1,3﹣丁二烯与等物质的量的单质溴在60℃时发生1,4﹣加成_________________________;
(3)1,2﹣二溴乙烷与氢氧化钠水溶液共热________________;
(4)乙醛的还原______________________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵是分析化学中重要的试剂,某实验小组制备和探究其分解产物的实验如下:I.制备硫酸亚铁铵
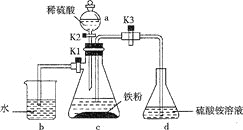
(1)仪器a的名称是__。
(2)将过量铁粉置于c中,加蒸馏水于b中,硫酸铵溶液于d中,按图连接好装置,打开K1、K2,关闭K3.使用铁粉“过量”的原因是___。
(3)关闭K1和K2,打开K3,c中浅绿色溶液流入d,其原因是___;d中析出沉淀,用化学方程式解释:___。
Ⅱ.探究硫酸亚铁铵的部分分解产物
假设气体产物仅有NH3、SO2、SO3(g)和H2O(g),设计如下所需装置进行实验;
已知:CaCl2+8NH3=CaCl2·8NH3
A.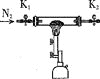 B.
B. C.
C.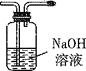 D.
D.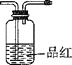 E.
E.![]()
①将I中制备的沉淀装入A,装置连接顺序为___,打开K1和K2,缓缓通入N2,一段时间后,关闭K1开始加热,实验后反应管中残留固体为红色粉末;
②B、D中有气泡冒出,还可观察到的现象分别为__,
③硫酸亚铁铵的分解方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一密闭容器中,反应mA(g)+nB(g) ![]() pC(g)达到平衡时,测得c(A)为0.5 mol·L-1;在温度不变的条件下,将容器体积扩大一倍,当达到平衡时,测得c(A)为0.3 mol·L-1。则下列判断正确的是
pC(g)达到平衡时,测得c(A)为0.5 mol·L-1;在温度不变的条件下,将容器体积扩大一倍,当达到平衡时,测得c(A)为0.3 mol·L-1。则下列判断正确的是
A. 化学计量数:m+n>p B. 平衡向正反应方向移动了
C. 物质B的转化率增大了 D. 物质C的质量分数增加了
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,下列叙述不是可逆反应A(g)+3B(g) ![]() 2C(g)达到平衡的标志的是( )
2C(g)达到平衡的标志的是( )
①C的生成速率与C的分解速率相等; ②单位时间内amol A生成,同时生成3amol B;③A、B、C的浓度不再变化;④混合气体的总压强不再变化;⑤混合气体的物质的量不再变化; ⑥单位时间消耗amol A,同时生成3amol B;⑦A 、B、C的分子数目比为1:3:2。
A.②⑤B.①③C.②⑦D.⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,某同学进行CO2 与Na2O2 反应的探究实验,回答下列问题。
(1)用下图装置制备纯净的CO2

①丙装置的名称是__________,乙、丙装置中盛装的试剂分别是__________、_________。
②若CO2 中混有HCl,则HCl 与Na2O2 反应的化学方程式为_____________。
(2)按照下面的装置图进行实验(夹持装置略)。

①先组装仪器,然后_____________,再用注射器1 抽取100 mL 纯净的CO2,将其连接在K1 处,注射器2 的活塞推到底后连接在K2 处,具支U 形管中装入足量的Na2O2 粉末与玻璃珠。
②打开止水夹K1、K2,向右推动注射器1 的活塞,可观察到的现象是_________。
③实验过程中,需缓慢推入CO2,其目的是_____________,为达到相同目的,还可进行的操作是_____________。
(3)实验结束后,当注射器1 的活塞推到底时,测得注射器2 中气体体积为65 mL,则CO2的转化率是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com