
【题目】CO和![]() 的某些性质及相关键能如下表所示,下列说法不正确的是
的某些性质及相关键能如下表所示,下列说法不正确的是
表一
分子 | 熔点 | 沸点 | 常温时在水中的溶解度 |
CO |
|
|
|
|
|
|
|
表二
碳氮键 |
|
|
|
键能 |
|
|
|
氮氮键 |
|
|
|
键键能 | 193 | 418 | 946 |
A.CO与![]() 的价电子总数相等
的价电子总数相等
B.由表2可知,CO的活泼性不及![]() ,因为
,因为![]() 的键能大于
的键能大于![]()
C.由表1可知,CO的熔沸点高于![]() ,因为CO分子间作用力大于
,因为CO分子间作用力大于![]()
D.由表1可知,室温时CO在水中的溶解度大于![]() ,因为CO是极性分子
,因为CO是极性分子
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素原子半径与原子序数的关系图。下列说法正确的是
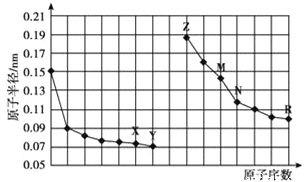
A.![]() 一定不与酸反应
一定不与酸反应
B.![]() 与水反应时,水是还原剂
与水反应时,水是还原剂
C.简单离子的半径:![]()
D.最高价氧化物对应水化物的碱性:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
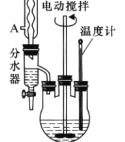
【题目】苯甲酸乙酯可由苯甲酸与乙醇在浓硫酸共热下反应制得,反应装置如图(部分装置省 略),反应原理如下:
 +C2H5OH
+C2H5OH +H2O
+H2O
实验操作步骤:
向三颈烧瓶内加入12.2g 苯甲酸、25mL乙醇、20mL 苯及4mL浓硫酸,摇匀,加入沸石。
①装上分水器、电动搅拌器和温度计,加热至分水器下层液体接近支管时将下层液体放入量筒 中,继续蒸馏,蒸出过量的乙醇,至瓶内有白烟(约3h),停止加热。
②将反应液倒入盛有80mL冷水的烧瓶中,在搅拌下分批加入碳酸钠粉末溶液至溶液无二氧化 碳逸出,用 pH 试纸检验至中性。
③用分液漏斗分出有机层,水层用25mL乙醚萃取,然后合并至有机层,用无水CaCl2干燥,粗产物进行蒸馏,低温蒸出乙醚。当温度超过140℃时,直接接受210-213℃的馏分,最终通过蒸馏得到纯净苯甲酸乙酯12.8mL。
可能用到的有关数据如下:
相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
苯甲酸 | 122 | 1.27 | 249 | 微溶于水,易溶于乙醇、乙醚 |
苯甲酸乙酯 | 150 | 1.05 | 211-213 | 微溶于热水,易溶于乙醇、乙醚 |
乙醇 | 46 | 0.79 | 78.5 | 易溶于水 |
乙醚 | 74 | 0.73 | 34.5 | 微溶于水 |
(1)反应装置中分水器上方的仪器名称是_______,其作用是______。
(2)步骤①中加入浓硫酸的作用是______,步骤②中电动搅拌棒的作用是_______。
(3)步骤②中使用分水器除水的目的是______。
(4)步骤③中加入碳酸钠的目的是______。
(5)有机层从分液漏斗的_______(选填“上口倒出”或“下口放出”span>)
(6)本实验所得到的苯甲酸乙酯的产率是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A和B,只由C、H、O两种或三种元素组成,相同物质的量的A和B完全燃烧时,消耗氧气的物质的量相等,下列对A、B的判断错误的是
A.A与B互为同分异构体B.A与B的分子组成相差n个“H2O”
C.A与B的分子组成相差n个“CO2”D.A与B可能是同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅烷是一种无色、与空气反应并会引起窒息的气体.其分子结构和![]() 相似,但
相似,但![]() 键键能比
键键能比![]() 键键能低。下列判断错误的是
键键能低。下列判断错误的是
A.![]() 分子呈正四面体形
分子呈正四面体形
B.![]() 分子是非极性分子
分子是非极性分子
C.因为![]() 键键能比
键键能比![]() 键键能低,所以
键键能低,所以![]() 沸点低于
沸点低于![]() 沸点
沸点
D.![]() 分子稳定性低于
分子稳定性低于![]() 分子,因为
分子,因为![]() 键键能高
键键能高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示的实验,能达到实验目的的是
A | B | C | D |
|
|
|
|
验证化学能转化为电能 | 研究催化剂对化学反应速率的影响 | 实验室制氨气 | 验证非金属性:Cl>C>Si |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+m Y(g)![]() 3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
A. m=2
B. 两次平衡的平衡常数相同
C. X与Y的平衡转化率之比为1:1
D. 第二次平衡时,Z的浓度为0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度下重水(D2O)的离子积常数为1.6×10-15,若用定义pH一样的方法来规定pD=-lg{c(D+)},则该温度下,下列叙述正确的是
A.纯净的重水(D2O)中,pD=7
B.溶解有NaCl的重水溶液,其pD=7
C.纯净的重水中(D2O),c(D+)=c(OD-)
D.1 L溶解有0.01 mol NaOD的重水溶液,其pD=12.0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向20 mL0.1 mol/L H2A溶液中逐滴加入0.1 mol/L NaOH溶液,H2A溶液中各粒子浓度分数δ(X)随溶液pH变化的关系如图所示。下列说法错误的是 ( )

A.当溶液中A元素的主要存在形态为A2-时,溶液可能为弱酸性、中性或碱性
B.当加入NaOH溶液至20 mL时,溶液中存在((Na+)=2c(A2-)+c(HA-)
C.室温下,反应A2-+H2A=2HA-的平衡常数的对数值lgK=3
D.室温下,弱酸H2A的第一级电离平衡常数用Ka1表示,Na2A的第二级水解平衡常数用Kh2表示,则Kal>Kh2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com