
氨和肼(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用。
(1)N2H4中的N原子可达到8电子的稳定结构,画出N2H4的结构式_____________。
(2)实验室用两种固体制取NH3 的反应方程式为______________________________。
(3)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 。
(4)肼——空气燃料电池是一种碱性电池,该电池放电时,负极的反应式 。
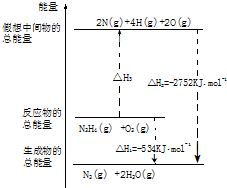
(5)肼是一种高能燃料,有关化学反应的能量变化如图所示,已知断裂1mol化学键所需的能量(kJ):N≡N为942,O=O为500,N-N为154,则断裂1molN-H键所需的能量是 kJ。

(1) (2)2NH4Cl+Ca(OH)2
(2)2NH4Cl+Ca(OH)2 2NH3↑+2H2O+CaCl2 (3) 2NH3+NaClO=N2
H4+NaCl+H2O
(4)N2H4-4e—+4OH—=N2+4H2O (5)391
2NH3↑+2H2O+CaCl2 (3) 2NH3+NaClO=N2
H4+NaCl+H2O
(4)N2H4-4e—+4OH—=N2+4H2O (5)391
【解析】
试题分析:(1)N2H4中的N原子可达到8电子的稳定结构,不难画出N2H4的结构式 。(2)实验室用两种固体制取NH3 的反应方程式为2NH4Cl+Ca(OH)2
。(2)实验室用两种固体制取NH3 的反应方程式为2NH4Cl+Ca(OH)2 2NH3↑+2H2O+CaCl2。(3)根据反应物和生成物,不难写出NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 2NH3+NaClO=N2
H4+NaCl+H2O。(4)作为燃料电池时,负极发生氧化反应,电解质溶液是20%-30%的KOH溶液,N2H4失去电子被氧化生成N2,故答案为:N2H4+4OH--4e-=N2+4H2O;(5)根据图中内容,可以看出N2H4(g)+O2(g)=2N(g)+4H(g)+2O(g),△H3=2752kJ/mol-534kJ/mol=2218kJ/mol,设断裂1molN-H键所需的能量为K,即154+4K+500=2218,解得K=391。
2NH3↑+2H2O+CaCl2。(3)根据反应物和生成物,不难写出NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 2NH3+NaClO=N2
H4+NaCl+H2O。(4)作为燃料电池时,负极发生氧化反应,电解质溶液是20%-30%的KOH溶液,N2H4失去电子被氧化生成N2,故答案为:N2H4+4OH--4e-=N2+4H2O;(5)根据图中内容,可以看出N2H4(g)+O2(g)=2N(g)+4H(g)+2O(g),△H3=2752kJ/mol-534kJ/mol=2218kJ/mol,设断裂1molN-H键所需的能量为K,即154+4K+500=2218,解得K=391。
考点:考查燃料电池正负极书写、热化学方程式书写。


科目:高中化学 来源: 题型:阅读理解
 (2013?江苏三模)氨和肼(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用.
(2013?江苏三模)氨和肼(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用.查看答案和解析>>
科目:高中化学 来源: 题型:
 氨和肼(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用.
氨和肼(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用.查看答案和解析>>
科目:高中化学 来源:2013-2014学年北京市东城区普通校高三12月联考化学试卷(解析版) 题型:填空题
氨在国民经济中占有重要地位。
(1)NH3的电子式为
(2)实验室中制取氨气的化学方程式为 ,生成的气体可以用蘸有浓盐酸的玻璃棒来检验,将产物溶于水,溶液呈酸性,用离子方程式表示原因 ;
溶液中离子浓度由大到小的顺序为
(3)欲快速制取氨气,可将浓氨水滴入固体氢氧化钠中,其装置如图,请结合化学用语从化学平衡的角度解释:

(4)将SO2气体通入氯化钡溶液,未见有沉淀生成,继续通入NH3,则出现白色沉淀,请写出反应的离子方程式 ;若将SO2气体通入酸化的硝酸钡溶液,也产生白色沉淀,用离子方程式加以说明
(5)氨和肼(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用。
肼——空气燃料电池是一种碱性电池,该电池放电时,负极的反应式 。
(6)氮氧化物的排放会对空气造成污染,利用氧化法除去烟气中的氮氧化物。首先向氮氧化物中补充氧气,然后将混合气体通入石灰乳中,使之转化为硝酸钙。已知某氮氧化物由NO和NO2组成,且n(NO):n(NO2)=1:3.写出氧化吸收法除去氮氧化物的化学方程式___________________
查看答案和解析>>
科目:高中化学 来源:2012-2013学年天津市高三毕业班联考(一)理综化学试卷(解析版) 题型:填空题
氮是地球上含量丰富的一种元素,氨和肼(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用。
Ⅰ.(1)N2H4中的N原子最外层达到8电子稳定结构,写出N2H4的结构式_____________。
(2)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 。
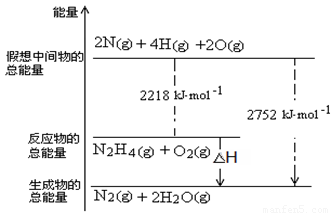
(3)肼是一种高能燃料,有关化学反应的能量变化如右图所示,写出肼燃烧的热化学方程式 。
Ⅱ.氨的合成是最重要的化工生产之一。已知:
N2(g)+3H2(g) 2NH3(g)ΔH=-92.4 kJ·mol-1
2NH3(g)ΔH=-92.4 kJ·mol-1
在3个体积均为2L的密闭容器中,在相同的温度下,使用相同的催化剂合成氨,实验测得反应在起始、达到平衡时的有关数据如下表所示:

试回答:
(1)下列各项能说明该反应已达到平衡状态的是______________(填写序号字母)。
a.容器内N2、H2、NH3的浓度之比为1︰3︰2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
(2)分析上表数据,下列关系正确的是_________(填写序号字母)。
A.2c1>1.5mol·L-1 B.w3=w1 C.2ρ1=ρ2 D.K甲= K乙= K丙
(3)容器乙中反应从开始到达平衡平均速率为v(H2)= _____________。
III.直接供氨式碱性燃料电池的电池反应式是4NH3+3O2=2N2+6H2O,电解质溶液一般使用KOH溶液,则负极电极反应式是__________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com