
| ∑ī”¶–ÚļŇ | ĽĮ—ß∑ī”¶ | ∑ī”¶»» |
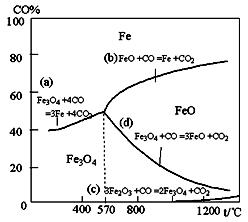
| ĘŔ | Fe2O3(s)£ę3CO(g)=2Fe(s)£ę3CO 2(g) | °ųH1= -26.7kJ°§mol-1 |
| Ęŕ | 3Fe2O3(s)£ęCO(g)=2Fe3O4(s)£ęCO2(g) | °ųH2= -50.8kJ°§mol-1 |
| ĘŘ | Fe3O4(s)£ęCO(g)=3FeO(s)£ęCO2 (g) | °ųH3= -36.5kJ°§mol-1 |
| Ę‹ | FeO(s)£ęCO(g)=Fe(s)£ęCO2(g) | °ųH4 |
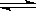 Fe(s)£ęCO2(g)£¨∆Ĺļ‚≥£ żK=0.4°£ĹŮ‘ŕ“Ľ√‹Ī’»›∆ų÷–£¨ľ”»Ž7.2gFeO£¨Õ¨ ĪÕ®»Ž4.48LCO(“—’ŘļŌő™ĪÍ◊ľ◊īŅŲ)£¨Ĺę∆š…żő¬ĶĹ1100°ś£¨≤Ęő¨≥÷ő¬∂»≤ĽĪš£¨īÔ∆Ĺļ‚ Ī£¨FeOĶń◊™ĽĮ¬ ő™£ļ °£
Fe(s)£ęCO2(g)£¨∆Ĺļ‚≥£ żK=0.4°£ĹŮ‘ŕ“Ľ√‹Ī’»›∆ų÷–£¨ľ”»Ž7.2gFeO£¨Õ¨ ĪÕ®»Ž4.48LCO(“—’ŘļŌő™ĪÍ◊ľ◊īŅŲ)£¨Ĺę∆š…żő¬ĶĹ1100°ś£¨≤Ęő¨≥÷ő¬∂»≤ĽĪš£¨īÔ∆Ĺļ‚ Ī£¨FeOĶń◊™ĽĮ¬ ő™£ļ °£
| ńÍľ∂ | łŖ÷–Ņő≥Ő | ńÍľ∂ | ≥ű÷–Ņő≥Ő |
| łŖ“Ľ | łŖ“Ľ√‚∑—Ņő≥ŐÕ∆ľŲ£° | ≥ű“Ľ | ≥ű“Ľ√‚∑—Ņő≥ŐÕ∆ľŲ£° |
| łŖ∂Ģ | łŖ∂Ģ√‚∑—Ņő≥ŐÕ∆ľŲ£° | ≥ű∂Ģ | ≥ű∂Ģ√‚∑—Ņő≥ŐÕ∆ľŲ£° |
| łŖ»ż | łŖ»ż√‚∑—Ņő≥ŐÕ∆ľŲ£° | ≥ű»ż | ≥ű»ż√‚∑—Ņő≥ŐÕ∆ľŲ£° |
Ņ∆ńŅ£ļłŖ÷–ĽĮ—ß ņī‘ī£ļ≤ĽŌÍ Ő‚–Õ£ļĶ•—°Ő‚
| A£ģ∑ņ÷Ļ Į”Õ∂Ő»Ī | B£ģĹĶĶÕ≥…Īĺ |
| C£ģľű…Ŕ∂‘īů∆ÝĶńőŘ»ĺ | D£ģľ”īů∑Ę∂ĮĽķĶń∂ĮѶ |
≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļłŖ÷–ĽĮ—ß ņī‘ī£ļ≤ĽŌÍ Ő‚–Õ£ļĶ•—°Ő‚
| A£ģ√ų∑ĮĺĽňģ”Ž“ļ¬»ĺĽňģĶń‘≠ņŪŌŗÕ¨ |
| B£ģ∂∆≤„∆∆ňūļů£¨∂∆Õ≠ŐķįŚĪ»∂∆–ŅŐķįŚłŁńÕłĮ ī |
| C£ģī”ļ£īÝ÷–ŐŠ»°Ķ‚Ķ•÷ ĶńĻż≥Ő…śľį—űĽĮĽĻ‘≠∑ī”¶ |
| D£ģ°įĪĶ≤Õ°Ī÷– Ļ”√ĶńŃÚňŠĪĶ «»űĶÁĹ‚÷ £¨ŐľňŠń∆Ņ…”√”ŕ÷őŃ∆őłňŠĻż∂ŗ÷Ę |
≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļłŖ÷–ĽĮ—ß ņī‘ī£ļ≤ĽŌÍ Ő‚–Õ£ļ Ķ—ťŐ‚
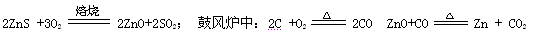

≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļłŖ÷–ĽĮ—ß ņī‘ī£ļ≤ĽŌÍ Ő‚–Õ£ļŐÓŅ’Ő‚
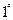 Ķńňģ «÷ł√Ņ…żňģļ¨10
Ķńňģ «÷ł√Ņ…żňģļ¨10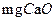 ĽÚ”Ž÷ģŌŗĶĪĶńőÔ÷ £®»Á7.1
ĽÚ”Ž÷ģŌŗĶĪĶńőÔ÷ £®»Á7.1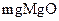 £©°£»Űń≥Őž»Ľňģ÷–
£©°£»Űń≥Őž»Ľňģ÷–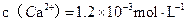 £¨
£¨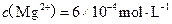 £¨‘ÚīňňģĶń”≤∂»ő™ £Ľ
£¨‘ÚīňňģĶń”≤∂»ő™ £Ľ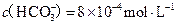 £¨Ō÷“™»ŪĽĮ10
£¨Ō÷“™»ŪĽĮ10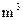 ’‚÷÷Őž»Ľňģ£¨‘Ú–ŤŌ»ľ”»Ž
’‚÷÷Őž»Ľňģ£¨‘Ú–ŤŌ»ľ”»Ž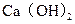
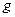 £¨ļůľ”»Ž
£¨ļůľ”»Ž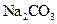
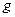 °£
°£≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļłŖ÷–ĽĮ—ß ņī‘ī£ļ≤ĽŌÍ Ő‚–Õ£ļ Ķ—ťŐ‚
 ņŪľŃ£¨őřňģFeCl3Ķń»ŘĶ„ő™555K°Ę∑–Ķ„ő™588K°£Ļ§“Ķ…Ō÷∆ĪłőřňģFeCl3Ķń“Ľ÷÷Ļ§“’»ÁŌ¬£ļ
ņŪľŃ£¨őřňģFeCl3Ķń»ŘĶ„ő™555K°Ę∑–Ķ„ő™588K°£Ļ§“Ķ…Ō÷∆ĪłőřňģFeCl3Ķń“Ľ÷÷Ļ§“’»ÁŌ¬£ļ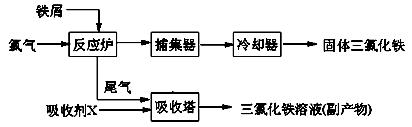
| ő¬∂»/°ś | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
| »‹Ĺ‚∂»(g/100gH20) | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
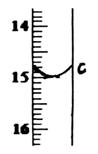
| Ķő∂®īő ż | īż≤‚“ļŐŚĽż(mL) | Ķő∂®«į∂Ń ż(mL) | Ķő∂®ļů∂Ń ż(mL) |
| Ķŕ“Ľīő | 25.00 | 0.00 | c= |
| Ķŕ∂Ģīő | 25.00 | 0.00 | 14.99 |
| Ķ໿īő | 25.00 | 0.00 | 15.01 |
≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļłŖ÷–ĽĮ—ß ņī‘ī£ļ≤ĽŌÍ Ő‚–Õ£ļŐÓŅ’Ő‚
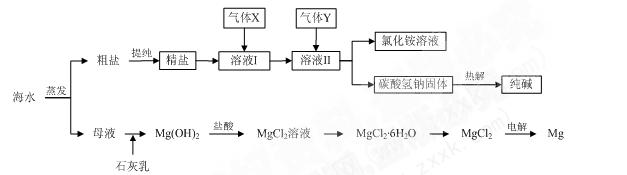
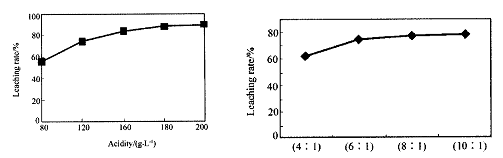
 3»‹“ļ£ĽĘ› °Ý £ĽĘřľ” ŃŅĶń—őňŠ£ĽĘŖ °Ý °£
3»‹“ļ£ĽĘ› °Ý £ĽĘřľ” ŃŅĶń—őňŠ£ĽĘŖ °Ý °£ ļŌ¬»ĽĮ√ĺĺßŐŚ(MgCl2°§6H2O)ňýĶ√ĻŐŐŚ «—űĽĮ√ĺ£¨ ‘–ī≥Ųł√∑ī”¶ĶńĽĮ—ß∑Ĺ≥Ő Ĺ °Ý °£
ļŌ¬»ĽĮ√ĺĺßŐŚ(MgCl2°§6H2O)ňýĶ√ĻŐŐŚ «—űĽĮ√ĺ£¨ ‘–ī≥Ųł√∑ī”¶ĶńĽĮ—ß∑Ĺ≥Ő Ĺ °Ý °£≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļłŖ÷–ĽĮ—ß ņī‘ī£ļ≤ĽŌÍ Ő‚–Õ£ļĶ•—°Ő‚
| A£ģ¬ŃļŌĹū | B£ģłŖő¬ĹŠĻĻĶ™ĽĮĻŤŐ’ī… |
| C£ģ”–Ľķ≤£Ńß | D£ģ◊©ÕŖ |
≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļłŖ÷–ĽĮ—ß ņī‘ī£ļ≤ĽŌÍ Ő‚–Õ£ļĶ•—°Ő‚
| A£ģĘŔĘŘĘ‹ | B£ģĘŕĘ‹Ęř | C£ģĘŕĘ‹Ę› | D£ģĘŘĘ‹Ę› |
≤ťŅīīūįłļÕĹ‚őŲ>>
Ļķľ —ß–£”Ň—° - Ń∑Ōį≤ŠŃ–ĪŪ - ‘Ő‚Ń–ĪŪ
ļĢĪĪ °Ľ•Ń™ÕÝő•∑®ļÕ≤ĽŃľ–ŇŌĘĺŔĪ®∆ĹŐ® | ÕÝ…Ō”–ļ¶–ŇŌĘĺŔĪ®◊®«Ý | ĶÁ–Ň’©∆≠ĺŔĪ®◊®«Ý | …śņķ ∑–ťőř÷ų“Ś”–ļ¶–ŇŌĘĺŔĪ®◊®«Ý | …ś∆ů«÷»®ĺŔĪ®◊®«Ý
ő•∑®ļÕ≤ĽŃľ–ŇŌĘĺŔĪ®ĶÁĽį£ļ027-86699610 ĺŔĪ®” Ōš£ļ58377363@163.com