
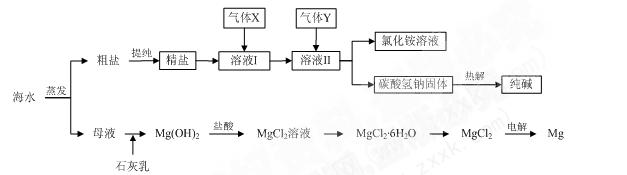
 3溶液;⑤ ▲ ;⑥加适量的盐酸;⑦ ▲ 。
3溶液;⑤ ▲ ;⑥加适量的盐酸;⑦ ▲ 。 合氯化镁晶体(MgCl2·6H2O)所得固体是氧化镁,试写出该反应的化学方程式 ▲ 。
合氯化镁晶体(MgCl2·6H2O)所得固体是氧化镁,试写出该反应的化学方程式 ▲ 。 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:填空题
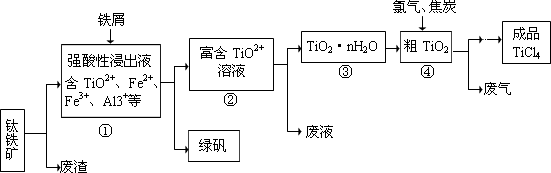
| | TiCl4 | SiCl4 |
| 熔点/℃ | -25.0 | -68.8 |
| 沸点/℃ | 136.4 | 57.6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.人类利用的能源都是通过化学反应获得的 |
| B.绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来 |
| C.物质的化学能可以在不同条件下转为热能、电能为人类所利用 |
| D.化石燃料蕴藏的能量来自远古时期生物体所吸收利用的太阳能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 氢铵和KCl为原料可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸氢铵等物质。合成路线如下:
氢铵和KCl为原料可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸氢铵等物质。合成路线如下: 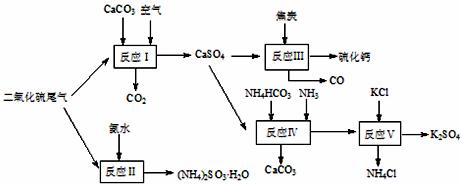
 中加入适量的对苯二酚等物质,其目的是 ▲ 。
中加入适量的对苯二酚等物质,其目的是 ▲ 。| A.反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙 |
B.反应Ⅲ中发生反应的化学方程式为:CaSO4+4C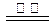 CaS +4CO↑ CaS +4CO↑ |
| C.反应Ⅳ需控制在60~70℃,目的之一是减少碳酸氢铵的分解 |
| D.反应Ⅴ中的副产物氯化铵可用作氮肥 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 可循环利用。请在下图的两个空框中填上循环过程中反应物和生成物的
可循环利用。请在下图的两个空框中填上循环过程中反应物和生成物的 分子式,以完成理想的氢能源循环体系图(循环中接受太阳能的物质在自然界中广泛存在)。从能量转移的角度看,过程Ⅱ主要是 能转化为 能。
分子式,以完成理想的氢能源循环体系图(循环中接受太阳能的物质在自然界中广泛存在)。从能量转移的角度看,过程Ⅱ主要是 能转化为 能。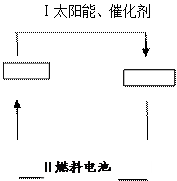
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.复合材料的使用可以使太阳能帆板承受超高温 |
| B.复合材料的使用可以使“神舟”飞船质量变轻 |
| C.复合材料的使用可以使太阳能帆板承受超高强度的改变 |
| D.复合材料的使用可以使太阳能帆板承受温差造成的热胀冷缩的难题 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
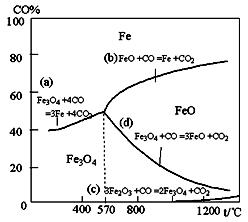
| 反应序号 | 化学反应 | 反应热 |
| ① | Fe2O3(s)+3CO(g)=2Fe(s)+3CO 2(g) | △H1= -26.7kJ·mol-1 |
| ② | 3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) | △H2= -50.8kJ·mol-1 |
| ③ | Fe3O4(s)+CO(g)=3FeO(s)+CO2 (g) | △H3= -36.5kJ·mol-1 |
| ④ | FeO(s)+CO(g)=Fe(s)+CO2(g) | △H4 |
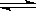 Fe(s)+CO2(g),平衡常数K=0.4。今在一密闭容器中,加入7.2gFeO,同时通入4.48LCO(已折合为标准状况),将其升温到1100℃,并维持温度不变,达平衡时,FeO的转化率为: 。
Fe(s)+CO2(g),平衡常数K=0.4。今在一密闭容器中,加入7.2gFeO,同时通入4.48LCO(已折合为标准状况),将其升温到1100℃,并维持温度不变,达平衡时,FeO的转化率为: 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.蒸馏法是海水淡化的方法之一 |
| B.海洋植物如海带、海藻中含有丰富的碘元素,所以多食海带可治疗和预防甲状腺肿大 |
| C.氯化钠、氯化镁和单质溴等物质不需要化学变化就能够从海水中获得 |
| D.重视和开发潮汐能、波浪能等新型清洁能源,有利于人类的可持续发展 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com