
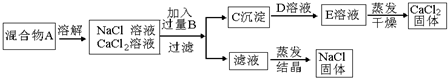
分析 分离NaCl和CaCl2两种固体混合物,溶解后加入过量B为碳酸钠溶液,生成沉淀C为碳酸钙沉淀和氯化钠溶液,碳酸钙和D为盐酸发生反应得到溶液E为氯化钙溶液,经蒸发可得到氯化钙固体;由于碳酸钠过量,所以滤液中的物质有氯化钠和碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠,加入稀盐酸最合适,碳酸钠和稀盐酸生成氯化钠和水和二氧化碳,蒸发后最后的固体物质是氯化钠,据此答题.
解答 解:分离NaCl和CaCl2两种固体混合物,溶解后加入过量B为碳酸钠溶液,生成沉淀C为碳酸钙沉淀和氯化钠溶液,碳酸钙和D为盐酸发生反应得到溶液E为氯化钙溶液,经蒸发可得到氯化钙固体;由于碳酸钠过量,所以滤液中的物质有氯化钠和碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠,加入稀盐酸最合适,碳酸钠和稀盐酸生成氯化钠和水和二氧化碳,蒸发后最后的固体物质是氯化钠,
(1)根据上面的分析可知,B溶液是Na2CO3,加入过量Na2CO3溶液的原因是 使Ca2+沉淀完全,反应的离子方程式是 Ca2++CO32-═CaCO3↓,
故答案为:Na2CO3;使Ca2+沉淀完全;Ca2++CO32-═CaCO3↓;
(2)根据上面的分析,若要得到纯净的NaCl,还应补充的实验操作步骤是加入了过量的Na2CO3,滤液中加入足量盐酸,
故答案为:加入了过量的Na2CO3,滤液中加入足量盐酸;
(3)C沉淀为碳酸钙,其质量m1,则混合物中CaCl2的质量为$\frac{{m}_{1}}{100}×111$,混合物的质量为m2,则混合物中NaCl的质量为m2-$\frac{{m}_{1}}{100}×111$,所以混合物中NaCl和CaCl2的质量比为(m2-$\frac{{m}_{1}}{100}×111$):$\frac{{m}_{1}}{100}×111$=$\frac{{m}_{2}-1.11{m}_{1}}{1.11{m}_{1}}$,
故答案为:$\frac{{m}_{2}-1.11{m}_{1}}{1.11{m}_{1}}$.
点评 本题考查物质的分离、提纯知识,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握实验的原理和操作方法,为解答该题的关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | NaCl中含有杂质Na2SO4(适量氯化钡) | |
| B. | FeSO4 中含有杂质CuSO4(铁粉) | |
| C. | SO2中含有少量HCl气体(氢氧化钠溶液) | |
| D. | CO2中含有少量的CO(灼热的氧化铜) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 预期现象与结论 |
| 步骤1: | 部分固体不溶解 |
| 步骤2: | |
| 步骤3:继续步骤2中的(2),进行固液分离,用蒸馏水洗涤固体至洗涤液无色.取少量固体于试管中,滴加过量HCl后,静置,取上层清液,滴加适量H2O2,充分振荡后滴加KSCN. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加入较多NaHSO4的溶液中:Fe3+、Cl-、NO3-、Na+ | |
| B. | 通入大量CO2气体的溶液中:Na+、Ba2+、Cl-、NO3- | |
| C. | 通入大量NH3的溶液中:Ca2+、Na+、HCO3-、Cl- | |
| D. | 通入大量SO2气体的溶液中:Na+、SO32-、NH4+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | |
| C | D |
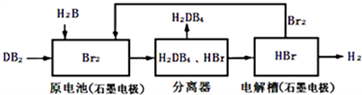
| 化学键 | H-H | Br-Br | H-Br |
| 键能(kJ/mol) | 436 | 194 | 362 |
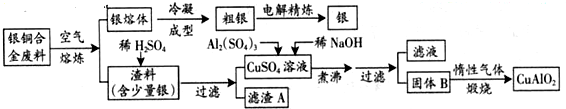
| 化学式 | Ag2SO4 | AgBr |
| 溶解度(g) | 0.796 | 8.4×10-6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com