
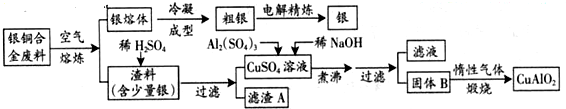
���� ���ɹ�������ͼ��֪�������ڿ���������ʱ��Cu�������������к���CuO������Ag���������м���������������CuO�����ᷴӦ�����˵õ�����ͭ��Һ���������ᣩ������AΪAg������Һ�м������������������ƣ��õ�����������������ͭ�������л�õ�CuO��Al2O3�����߷�Ӧ�õ�CuAlO2��
��1��δ���֮ǰ��Cu��OH��2��Al��OH��3������Al��OH��3��Cu��OH��2��ʼ�ֽ���¶ȷֱ�Ϊ450���80���жϲ������������������������Ӧ��
��2�����ݻ��ϼ�������������Լ�ԭ���غ�����ƽ��
��3������ͭԪ���غ㽨����ϵʽ��Cu��CuAlO2��������Ԫ���غ㽨����ϵʽ��Al2��SO4��3��2CuAlO2��������������ϵʽ���ͭ�������ɼ���Al2��SO4��3��Һ�������
�����������������ԣ�������л�ԭ�ԣ�����֮�䷢��������ԭ��Ӧ����ѧ����ʽΪ2FeCl3+H2S�T2FeCl2+S��+2HCl���ٸ�дΪ���ӷ�Ӧ����ʽ������Ȼ�����ʱ������ʧȥ���ӷ���������Ӧ����Fe3+�������ɫ��ѧ�����۲�����FeCl3����ѭ������ȷ����ʵ��������������ŵ㣮
��� �⣺���ɹ�������ͼ��֪�������ڿ���������ʱ��Cu�������������к���CuO������Ag���������м���������������CuO�����ᷴӦ�����˵õ�����ͭ��Һ���������ᣩ������AΪAg������Һ�м������������������ƣ��õ�����������������ͭ�������л�õ�CuO��Al2O3�����߷�Ӧ�õ�CuAlO2��
��1��δ���֮ǰ��Cu��OH��2��Al��OH��3��Al��OH��3��Cu��OH��2��ʼ�ֽ���¶ȷֱ�Ϊ450���80�棬��к�Cu��OH��2�ֽ��������ͭ����֪BΪAl��OH��3��CuO��������������������Ӧ��Al��OH��3+NaOH=NaAlO2+2H2O��
�ʴ�Ϊ��Al��OH��3��CuO��Al��OH��3+OH-=AlO2-+2H2O��
��2����ӦǰCuΪ+2�ۣ���Ӧ��Ϊ+1�����ϼ۽���1��Al���ϼ�û�б仯��������Ԫ�صĻ��ϼ����ߣ�������������Ӧǰ��Ϊ-2�ۣ���Ӧ��Ϊ0�����ϼ�����2�����ߵ���С��������2���ٸ���ԭ���غ�ã�4CuO+2Al2O3=4CuAlO2+O2����
�ʴ�Ϊ��4CuO+2Al2O3=4CuAlO2+O2����
��4���ɹ�ϵʽ��Cu��CuAlO2��n��CuAlO2��=$\frac{5.0��1000��64%}{64}$mol=50.0mol����CuAlO2Ϊ50.0mol���ɹ�ϵʽ��Al2��SO4��3��2CuAlO2��Al2��SO4��3=n��CuAlO2����$\frac{1}{2}$=25.0mol��������Ҫ���Ϊ$\frac{25.0mol}{1.0mol/L}$=25.0L��
�ʴ�Ϊ��25.0��
��4��FeCl3��H2S������ӦΪ2FeCl3+H2S=2FeCl2+2HCl+S�������ӷ���ʽΪ��2Fe3++H2S=2Fe2++S��+2H+��
�ʴ�Ϊ��2Fe3++H2S=2Fe2++S��+2H+��
��5������Ȼ�����ʱ��������������ʧȥ���ӷ���������Ӧ����Fe3+���缫��ӦʽΪFe2+-e-=Fe3+���ʴ�Ϊ��Fe2+-e-=Fe3+��
��6������ʵ��ԭ����֪�����������յõ���FeCl3��������������H2S���õ�ѭ�����ã��ʴ�Ϊ��FeCl3����ѭ�����ã�
���� �����Դӷ����л��������Ʊ�ͭ������ƷΪ�����������������Ʊ�ԭ������Ӧ�ã���Ŀ�Ѷ��еȣ��漰���ԭ�����������жϡ�������ԭ��Ӧ����д�Լ���ѧ�����֪ʶ������֪ʶ��϶ࡢ�ۺ��Խ�ǿ����ֿ���ѧ���ķ�����������������ѧʵ�顢��ѧ����������


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ǻ�Ϊͬλ�� | B�� | ԭ�Ӻ��е���������ͬ | ||
| C�� | ������ͬ�������� | D�� | 23595Am��23592U��3������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
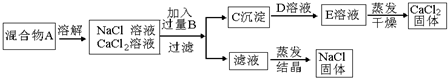
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al | B�� | Mg | C�� | Fe | D�� | Na |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
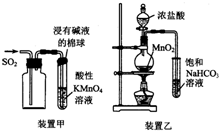
| A�� | ��װ�ü��ռ�SO2����֤��Ư���� | |
| B�� | ��װ������֤������ˮ��Ӧ���������� | |
| C�� | �ó���ʯ��ˮ�����մ���Һ��С�մ���Һ | |
| D�� | ��NaOH��Һ��ȥ���л��е��������ӣ���Ӧ���Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
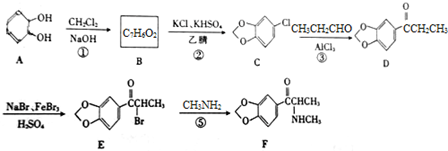
 ��
�� ����ṹ��ʽ����
����ṹ��ʽ���� ���ĺϳ�·�ߣ�
���ĺϳ�·�ߣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ���� | ��ʼ������pHֵ | ��ȫ������pHֵ |
| Fe��OH��3 | 2.7 | 3.7 |
| Al��OH��3 | 3.4 | 4.4 |
| Cr ��OH��3 | 4.6 | 5.9 |
| Fe��OH��2 | 7.5 | 9.7 |
| Bi��OH��3 | 0.7 | 4.5 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
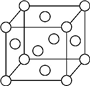 A��B��X��Y��Z��Ԫ�����ڱ�ǰ�������еij���Ԫ�أ�ԭ��������������AԪ�ؿ��γ���Ȼ��Ӳ�����ĵ��ʣ�B��Aͬ���ڣ�����������δ�ɶԵ��ӣ�Xԭ�ӵĵ�һ�����������ĵ����ֱܷ��ǣ�I1=578kJ/mol��I2=1 817kJ/mol��I3=2 745kJ/mol��I4=11 575kJ/mol�����³�ѹ�£�Y�����ǹ��壬�����������γ��������Ҫ���ʣ�Z��һ��ͬλ�ص�������Ϊ63��������Ϊ34����ش��������⣺
A��B��X��Y��Z��Ԫ�����ڱ�ǰ�������еij���Ԫ�أ�ԭ��������������AԪ�ؿ��γ���Ȼ��Ӳ�����ĵ��ʣ�B��Aͬ���ڣ�����������δ�ɶԵ��ӣ�Xԭ�ӵĵ�һ�����������ĵ����ֱܷ��ǣ�I1=578kJ/mol��I2=1 817kJ/mol��I3=2 745kJ/mol��I4=11 575kJ/mol�����³�ѹ�£�Y�����ǹ��壬�����������γ��������Ҫ���ʣ�Z��һ��ͬλ�ص�������Ϊ63��������Ϊ34����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
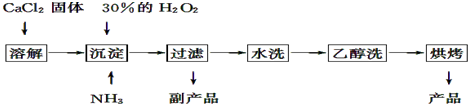
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com