
【题目】2 mol A与2 mol B混合于2 L的密闭容器中,发生反应:2A(g)+3B(g)![]() 2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
A.v(C)=0.2 mol·L-1·s-1
B.z=3
C.B的转化率为25%
D.C平衡时的浓度为0.5 mol·L-1
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】(1)用下列物质的编号填空:
①NaCl晶体 ②盐酸 ③HCl ④熔融KCl ⑤蔗糖 ⑥铜 ⑦CO2 ⑧稀硫酸 ⑨KOH溶液;
以上物质中属于电解质的是___________,属于非电解质的是___________,能导电的是___________。
(2)某烧杯中盛有100 mLHCl和CuCl2的混合液,混合溶液中c(HCl)=2 mol/L,c(CuCl2)=1 mol/L。请回答下列问题:
①该混合溶液中,n(H+)=________mol;c(Cl-)=__________mol/L。
向上述烧杯中加入足量铁粉并使之充分反应。写出有关的离子方程式:
② ; 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用12moL·L-1浓盐酸配制250mi-0.1 mol.L-1的盐酸溶液时,下列实验操作会使配得的溶液浓度偏大的是( )
A. 用量筒量取浓盐酸时俯视读数
B. 最后定容时仰视读数
C. 将浓盐酸倒入烧杯后,用水洗涤量筒2—3次,并将洗涤液一并倒入容量瓶中
D. 定容后把容量瓶倒置摇匀,发现液面低于刻度,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中进行氢气与碘(气态)合成HI的反应,下列说法能表明反应达到平衡的是
A.气体的平均分子量不再变化 B.反应的平衡常数不变
C.(H2) = 2 (HI) D.气体的颜色不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,两种气体的体积如果不相同,其主要原因是
A.气体的分子大小不同 B.气体分子间的平均距离不同
C.气体的性质不同 D.气体的物质的量不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素A、B、C、D、E原子序数依次增大,A是周期表中原子半径最小的元素,B是形成化合物种类最多的元素,C原子的最外层电子数是次外层电子数的3倍,D是同周期中金属性最强的元素,E的负一价离子与C的某种氢化物分子含有相同的电子数.
(1)A、C、D形成的化合物中含有的化学键类型为 .
(2)已知:
①E﹣E→2E△H=+a kJmol﹣1;
②2A→A﹣A△H=﹣b kJmol﹣1;
③E+A→A﹣E△H=﹣c kJmol﹣1;
写出298K时,A2与E2反应的热化学方程式 .
(3)在某温度下、容积均为2L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2A2(g)+BC(g)X(g)△H=﹣a kJmol﹣1(a>0,X为A、B、C三种元素组成的一种化合物).初始投料与各容器达到平衡时的有关数据如下:
实验 | 甲 | 乙 | 丙 |
初始投料 | 2molA2、1molBC | 1molX | 4molA2、2molBC |
平衡时n(X) | 0.5mol | n2 | n3 |
反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
体系的压强 | P1 | P2 | P3 |
反应物的转化率 | α1 | α2 | α3 |
①在该温度下,假设甲容器从反应开始到平衡所需时间为4min,则A2的平均反应速率v(A2)= .
②计算该温度下此反应的平衡常数K= .
③三个容器中的反应分别达平衡时各组数据关系正确的是 (填字母).
A.α1+α2=1
B.Q1+Q2=a
C.α3<α1
D.P3<2P1=2P2
E.n2<n3<1.0mol
F.Q3=2Q1
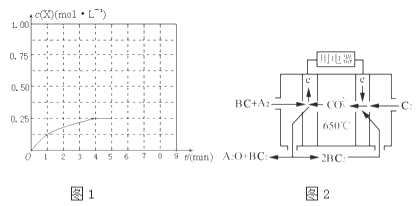
④在其他条件不变的情况下,将甲容器的体系体积压缩到1L,若在第8min达到新的平衡时A2的总转化率为75%,请在图1中画出第5min到新平衡时X的物质的量浓度的变化曲线.
(4)熔融碳酸盐燃料电池(MCFC)是一种高温燃料电池,被称为第二代燃料电池.目前已接近商业化,示范电站规模已达2MW,从技术发展趋势来看,是未来民用发电的理想选择方案之一.现以A2(g)、BC(g)为燃料,以一定比例Li2CO3和Na2CO3低熔混合物为电解质.写出碳酸盐燃料电池(MCFC)正极电极反应式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列化合物:①NaCl、②NaOH、③HCl、④NH4Cl、⑤CH3COONa、⑥CH3COOH、⑦NH3·H2O、⑧H2O。回答下列问题。
(1)NH4Cl溶液显________性,用离子方程式表示原因______________,其溶液中离子浓度大小顺序为________________
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=__________mol/L,在pH=3的CH3COOH溶液中,水电离出来的c(H+)=__________mol/L。
(3)已知纯水中存在如下平衡:H2O+H2O![]() H3O++OH- △H>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是______(填字母序号)。
H3O++OH- △H>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是______(填字母序号)。
A.向水中加入NaHSO4固体 B.向水中加Na2CO3固体
C.加热至100℃ D.向水中加入(NH4)2SO4固体
(4)若将等pH、等体积的②NaOH和⑦NH3·H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等,则m______n(填“<”、“>”或“=”)。
(5)除④⑦⑧外,若其余5种溶液的物质的量浓度相同,则这5种溶液按pH由大到小的顺序为:_________________(填序号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实,不能用氢键知识解释的是 ( )
A. 水分子高温下也很稳定
B. 水和乙醇可以完全互溶
C. 冰的密度比液态水的密度小
D. 液态氟化氢的化学式有时可以写成(HF)n的形式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、M、N四种金属,有如下相关信息,据此分析,这四种金属的活动性由强到弱的顺序是( )
① X + Y(NO3)2 = X(NO3)2 + Y
② X 与H2SO4(稀)不反应
③ M + H2SO4(稀) =MSO4 + H2↑
④ N + MSO4 = NSO4 + M
A. N>M>X>Y B. Y>X>M>N C. X>Y>M>N D.N>M>Y>X
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com