
【题目】在恒容密闭容器中进行氢气与碘(气态)合成HI的反应,下列说法能表明反应达到平衡的是
A.气体的平均分子量不再变化 B.反应的平衡常数不变
C.(H2) = 2 (HI) D.气体的颜色不再变化
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.硫在空气中的燃烧产物是二氧化硫,在纯氧中的燃烧产物是三氧化硫
B.二氧化碳和CaCl2溶液反应,生成白色沉淀
C.二氧化硅和烧碱溶液反应,使溶液的碱性一定减弱
D.在常温下,浓硫酸不与铜反应,是因为铜被钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 设NA为阿伏加德罗常数,下列说法正确的是( )
A.标准状况下,5.6L CCl4含有的分子数为0.25NA
B.标准状况下,14 g氮气含有的核外电子数为5NA
C.标准状况下,22.4 L任意比的氢气和氯气的混合气体中含有的分子总数均为NA
D.在标准状况下,18gH2O所含有的电子数不是10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国首个空间实验室——“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),它是一种将水电解技术与氢氣燃料电池技术相结合的可充电电池。下图为RFC工作原理示意图,a、b、c、d均为Pt电极。 下列说法正确的是( )
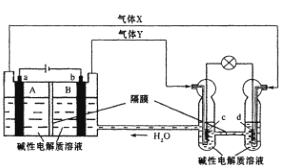
A. B区的OH-通过隔膜向a电极移动,A 区pH增大
B. 图中右管中的OH-通过隔膜向c电极移动,d电极上发生还原反应
C. c是正极,电极上的电极反应为2H++2e-=H2↑
D. 当有lmol电子转移时,b电极产生气体Y的体积为11.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2 mol A与2 mol B混合于2 L的密闭容器中,发生反应:2A(g)+3B(g)![]() 2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
A.v(C)=0.2 mol·L-1·s-1
B.z=3
C.B的转化率为25%
D.C平衡时的浓度为0.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大。A与D、C与E分别同主族,D、E、F同周期,B原子的最外层电子数是内层电子数的2.5倍,A与C形成的常见化合物在常温下为液态。
(1)元素A在周期表中的位置是________;D、E、F形成的简单离子中半径最大的是_______(填离子符号)。
(2)常温下,F的单质能与由A、C、D三种元素组成的一种常见化合物发生反应,该反应的化学方程式为________。
(3) E与F的最简单气态氢化物中稳定性较强的是________(填化学式)。
(4)元素B和元素F能形成一种化合物BF3,其中F显+1价。BF3能发生水解反应生成一种弱碱和一种弱酸,写出该反应的化学方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O反应中
(1) 是还原剂, 是还原产物。
(2) 该反应的离子方程式为: 。
(3) 用双线桥法表示此氧化还原反应电子转移的方向和数目
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(4)NA表示阿伏伽德罗常数,若产生标准状况下的气体的体积为2.24 L,则反应过程中转移电子的数目为 ,被氧化的HCl的质量为 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com